Clear Sky Science · pl
Synteza i biologiczna ocena kompleksów zasady Schiffa z ibuprofenem/o‑waniliną o działaniu przeciwzapalnym, przeciwnowotworowym i przeciw SARS‑CoV‑19
Dlaczego warto unowocześniać znany środek przeciwbólowy
Ibuprofen jest jednym z najczęściej stosowanych na świecie leków przeciwbólowych i przeciwgorączkowych, lecz długotrwałe stosowanie może podrażniać żołądek, a sam lek nie był projektowany do zwalczania zakażeń, nowotworów ani nowych wirusów. W tym badaniu chemicy przeprojektowali ibuprofen, łącząc go z naturalną cząsteczką o zapachu wanilii, a następnie przyłączyli różne metale. W rezultacie powstała rodzina nowych związków, które działają nie tylko jako leki przeciwbólowe, lecz także jako potencjalne antybiotyki, środki przeciwnowotworowe, leki przeciwzapalne, a nawet blokery kluczowego enzymu SARS‑CoV‑2, dostarczając jednocześnie wskazówek, jak projektować „mądrzejsze” leki z powszechnie stosowanych substancji.
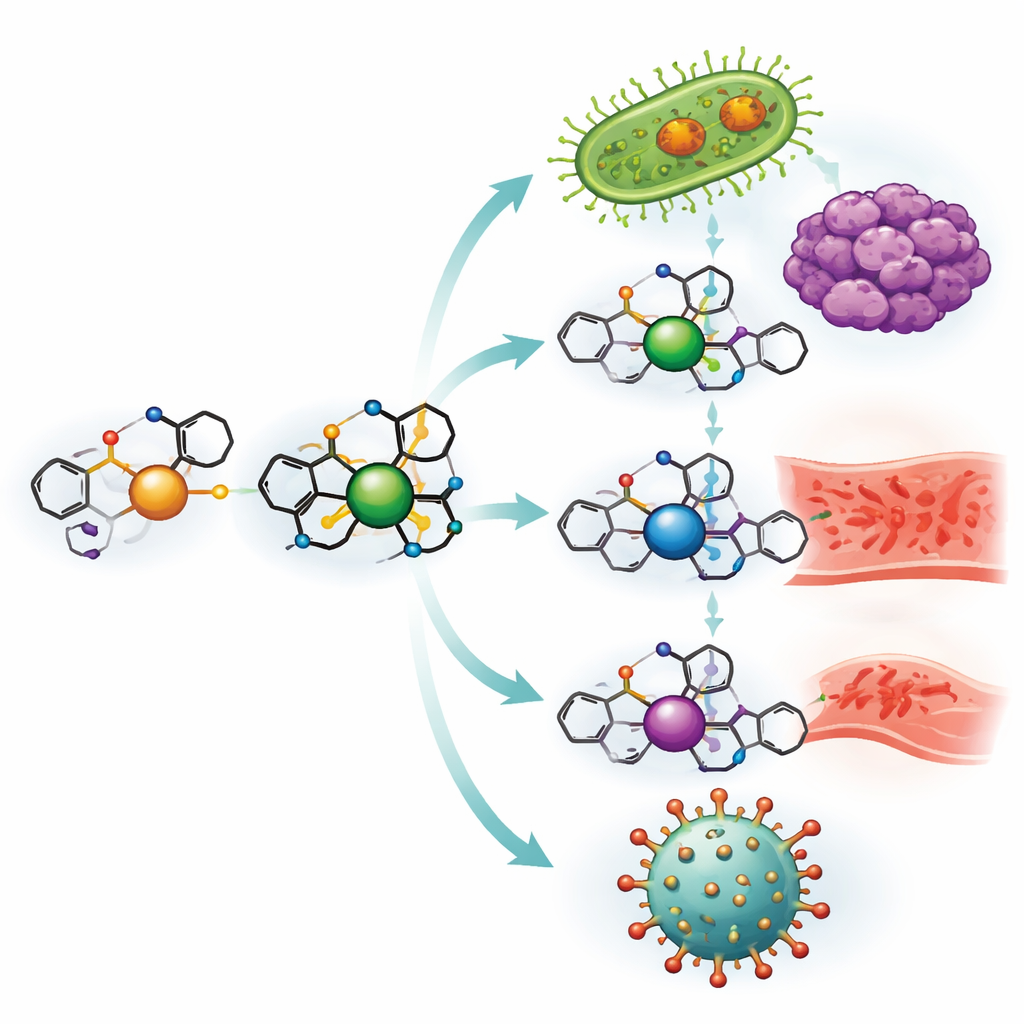
Budowanie nowych cząsteczek o cechach leków z ibuprofenu
Zespół rozpoczął od przekształcenia ibuprofenu w bardziej uniwersalny blok budulcowy, a następnie połączył go z o‑waniliną, chemicznym krewnym związku nadającego wanilii smak. Razem tworzą ligand typu „zasada Schiffa” — w praktyce dostosowany „uchwyt”, który może wiązać jony metali. Ten ligand połączono osobno z solami miedzi, niklu, cynku i wanadu, uzyskując cztery różne kompleksy metali. Dokładne testy laboratoryjne, w tym pomiary topnienia, pochłaniania światła, właściwości magnetycznych i struktury krystalicznej, potwierdziły, jak ligand otacza każdy metal i jak stabilne są powstałe kompleksy, nawet w wysokich temperaturach i w szerokim zakresie kwasowości.
Jak kompleksy wchodzą w interakcje z komórkami i DNA
Ponieważ działanie leku często zależy od sposobu, w jaki oddziałuje z celami biologicznymi, badacze zbadali, jak nowe kompleksy wiążą się z DNA i żywymi komórkami. W doświadczeniach probówkowych szczególnie kompleks miedzi silnie wiązał nici DNA i potrafił je uszkadzać lub „ ciąć”, co jest zachowaniem często obserwowanym u silnych środków przeciwnowotworowych i przeciwbakteryjnych. Po przetestowaniu na ludzkich liniach komórkowych nowotworów piersi, jelita grubego i wątroby wszystkie cztery kompleksy były bardziej toksyczne dla komórek nowotworowych niż sam ligand ibuprofenowy, a kompleks miedzi zbliżał się skutecznością do leku chemioterapeutycznego winblastyny przy podobnych dawkach.
Walką z zarazkami, grzybami i stanem zapalnym
Te same związki poddano próbom przeciwko powszechnym patogennym mikrobom, w tym bakteriom Gram‑dodatnim i Gram‑ujemnym oraz dwóm problematycznym grzybom. Ponownie kompleksy metaliczne przewyższały wolny ligand, a liderem była miedź, silnie hamująca zarówno bakterie, jak i grzyby. Autorzy tłumaczą to teorią chelatacji: gdy metal jest związany przez ligand, jego ładunek jest częściowo ekranowany, a cały kompleks staje się bardziej lipofilowy, co ułatwia mu przenikanie przez błony mikroorganizmów i zaburzanie istotnych enzymów. W prostym teście przeciwzapalnym opartym na denaturacji białka jajowego uszkodzonego przez ciepło, nowe kompleksy również skuteczniej zmniejszały denaturację białka niż sam ibuprofen, co sugeruje, że mogłyby łagodzić procesy zapalne przy niższych dawkach.
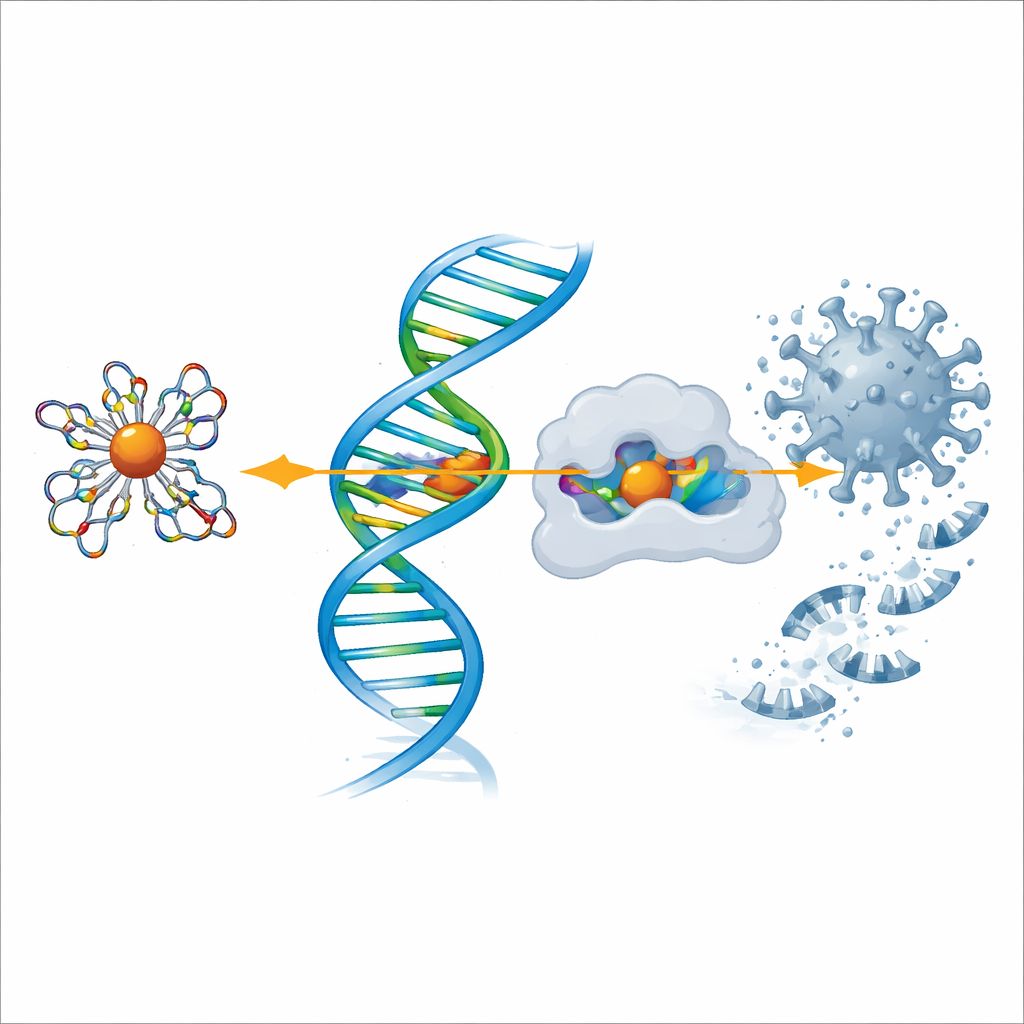
Badanie działania przeciw COVID‑19 i enzymom bólu
Aby zbadać potencjał przeciwwirusowy, zespół wykorzystał modelowanie komputerowe do dokowania liganda i każdego kompleksu metalicznego w trójwymiarowych kształtach dwóch kluczowych białek: głównej proteazy SARS‑CoV‑2, której wirus używa do rozcinania swoich poliobiałek, oraz cyklooksygenazy‑2 (COX‑2), enzymu zaangażowanego w ból i stan zapalny. Symulacje wykazały, że kompleksy, szczególnie te miedzi i cynku, dobrze dopasowują się do aktywnych kieszeni tych białek i tworzą wiele stabilizujących oddziaływań. Im bardziej ujemna obliczona energia wiązania, tym silniejsze przewidywane wiązanie, i ponownie kompleks miedzi wyróżniał się, a tuż za nim plasowały się cynk i nikiel, co potwierdza obserwacje laboratoryjne dotyczące działania przeciwzapalnego i przeciwbakteryjnego.
Co to może znaczyć dla przyszłych leków
Podsumowując, praca pokazuje, że znany lek dostępny bez recepty można przekształcić w wielozadaniowe narzędzie chemiczne, łącząc go z starannie dobranym partnerem organicznym i odpowiednim jonem metalu. Spośród czterech testowanych metali miedź dała najbardziej obiecujący kandydat, o silnym działaniu antybakteryjnym, przeciwgrzybiczym, przeciwnowotworowym, przeciwzapalnym oraz przewidywanym komputerowo działaniu przeciw SARS‑CoV‑2, podczas gdy nikiel i cynk wykazywały nieco łagodniejsze, ale nadal godne uwagi efekty. Chociaż wyniki te dotyczą etapów laboratoryjnych i modelowania komputerowego, wskazują one strategię polegającą na „unowocześnianiu” codziennych leków poprzez tworzenie ukierunkowanych kompleksów metali, które mogą działać przy niższych dawkach i na szersze spektrum chorób niż leki wyjściowe.
Cytowanie: Abdel-Rahman, L.H., El-ezz, D.A., Abdel-Mawgoud, AM.M. et al. Synthesis and biological evaluation of ibuprofen/o-vanillin Schiff base complexes with anti-inflammatory, anti-proliferative and anti-SARS-COV-19 activities. Sci Rep 16, 8501 (2026). https://doi.org/10.1038/s41598-026-38270-8
Słowa kluczowe: pochodne ibuprofenu, kompleksy lek‑metal, środki przeciwnowotworowe, terapia przeciwbakteryjna, proteaza COVID‑19