Clear Sky Science · pl
Strukturalne podstawy transportu prostaglandyn i leków przez SLCO2A1
Jak molekularny strażnik kształtuje działanie leków i hormonów
Wiele codziennych leków i cząsteczek podobnych do hormonów musi przejść przez drobne bramki w naszych komórkach, zanim będą mogły zadziałać. Artykuł opisuje jedną taką bramkę — białko o nazwie SLCO2A1, które pomaga transportować silne sygnalizujące lipidy zwane prostaglandynami oraz kilka powszechnie stosowanych leków do wnętrza komórek. Odkrywając trójwymiarową strukturę tego białka i sposób, w jaki chwyta swój ładunek, badacze wyjaśniają, dlaczego niektóre leki są przenoszone, podczas gdy inne tylko blokują bramę. Te ustalenia mogą ukierunkować bezpieczniejsze projektowanie leków oraz nowe terapie chorób związanych z zapaleniem, bólem, schorzeniami jelit i zaburzeniami gojenia ran.
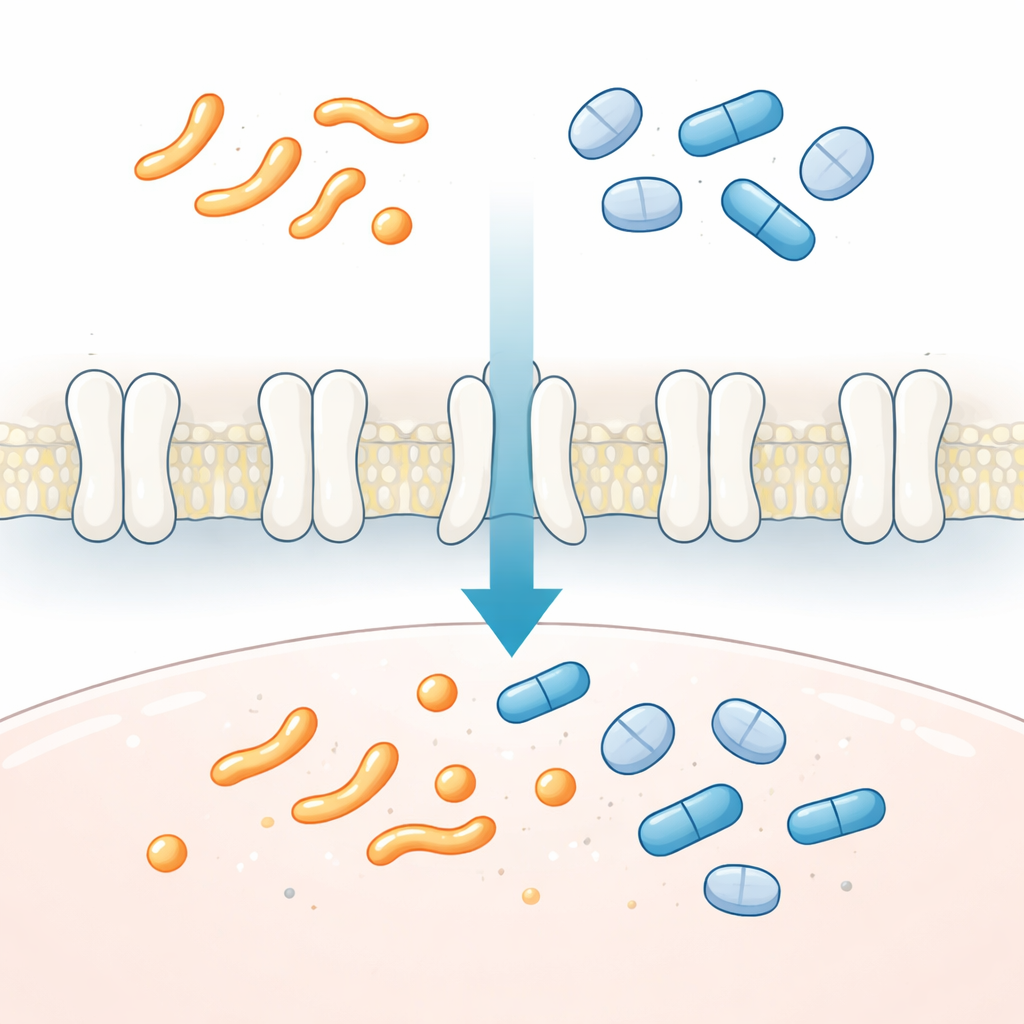
Kontroler ruchu w organizmie dla sygnałów bólu i zapalenia
Prostaglandyny to krótkożyjące, hormonopodobne lipidy, które kontrolują zapalenie, ból, gorączkę, przepływ krwi i rozwój narządów. Działają blisko miejsca powstania i muszą być szybko usunięte po wykonaniu zadania. SLCO2A1 znajduje się w błonie komórkowej i pomaga wyciągać prostaglandyny oraz spokrewnione cząsteczki, takie jak tromboksany, z płynu zewnątrzkomórkowego do wnętrza komórek, gdzie są rozkładane. Gdy ten transport zawodzi, poziomy prostaglandyn mogą pozostać nieprawidłowo wysokie. Wrodzone usterki w SLCO2A1 wiązano z rzadkimi schorzeniami nadmiernego wzrostu kości i skóry, przewlekłymi chorobami jelit oraz słabym gojeniem wrzodów. Ponieważ prostaglandyny i wiele powszechnie używanych leków korzysta z tej samej drogi do komórek, zrozumienie działania SLCO2A1 jest kluczowe do przewidywania efektów i skutków ubocznych leków w całym organizmie.
Obserwacja bramy w skali atomowej
Aby ustalić, jak SLCO2A1 rozpoznaje i przemieszcza swoje ładunki, zespół użył krioelektronowej mikroskopii elektronowej — techniki obrazowania flash‑zamrożonych białek z niemal atomową rozdzielczością. Badali blisko spokrewnioną wersję transportera pochodzącą od szczura, która zachowuje się bardzo podobnie do ludzkiej. Utrwalili struktury białka związane z dwoma naturalnymi prostaglandynami oraz z czterema lekami stosowanymi w leczeniu astmy, nadciśnienia, stanów zapalnych i choroby Parkinsona. We wszystkich tych ujęciach SLCO2A1 ukazuje się jako pęknięcie dwunastu helis przecinających błonę, tworzące centralną jamę otwartą na zewnątrz komórki. Prostaglandyny leżą głęboko w tej jamie: ich pierścieniowe rdzenie znajdują się blisko skupiska kluczowych aminokwasów, a ich tłuszczowe ogony wchodzą w przeważnie oleistą szczelinę odpowiadającą ich hydrofobowej naturze.
Chwyt-klucz, który wybiera, co przepuszczać
Porównując struktury i prowadząc długie symulacje komputerowe, badacze zidentyfikowali cechy pozwalające SLCO2A1 odróżniać prawdziwy ładunek od podobnych cząsteczek. Dodatnio naładowany aminokwas, arginina 561, oraz sąsiednie tryptofan i fenyloalanina tworzą kluczowy „chwyt” dla ujemnie naładowanego końca prostaglandyn. Gdy zespół mutował te reszty, transport w dużej mierze ustawał, co pokazuje krytyczne znaczenie tego kontaktu. Otaczająca jama jest przeważnie hydrofobowa, faworyzując oleiste, lipofilne cząsteczki, i zawiera „pasmo” działające jako punkt obrotu podczas zmiany kształtu białka. Dwa leki, zafirlukast i losartan, są faktycznie transportowane, ponieważ naśladują sposób, w jaki prostaglandyny prezentują grupę ujemną tej argininie, jednocześnie angażując te same hydrofobowe powierzchnie. W przeciwieństwie do nich przeciwzapalny fentiazac i lek na Parkinsona tolkapon wiążą się mniej ciasno i nie stabilizują właściwej pozy, więc blokują miejsce zamiast być przenoszone.
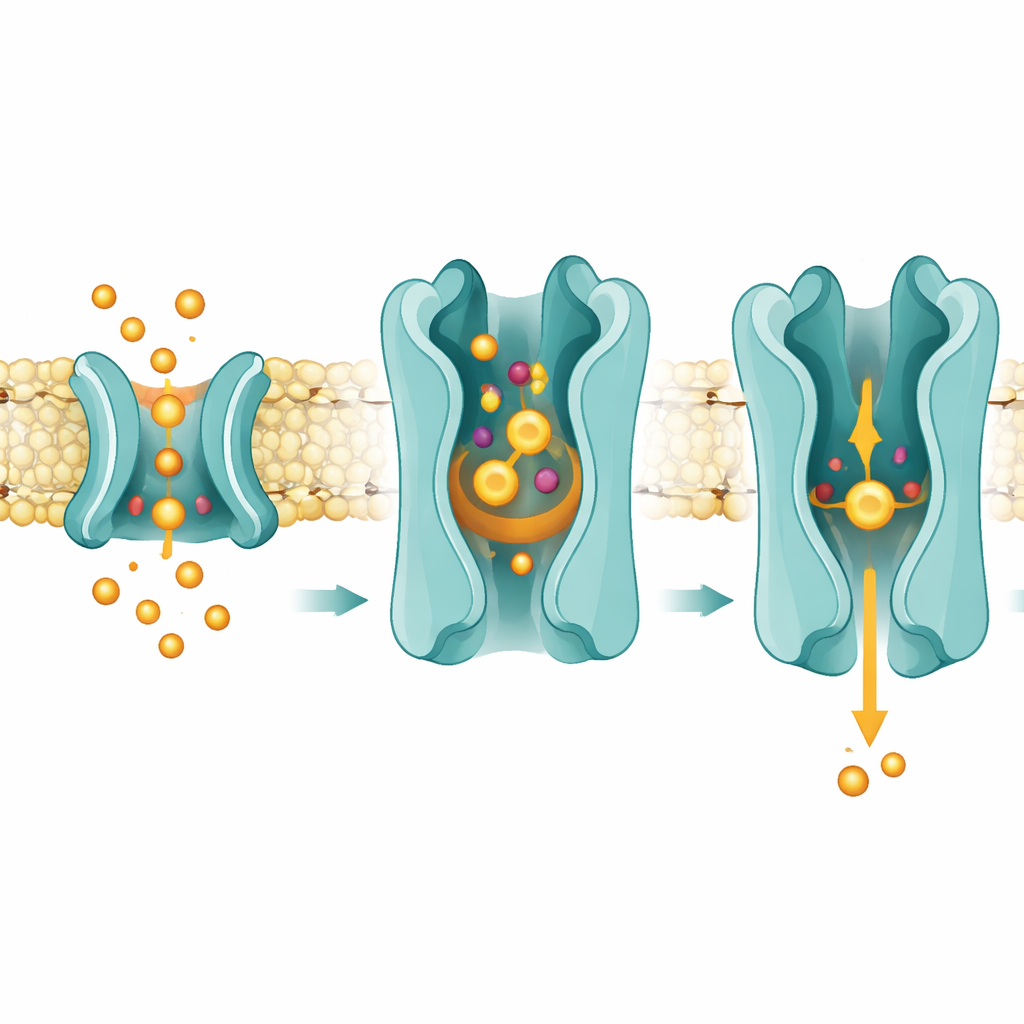
Boczne wejście przez błonę
Struktury sugerują również, że prostaglandyny docierają do SLCO2A1 nie z otwartej wody, lecz przesuwając się bocznie przez tłustą warstwę błony. Badacze zaobserwowali gęstości zgodne z lipidopodobnymi cząsteczkami umieszczonymi w bocznym otworze między dwiema helisami, tuż nad miejscem wiązania prostaglandyn. Mutacje powodujące choroby i testy funkcjonalne wskazały ten obszar jako kluczowy dla transportu. Proponowany mechanizm zakłada, że prostaglandyny najpierw rozpuszczają się w zewnętrznej warstwie błony, a następnie wślizgują się do transportera przez to boczne wejście. Po związaniu w centralnej kieszeni zakłócają zachowaną wiązkę soli między argininą 561 a resztą glutaminianu, co z kolei pomaga wyzwolić przejście transportera z konfiguracji otwartej na zewnątrz do otwartej do wnętrza, uwalniając prostaglandynę w kierunku wewnętrznej warstwy błony i wnętrza komórki.
Dlaczego to ma znaczenie dla leków i chorób
Dla laika główne przesłanie jest takie, że SLCO2A1 działa jak precyzyjnie wyregulowana brama, która kontroluje, jak szybko chemiczne sygnały bólu, gorączki i zapalenia są wyłączane, oraz jak niektóre leki wnikają do komórek. Badanie pokazuje w detalach molekularnych, jak brama rozpoznaje prostaglandyny i dlaczego tylko niektóre leki mogą się nimi poruszać, podczas gdy inne zacinają drzwi. Mapując kluczowe punkty styku i boczną drogę wejścia przez błonę, praca dostarcza planu pozwalającego projektować nowe leki, które albo efektywnie korzystają z tego systemu transportowego, albo celowo go blokują w kontrolowany sposób. Ostatecznie taka wiedza może poprawić terapie chorób zapalnych, zaburzeń jelit związanych z nierównowagą prostaglandyn oraz schematy leczenia, w których interakcje z transporterem obecnie powodują nieprzewidywalne odpowiedzi.
Cytowanie: Joshi, C., Deme, J.C., Nakamura, Y. et al. Structural basis for prostaglandin and drug transport via SLCO2A1. Nat Commun 17, 2285 (2026). https://doi.org/10.1038/s41467-026-70227-3
Słowa kluczowe: transport prostaglandyn, transportery leków, SLCO2A1, białka błonowe, struktura cryo-EM