Clear Sky Science · pl
Katalityczna asymetryczna funkcjonalizacja estry boranowych bicyclo[1.1.0]butanu umożliwiona przez migrację 1,2-tlenową
Dlaczego małe pierścienie kwadratowe mają znaczenie
Chemicy chętnie budują nowe leki i materiały, składając małe cząsteczkowe elementy jak klocki Lego. Czteroczłonowe pierścienie węglowe zwane cyklobutanami są szczególnie cenione, ponieważ mieszczą dużo energii i specyficznej geometrii w niewielkiej objętości, co może zmieniać zachowanie leku w organizmie. Niniejszy artykuł opisuje nowy sposób wytwarzania tych pierścieni w bardzo kontrolowanej, „jednoręcznej” (chiralnej) formie, wykorzystując sprytne przemieszczenie grupy zawierającej tlen z jednego atomu na drugi. Praca ta otwiera możliwości projektowania bardziej złożonych i precyzyjnych cząsteczek dla farmaceutyków i zaawansowanych materiałów.
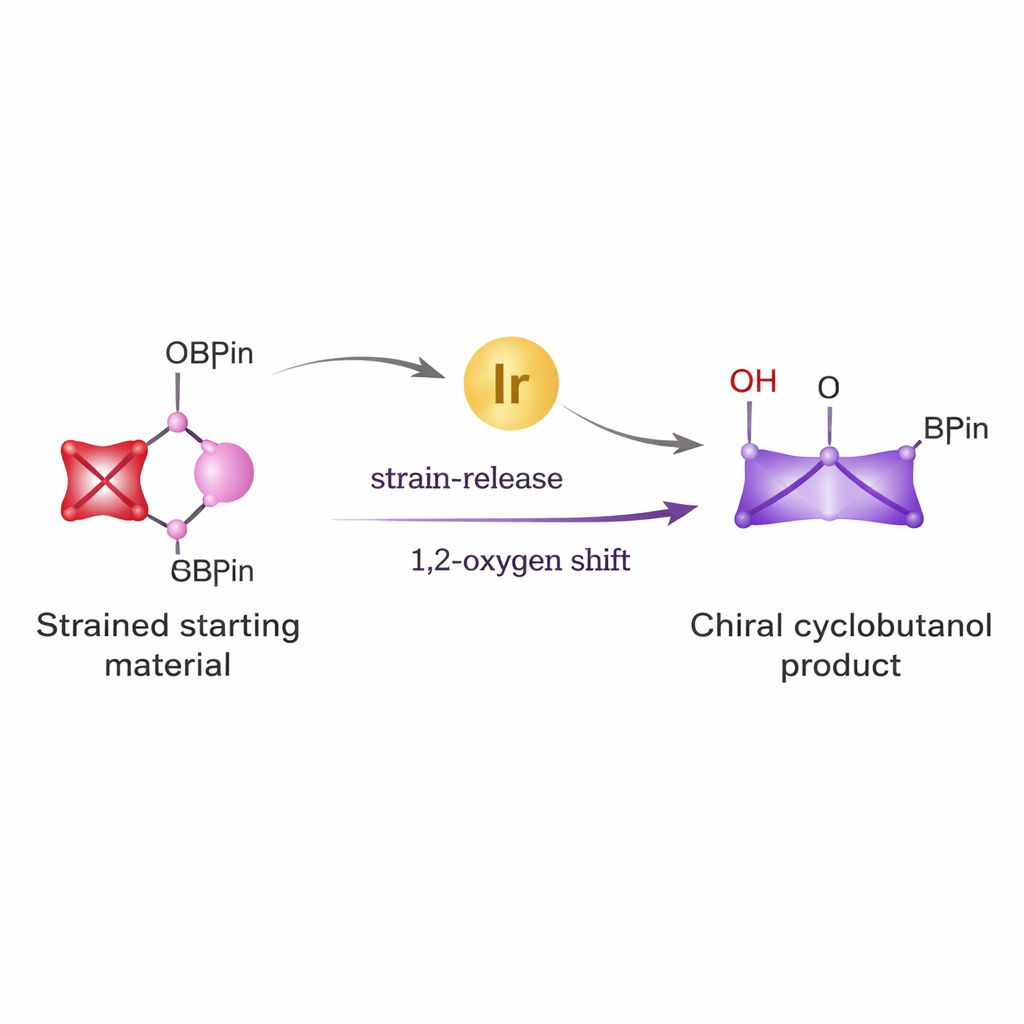
Od prostych cegiełek do silnych pierścieni
Cyklobutany występują w szeregu środków przeciwwirusowych, kandydatach na leki przeciwnowotworowe i innych bioaktywnych molekułach. Budowanie ich w dokładnie wymaganym ułożeniu trójwymiarowym było jednak trudne. Tradycyjne metody często wymagają ostrych reagentów i dają mieszaniny enancjomerów trudnych do rozdzielenia. Autorzy postanowili rozwiązać ten problem, łącząc dwa potężne pomysły: nietypową reaktywność małego, silnie spolaryzowanego pierścienia bicyclo[1.1.0]butanu oraz wszechstronność estrów boranowych — dobrze znanej klasy reagentów szeroko stosowanych w chemii sprzęgania w celu tworzenia wiązań węgiel–węgiel.
Przełożenie wad na nową ścieżkę reakcji
W standardowych reakcjach sprzęgania katalizowanych metalami, estry boranowe tworzą pośredni kompleks z alkoholoksydem (zasadą na bazie tlenu). Ten kompleks niemal zawsze podąża utartą ścieżką zwaną transmetalacją, która prowadzi bezpośrednio do nowych wiązań węgiel–węgiel lub węgiel–halogen. Ta „domyślna” droga utrudniała badanie innych możliwości, takich jak przemieszczenie samej grupy tlenowej. Zespół zauważył, że startując od estru boranowego bicyclo[1.1.0]butanu, wbudowane naprężenie małego pierścienia można wykorzystać do przeforsowania odstępstwa od zwykłej ścieżki. Parując ten naprężony system z katalizatorem irydu i starannie dobranym ligandem chiralnym, badacze mieli nadzieję nakłonić grupę tlenową do kontrolowanej migracji, podczas gdy pierścień otwiera się i ponownie zamyka do postaci cyklobutanu.
Krokowy taniec kierowany naprężeniem
Doświadczenia potwierdziły skuteczność tej strategii. Używając alkoholoksydów litowych otrzymanych z różnorodnych alkoholi — w tym cukrów, terpenów, steroidów i prostych alkoholi alifatycznych — autorzy przekształcili estry boranowe bicyclo[1.1.0]butanu w produkty cis-cyklobutanoli o wysokych wydajnościach i doskonałej kontroli chiralności. Katalizator irydu najpierw tworzy reaktywny kompleks allylowy z partnerem w postaci węglanu allylowego. Ten kompleks następnie atakuje naprężony system bicyclo[1.1.0]butanu, tworząc nowe wiązanie węgiel–węgiel w miarę otwierania się małego pierścienia. Co istotne, zamiast natychmiast podążać zwykłą drogą transmetalacji, powstały pośrednik zawierający bor ulega subtelnej rotacji wiązania węgiel–bor, ustawiając dołączoną grupę tlenową tak, by mogła czysto przesunąć się na sąsiedni atom węgla. Ta migracja 1,2-tlenowa utrwala pożądaną konfigurację cis na nowym pierścieniu cyklobutanowym.
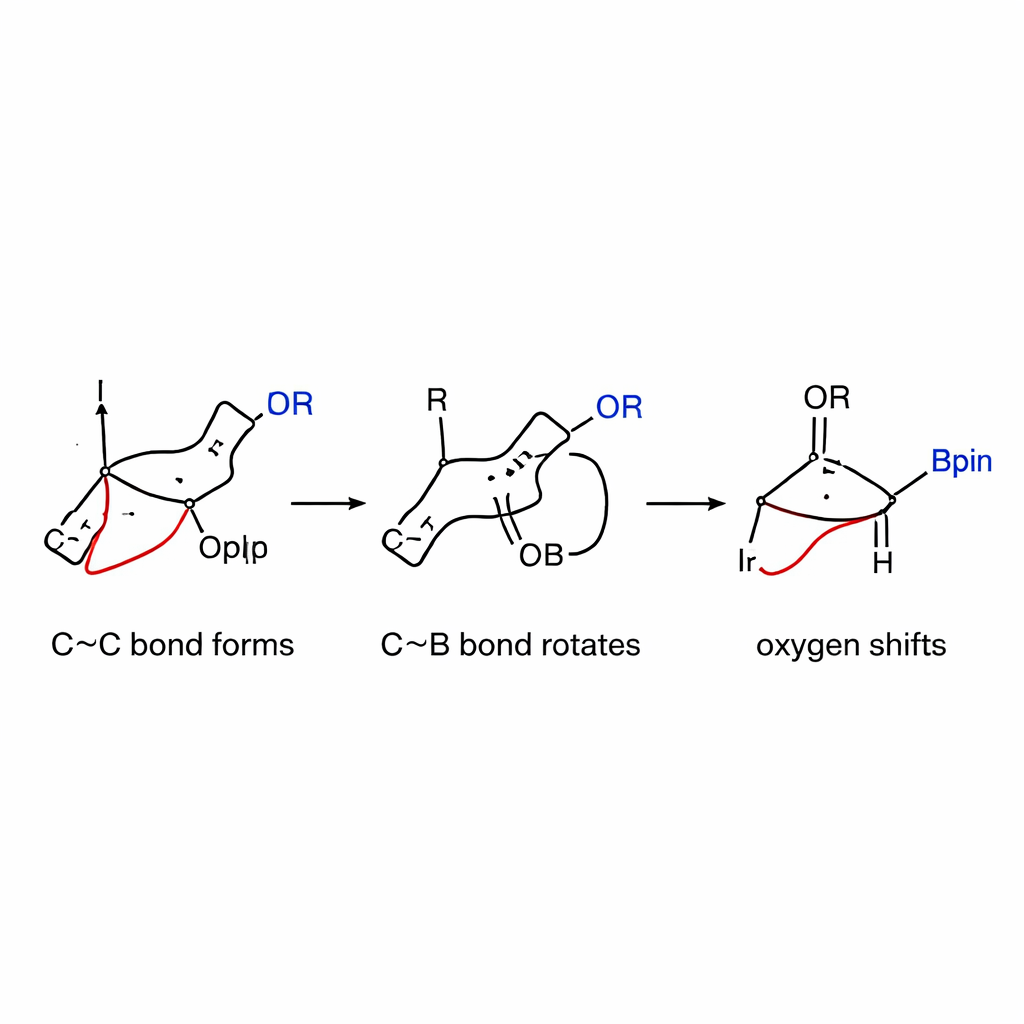
Zajrzenie pod maskę mechanizmu
Aby zrozumieć, dlaczego reakcja jest tak selektywna, autorzy połączyli pomiary kinetyczne ze szczegółowymi symulacjami komputerowymi. Stwierdzili, że wolnym, kontrolującym szybkość etapem jest początkowe tworzenie wiązania węgiel–węgiel między gatunkiem iryd–allyl a naprężonym kompleksem boronianowym, a nie wcześniejsza aktywacja węglanu allylowego. Testy elektronowe wykazały, że partnerzy allylowi stabilizujący ładunek dodatni reagują szybciej, co wspiera mechanizm obejmujący powstawanie częściowo naładowanego pośrednika. Obliczenia ujawniły ponadto, że rotacja wokół wiązania węgiel–bor — wcześniej uważana za trudną — ma w tym układzie zaskakująco niski barierę energetyczną dzięki zgromadzonemu naprężeniu pierścienia. Gdy rotacja wyrówna grupę tlenową, przesunięcie 1,2 przebiega gładko i preferencyjnie prowadzi do produktu cis zamiast częściej spotykanej formy trans.
Nowe narzędzia do kształtowania przyszłych leków
Ponad dowodem mechanistycznym, reakcja dostarcza uniwersalnych produktów. Cyklobutanole zachowują jednostkę estru boranowego, którą można przekształcić w wiele innych grup funkcyjnych przy użyciu ugruntowanej chemii. Autorzy zaprezentowali liczne „modyfikacje na późnym etapie”, takie jak hydrogenacja, utlenianie, metateza olefin i dalsze sprzęgania, przy jednoczesnym zachowaniu precyzyjnego ułożenia trójwymiarowego pierścienia. Mówiąc prosto, praca ta zamienia kiedyś problematyczną boczną ścieżkę — migrację tlenu w kompleksach boronianowych — w potężne narzędzie syntetyczne. Dzięki wykorzystaniu naprężenia pierścienia i precyzyjnie dostrojonego katalizatora irydu, badacze dostarczają chemikom wiarygodny sposób budowy złożonych, chiralnych cyklobutanów, które mogą odegrać kluczowe role w następnej generacji leków i zaawansowanych materiałów molekularnych.
Cytowanie: Zhu, XY., Ji, CL., Dong, TG. et al. Catalytic asymmetric functionalization of bicyclo[1.1.0]butane boronic esters enabled by 1,2-oxygen migration. Nat Commun 17, 1941 (2026). https://doi.org/10.1038/s41467-026-69860-9
Słowa kluczowe: cyklobutan, chemia organoboronowa, kataliza asymetryczna, bicyclobutan, migracja tlenu