Clear Sky Science · pl
Makrofagi związane z guzem CD19+ wywołują immunosupresyjne mikrośrodowisko w raku wątrobowokomórkowym
Dlaczego obrońcy organizmu czasem wspierają raka wątroby
Rak wątroby jest jednym z najgroźniejszych nowotworów na świecie, częściowo dlatego, że guzy potrafią obrócić przeciwko sobie układ odpornościowy gospodarza. To badanie ujawnia zaskakującą podgrupę komórek immunologicznych w obrębie guzów wątroby, które zamiast zwalczać nowotwór, aktywnie pomagają mu się ukrywać i rosnąć. Poznanie tożsamości tych „zdrajców” i mechanizmów ich działania otwiera nowe drogi do zwiększenia skuteczności immunoterapii u osób z rakiem wątrobowokomórkowym, najczęstszą postacią raka wątroby.
Szczególna grupa komórek odpornościowych wewnątrz guzów
Autorzy skupili się na makrofagach związanych z guzem, komórkach odpornościowych, które zwykle pochłaniają drobnoustroje i pozostałości, lecz często ulegają korupcji w obrębie nowotworów. Analiza próbek guzów wątrobowych od wielu pacjentów wykazała wyraźną podgrupę makrofagów z cząsteczką powierzchniową CD19, zazwyczaj spotykaną na limfocytach B, a nie na makrofagach. Makrofagi CD19-dodatnie były znacznie liczniejsze w guzach wątroby niż w sąsiedniej zdrowej tkance wątrobowej czy we krwi i występowały też w większym stopniu w kilku innych nowotworach litych. Analizy pojedynczych komórek potwierdziły, że są to prawdziwe makrofagi o unikalnym profilu genowym i białkowym, a nie błędnie zidentyfikowane limfocyty B.
Jak te komórki kształtują sprzyjające guzkowi środowisko
Pacjenci, których guzy zawierały dużo makrofagów CD19-dodatnich, mieli tendencję do większych, bardziej agresywnych nowotworów i krótszego czasu przeżycia. Próbki bogate w te komórki wykazywały mniej cytotoksycznych limfocytów CD8 i więcej komórek T regulatorowych, co odpowiada wzorcowi silnie immunosupresyjnego mikrośrodowiska. W modelach mysich dodanie makrofagów CD19-dodatnich do komórek raka wątroby przyspieszało wzrost guzów i zmniejszało obecność korzystnych limfocytów T, jednocześnie zwiększając inne supresyjne komórki mieloidalne. Co istotne, gdy badacze użyli zmodyfikowanych komórek T rozpoznających CD19, aby selektywnie eliminować te makrofagi, guzy wątroby zmniejszały się nawet u myszy pozbawionych normalnych limfocytów B, wskazując bezpośrednio na makrofagi jako cel terapeutyczny.
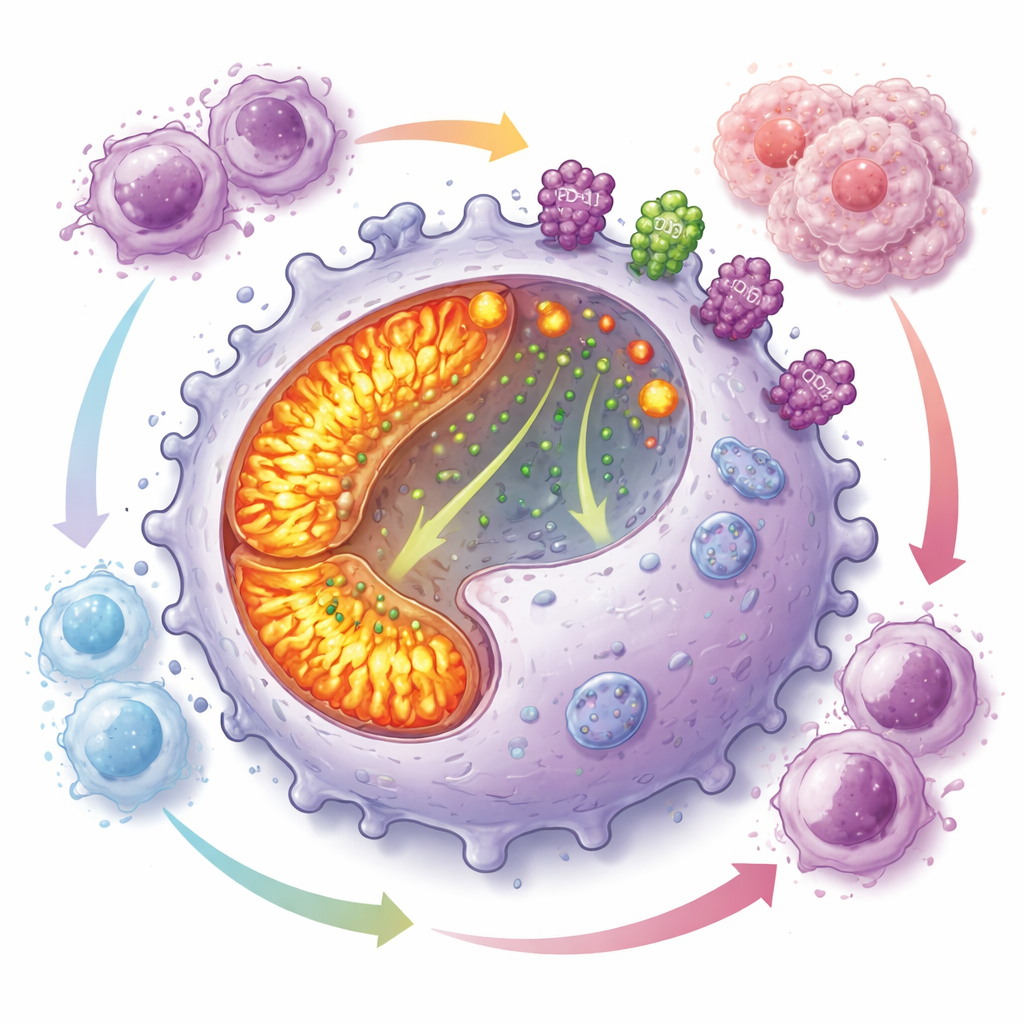
Głodny energii program, który tłumi atak immunologiczny
Dalsze badania wykazały, że makrofagi CD19-dodatnie działają ze zwiększoną aktywnością swoich „elektrowni” wewnątrzkomórkowych. Ich mitochondria były liczniejsze i bardziej aktywne niż w innych makrofagach, z podwyższoną fosforylacją oksydacyjną i produkcją reaktywnych form tlenu. Pomimo tego intensywnego stanu energetycznego, komórki te miały słabą zdolność fagocytozy, lecz szybko się dzieliły, co ułatwiało ich kumulację w guzach. Równocześnie wykazywały wysokie poziomy PD-L1 i CD73 na powierzchni — dwóch cząsteczek znanych z hamowania odpowiedzi limfocytów T i wytwarzania adenozyny, małej cząsteczki silnie tłumiącej odporność. Eksperymenty współhodowli pokazały, że te makrofagi silnie hamują aktywację i proliferację różnych typów limfocytów T.
Główny przełącznik stojący za „zdradzieckimi” makrofagami
Naukowcy zidentyfikowali czynnik transkrypcyjny PAX5 jako centralnego regulatora tego szkodliwego programu makrofagów. PAX5 jest powszechnie znany z kierowania rozwojem komórek B, a tutaj był silnie aktywny w makrofagach CD19-dodatnich. Wymuszenie ekspresji PAX5 w komórkopodobnych makrofagach zwiększało biogenezę mitochondriów, podnosiło produkcję energii i podwyższało poziomy białkowe — lecz nie mRNA — PD-L1, CD73 i CD19. Badania mechanistyczne wykazały, że PAX5 kieruje transportem wapnia do mitochondriów, obniżając poziom wapnia w cytoplazmie i uniemożliwiając kluczowemu regulatorowi TFEB wejście do jądra. Gdy TFEB jest zatrzymany, produkcja i funkcja lizosomów spadają, więc białka takie jak PD-L1 i CD73 nie są efektywnie degradowane i zamiast tego kumulują się na powierzchni komórki, nasilając immunosupresję.
Przekucie odkrycia w lepsze opcje terapeutyczne
Skoro te makrofagi silnie polegają na aktywności CD73 i metabolizmie mitochondrialnym, autorzy sprawdzili, czy blokada tych szlaków może poprawić skuteczność immunoterapii. W mysich modelach raka wątroby połączenie blokady PD-L1 z przeciwciałami przeciw CD73 lub z inhibitorem CD73 prowadziło do mniejszych guzów, większej liczby infiltrujących limfocytów T i mniejszej proliferacji komórek nowotworowych. Podobnie, skojarzenie przeciwciał anty-PD-L1 z inhibitorem fosforylacji oksydacyjnej mitochondriów poprawiło kontrolę guza i zwiększyło napływ komórek odpornościowych do nowotworu. Co znamienne, te korzyści znikały u myszy, których makrofagi nie miały PAX5, potwierdzając, że efekty leków wiązały się z dezaktywacją programu makrofagów CD19-dodatnich napędzanego przez PAX5. Łącznie wyniki sugerują, że selektywne celowanie w tę podgrupę makrofagów — przy pomocy terapii komórkowych skierowanych przeciw CD19, hamowania CD73 lub leków metabolicznych — mogłoby pomóc przekształcić immunologicznie „zimny” guz wątroby w taki, który lepiej odpowiada na istniejące terapie blokujące punkty kontrolne.
Cytowanie: Wang, J., Cao, W., Huang, J. et al. Tumor-associated CD19+ macrophages induce immunosuppressive microenvironment in hepatocellular carcinoma. Nat Commun 17, 3250 (2026). https://doi.org/10.1038/s41467-026-69638-z
Słowa kluczowe: rak wątrobowokomórkowy, makrofagi związane z guzem, immunoterapia, PD-L1 i CD73, metabolizm mitochondrialny