Clear Sky Science · pl
Specyficzna dla nowotworów ekspresja HORMAD1 zaburza zatrzymanie mitotyczne i zwiększa wrażliwość na inhibitory kinaz mitotycznych
Dlaczego to ma znaczenie dla leczenia raka
Podczas podziału komórek polegamy na złożonych mechanizmach bezpieczeństwa, które mają zapewnić przekazanie poprawnego zestawu chromosomów. Nowotwory często przejmują lub osłabiają te zabezpieczenia, prowadząc do chaotycznych genomów, co zarówno napędza chorobę, jak i wpływa na odpowiedź guzów na leki. W badaniu tym opisano, jak nietypowe białko HORMAD1, normalnie aktywne jedynie w komórkach rozrodczych, zostaje włączone w wielu agresywnych rakach piersi i innych guzach. Poprzez subtelne sabotażowanie kluczowego punktu kontrolnego podziału komórki HORMAD1 zwiększa niestabilność komórek nowotworowych — ale równocześnie czyni je wyjątkowo podatnymi na nową klasę eksperymentalnych leków.
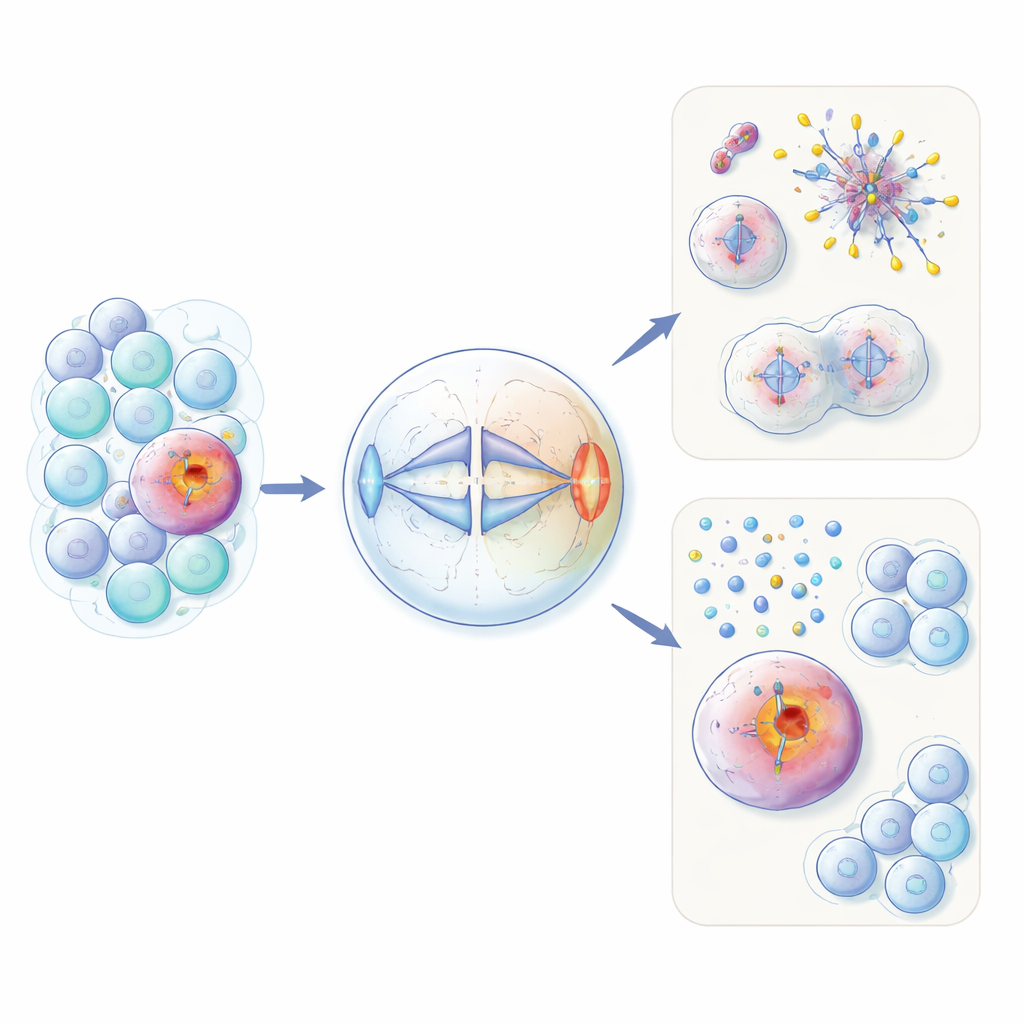
Nie na miejscu białko płodności w komórkach nowotworowych
HORMAD1 zwykle występuje jedynie w komórkach germinalnych, gdzie powstają komórki jajowe i plemniki. Tam uczestniczy w przebudowie DNA i kontroli jakości podczas specjalnego rodzaju podziału zwanego mejozą. Autorzy pokazują, że u około 60% raków piersi potrójnie ujemnych — oraz w podzbiorach kilku innych typów nowotworów — to białko jest niewłaściwie ponownie włączane. Na modelach zarówno inżynierowanych komórek nie-nowotworowych, jak i linii komórkowych raka wykazano, że nadmiar HORMAD1 zaburza równomierny podział chromosomów podczas zwykłej mitozy. Komórki eksprymujące HORMAD1 wykazywały więcej opóźnionych chromosomów, dodatkowych lub brakujących chromosomów (aneuploidia) oraz małych „micronukleusów” zawierających DNA — wszystkie te cechy są znakami genomicznego chaosu obserwowanego w agresywnych nowotworach.
Jak działają mechanizmy bezpieczeństwa podczas podziału komórki
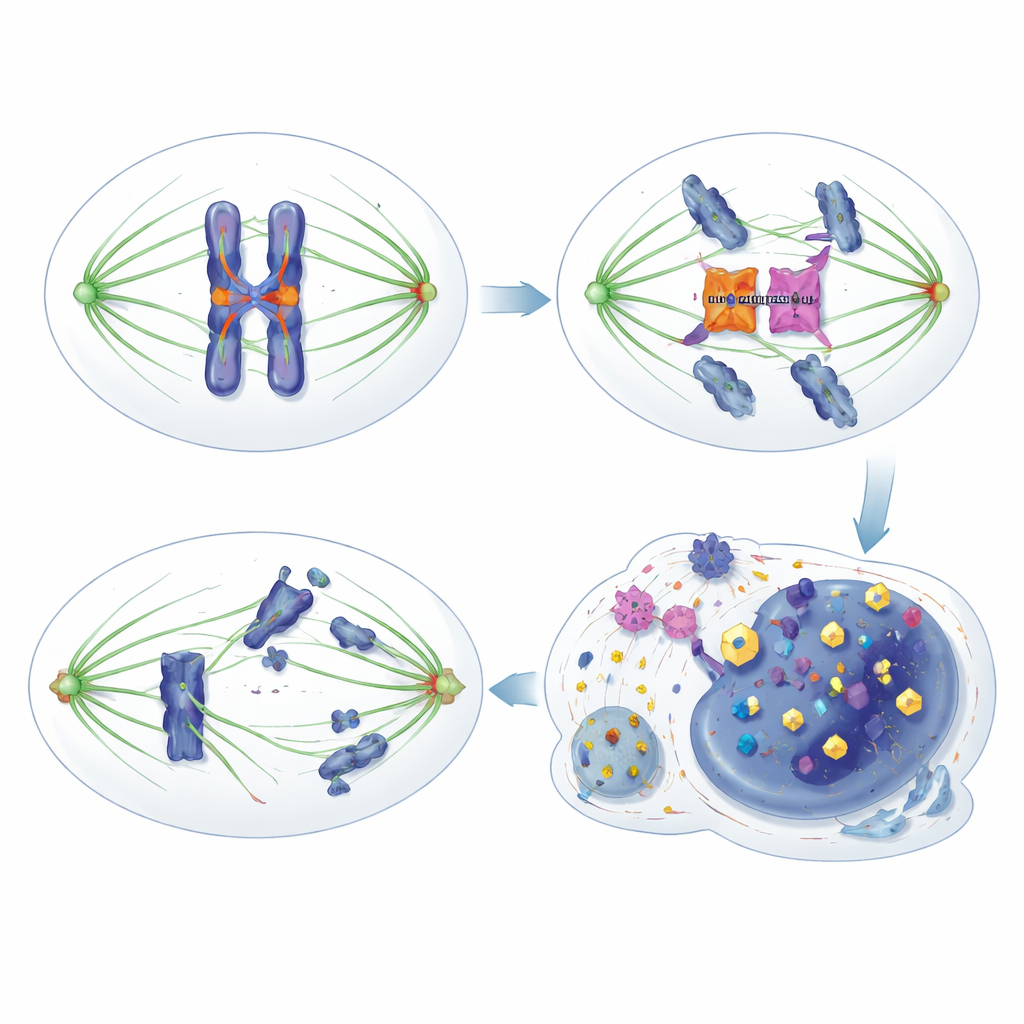
Aby podzielić się poprawnie, komórka buduje wrzeciono z włókien mikrotubularnych, które przyłączają się do każdego chromosomu. System nadzoru zwany punktem kontrolnym tworzenia wrzeciona działa jak hamulec czuły na napięcie: jeśli którykolwiek chromosom nie jest prawidłowo przyłączony, hamulec blokuje postęp, zapobiegając rozdzieleniu dopóki błędy nie zostaną naprawione. Kilka enzymów zwanych kinazami mitotycznymi, w tym MPS1, Aurora B i BUB1, pomaga wykrywać złe przyłączenia i promować „korektę błędów”, aby każda komórka potomna otrzymała właściwy zestaw chromosomów. Zakłócenie tego systemu może zarówno napędzać rozwój raka, jak i tworzyć specyficzne słabości, które można wykorzystać terapiami.
HORMAD1 subtelnie osłabia hamulec
Naukowcy odkryli, że HORMAD1 podkopuje ten mechanizm bezpieczeństwa w sposób subtelny, lecz istotny. Zamiast zakłócać klasyczne komponenty punktu kontrolnego, takie jak białko HORMA MAD2L1, HORMAD1 wiąże się bezpośrednio z kinazą Aurora B. Aurora B zwykle współdziała z innym białkiem, INCENP, by stać się w pełni aktywna i modyfikować białka przy centromerach i kinetochorach — kluczowych miejscach na chromosomach, gdzie przyłączają się włókna wrzeciona. Gdy HORMAD1 jest obecny w dzielących się komórkach nowotworowych, konkuruje z INCENP o dostęp do Aurory B, osłabiając ich współpracę i zmniejszając aktywność Aurory B. W efekcie zwykłe sygnały fosforylacyjne Aurory B na wielu celach są osłabione, korekta błędów jest mniej skuteczna, a punkt kontrolny staje się „przeciekający”: komórki zbyt wcześnie wychodzą z mitozy, nawet gdy przyłączenia są wadliwe, co prowadzi do nieprawidłowego rozdziału chromosomów i niestabilności genomowej.
Od słabości do możliwości terapeutycznej
Ponieważ HORMAD1 tylko częściowo unieszkodliwia Aurorę B i powiązane zabezpieczenia, komórki nowotworowe pozostają na granicy przeżywalności, ale silnie zależą od pozostałej funkcji kinaz mitotycznych, aby przetrwać kolejne wadliwe podziały. Zespół przetestował to, eksponując komórki HORMAD1-dodatnie i HORMAD1-ujemne na eksperymentalne inhibitory MPS1, Aurory B i BUB1. W wielu modelach ekspresja HORMAD1 znacząco zwiększała wrażliwość komórek na te leki, drastycznie zmniejszając ich zdolność do proliferacji lub formowania kolonii. Genetyczne wyłączenie BUB1 było szczególnie śmiertelne tylko w obecności HORMAD1, ujawniając silne, selektywne uzależnienie. W modelach mysich z guzami potrójnie ujemnymi pochodzącymi od pacjentów, nowotwory o wysokim poziomie HORMAD1 kurczyły się lub rosły wolniej po leczeniu nanopartikularną formułą inhibitora Aurory B, podczas gdy guzy pozbawione HORMAD1 w dużej mierze opierały się temu samemu leczeniu.
Co to oznacza dla pacjentów
Dla laika HORMAD1 działa w raku jak miecz obosieczny: popycha komórki guza ku większemu nieporządkowi chromosomalnemu, co może napędzać chorobę, ale jednocześnie sprawia, że komórki te stają się niebezpiecznie zależne od kilku pozostałych mechanizmów ochronnych podziału komórki. Badanie pokazuje, że to niewłaściwie włączone białko płodności osłabia kluczowy punkt kontrolny przez przekierowywanie Aurory B, czyniąc guzy HORMAD1-dodatnie szczególnie podatnymi na leki celujące w Aurorę B, MPS1 lub BUB1. Ponieważ HORMAD1 jest praktycznie nieobecne w normalnych tkankach, a jednocześnie obecne w wyraźnym podzbiorze nowotworów, może służyć jako biomarker do identyfikacji pacjentów, którzy najprawdopodobniej skorzystają z tych rozwijanych inhibitorów kinaz mitotycznych, otwierając potencjalnie nowe, ukierunkowane opcje leczenia dla trudnych do leczenia nowotworów, takich jak rak piersi potrójnie ujemny.
Cytowanie: Walker, C., Kollarovic, G., Weekes, D. et al. Tumour specific HORMAD1 expression perturbs mitotic arrest and drives sensitivity to mitotic kinase inhibitors. Nat Commun 17, 2157 (2026). https://doi.org/10.1038/s41467-026-69561-3
Słowa kluczowe: HORMAD1, rak piersi potrójnie ujemny, niestabilność chromosomalna, kinaza Aurora B, inhibitory punktu kontrolnego mitozy