Clear Sky Science · pl
Heterobifunkcyjne proteomimetyczne polimery do ukierunkowanej degradacji MYC i KRAS
Nowe narzędzia do likwidowania najtrudniejszych białek raka
Wiele z najbardziej niebezpiecznych białek napędzających raka, takich jak MYC i KRAS, przez długi czas określano jako „niedające się ująć lekami”, ponieważ środki farmakologiczne trudno się do nich przyczepiają. Badanie to odsłania nowy rodzaj miękkiego, syntetycznego materiału — nazwanego polimerami HYDRAC — który potrafi chwycić te śliskie białka i skierować je do komórkowego systemu utylizacji. Dla czytelników praca ta ukazuje, jak chemia i nanotechnologia mogą otworzyć możliwości leczenia nowotworów opornych na tradycyjne leki.
Elastyczny szkielet zamiast jednej pigułki
Większość ukierunkowanych leków przeciwnowotworowych to małe cząsteczki, które dopasowują się do kieszonek na powierzchni białka, niczym klucz w zamku. Jednak białka takie jak MYC są wiotkie i nie mają dobrych kieszonek, zaś KRAS często mutuje w sposoby obezwładniające klasyczne leki. Autorzy zaprojektowali zamiast tego długie, łańcuchowe polimery zbudowane z powtarzalnych jednostek. Na tych łańcuchach umieszczają dwa rodzaje elementów: krótkie segmenty wiążące białko, które rozpoznają cel taki jak MYC czy RAS, oraz segmenty „degronowe”, które rekrutują komórkowe mechanizmy utylizacji. Ponieważ wiele kopii każdego elementu zdobi ten sam łańcuch, pojedyncza cząsteczka HYDRAC może jednocześnie sięgać wielu białek i enzymów — coś trudnego do osiągnięcia za pomocą jednej, sztywnej cząsteczki leku.
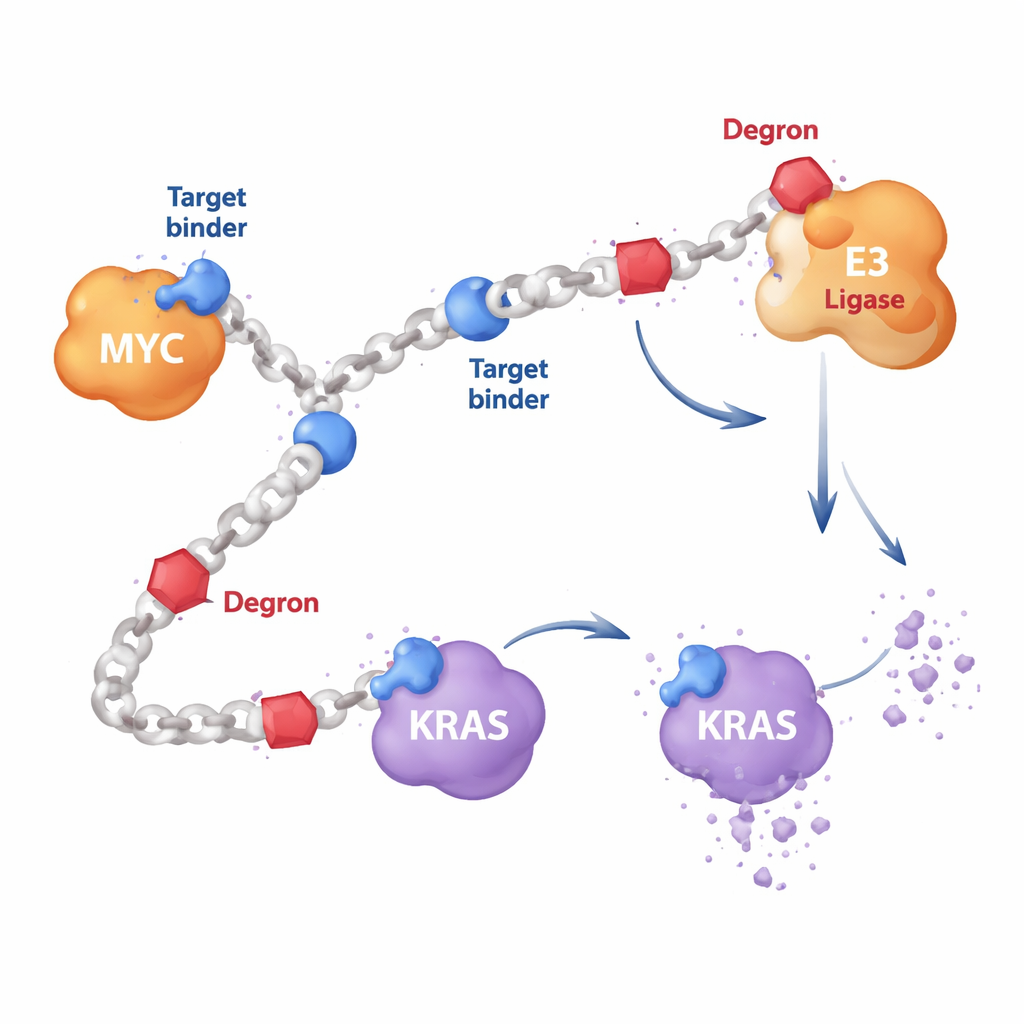
Nauka komórek żucia MYC
W pierwszym teście badacze skupili się na MYC, głównym przełączniku napędzającym wzrost w wielu nowotworach, który od dziesięcioleci opiera się bezpośrednim atakom. Zbudowali polimery HYDRAC eksponujące znany peptyd wiążący MYC obok prostego motywu degronowego, który oznacza białka do zniszczenia przez proteasom komórkowy — główny niszczący białka mechanizm. W eksperymentach in vitro polimery te składały się w zwarte, przypominające białka struktury i silnie wiązały MYC, ale nie powiązane białka. W komórkach nowotworowych HYDRACy łatwo przenikały do wnętrza, zakłócały programy genowe kontrolowane przez MYC i wywoływały śmierć komórek — efekty zależały od obecności zarówno części rozpoznającej, jak i degronowej na tym samym łańcuchu polimerowym.
Od hodowli komórek do kurczenia się guzów
Wewnątrz komórek leczenie HYDRAC spowodowało gwałtowny spadek poziomu białka MYC bez obniżenia RNA MYC, co wskazuje na rzeczywiste zniszczenie, a nie jedynie wyciszenie. Zablokowanie proteasomu lub kluczowych enzymów aktywujących pewne szlaki degradacyjne przywracało poziomy MYC, pokazując, że polimery działają przez przekierowanie własnych systemów utylizacji komórki. Analizy proteomu wykazały, że bardzo niewiele innych białek zostało dotkniętych, co sugeruje wyjątkową selektywność. W modelach mysich z guzami napędzanymi przez MYC, fluorescencyjnie znakowane HYDRACy gromadziły się preferencyjnie w guzach po wstrzyknięciu i pozostawały tam przez dni. Powtarzane podawanie spowalniało wzrost guzów bez istotnej utraty masy ciała czy oczywistych uszkodzeń tkanek, a próbki nowotworów wykazywały mniej dzielących się komórek i więcej oznak zaprogramowanej śmierci komórkowej.
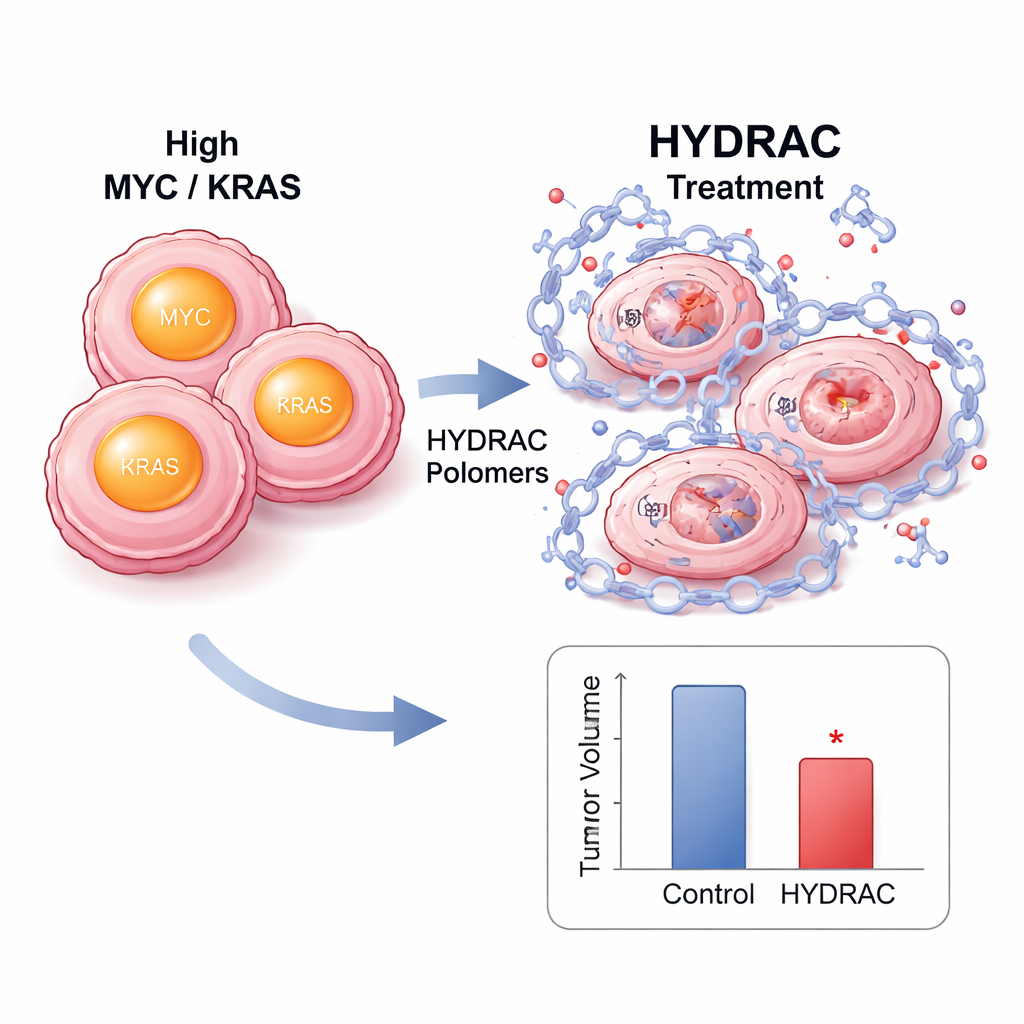
Platforma typu plug-and-play dla wielu celów chorobowych
Jedną ze zalet podejścia HYDRAC jest możliwość wymiany grup bocznych jak części wymienialnych. Zespół zastąpił oryginalny degron innymi elementami rekrutującymi, które przywołują różne enzymy komórkowe, w tym te rozpoznające lek talidomid. Każda wersja degradowa obniżała poziom MYC tylko wtedy, gdy zamierzony enzym był obecny i funkcjonalny, co potwierdza, że polimery można dostroić do korzystania z odrębnych dróg komórkowych. Aby sprawdzić ogólność podejścia, badacze zbudowali następnie HYDRACy celujące w RAS, wykorzystując peptyd rozpoznający białka RAS. Konstrukty te skutecznie degradowały zmutowany KRAS w dwóch różnych liniach komórkowych raka, sugerując potencjał „pan-KRAS”, niezależny od konkretnej mutacji — ważny krok dla nowotworów, w których współistnieje wiele wariantów KRAS.
Dlaczego to ma znaczenie dla przyszłej opieki onkologicznej
Praca ta wprowadza HYDRACy jako nową klasę programowalnych materiałów, które nie tylko blokują kłopotliwe białka — pomagają komórkom je wymazać. Dzięki połączeniu licznych jednostek celujących i degradacyjnych na elastycznym polimerze HYDRACy omijają ograniczenia projektowe tradycyjnych leków małocząsteczkowych i PROTACów, które zazwyczaj mogą nieść tylko po jednej z każdej funkcji. Chociaż przed wprowadzeniem tych materiałów do kliniki pozostaje dużo pracy, wyniki w modelach napędzanych przez MYC i KRAS sugerują, że białka raka długo uważane za „niedające się ująć lekami” mogą w rzeczywistości być wrażliwe, gdy medycyna wygląda bardziej jak dopasowany molekularny pędzel niż jedna mała pigułka.
Cytowanie: Wang, M.M., Truica, M.I., Gattis, B.S. et al. Heterobifunctional proteomimetic polymers for targeted degradation of MYC and KRAS. Nat Commun 17, 1706 (2026). https://doi.org/10.1038/s41467-026-68913-3
Słowa kluczowe: ukierunkowana degradacja białek, MYC, KRAS, terapeutyki polimerowe, nanomedycyna przeciwnowotworowa