Clear Sky Science · pl
Integracyjny epigenomiczny krajobraz mózgów chorych na chorobę Alzheimera ujawnia molekularne zaburzenia oligodendrocytów związane z tau
Dlaczego te badania mózgu są ważne
Choroba Alzheimera jest najbardziej znana z utraty pamięci i odkładania się w mózgu dwóch problematycznych białek: amyloidu i tau. Jednak osoby z Alzheimerem mogą mieć bardzo różne wzorce uszkodzeń, nawet przy tej samej diagnozie. W tym badaniu postawiono istotne pytanie: jakie przełączniki wewnątrz komórek mózgowych wpływają na to, ile tych szkodliwych białek się gromadzi i jak oddziałują na różne typy komórek? Analizując chemiczne znaczniki na DNA w setkach mózgów, badacze odkryli zaskakujące powiązanie między tau a komórkami odpowiedzialnymi za przewodzenie w mózgu.
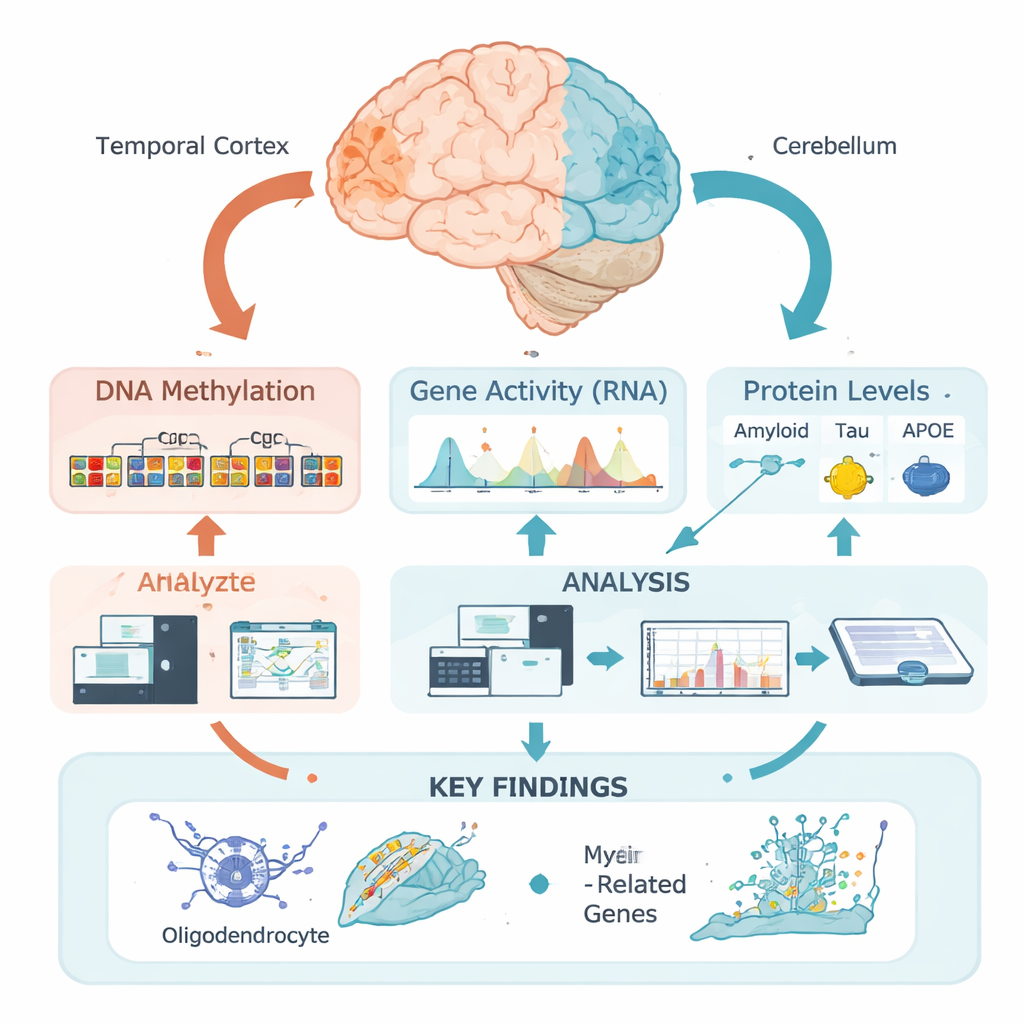
Chemiczne znaczniki na DNA jako ukryte przełączniki
Nasze DNA zawiera podstawowe instrukcje do budowy i funkcjonowania komórek mózgowych, ale te instrukcje są regulowane przez znaki epigenetyczne — chemiczne oznaczenia, które mogą włączać lub wyłączać pobliskie geny bez zmiany kodu genetycznego. Jednym z najważniejszych znaczników jest metylacja DNA, w której małe grupy chemiczne przyłączają się do określonych miejsc w DNA. Zamiast badać pojedyncze miejsca osobno, zespół zastosował nowe, „regionalne” podejście: pogrupowali wiele pobliskich miejsc w funkcjonalne strefy na podstawie tego, jak DNA jest upakowane w korze skroniowej — obszarze silnie dotkniętym w chorobie Alzheimera — oraz w móżdżku, który jest stosunkowo oszczędzony. Pozwoliło to zapytać, gdzie w sensie biologicznym wzorce metylacji zmieniają się w związku z cechami choroby.
Łączenie znaków DNA z białkami Alzheimera
Badacze przeanalizowali tkankę mózgową od 472 osób, u których choroba Alzheimera została potwierdzona pośmiertnie. Dla każdej próbki kory skroniowej zmierzyli szczegółowe poziomy amyloidu, tau i białek APOE w różnych formach biochemicznych, a także klasyczne mikroskopowe oceny blaszek amyloidowych i splątków tau. Następnie przeprowadzili badania asocjacji obejmujące cały epigenom, sprawdzając, czy regionalne poziomy metylacji DNA korelują z tymi pomiarami. Uderzające jest to, że niemal wszystkie silne skojarzenia dotyczyły nie amyloidu, lecz tau — szczególnie tau rozpuszczalnego całkowitego i związanej z błoną formy ufosforylowanej (chemicznie zmodyfikowanej), uważanej za szczególnie toksyczną.
Silny sygnał w komórkach odpowiedzialnych za przewodzenie
Wiele regionów DNA związanych z tau znajdowało się w „aktywnych” częściach genomu, które wpływają na pobliskie geny. Łącząc dane o metylacji z pomiarami aktywności genów z tych samych mózgów, zespół wykazał, że te regiony często kontrolowały geny wykorzystywane przez oligodendrocyty — komórki owijające włókna nerwowe mieliną, co pozwala sygnałom elektrycznym podróżować szybko i niezawodnie. Kluczowe geny związane z mieliną, takie jak MBP, MAG i MYRF, wraz z genem ryzyka Alzheimera BIN1 i nowszym kandydatem o nazwie LDB3, pojawiały się w tym zestawie. Wyższe poziomy toksycznego, ufosforylowanego tau zwykle współwystępowały z wyższą metylacją w tych regionach i niższą ekspresją powiązanych genów oligodendrocytów i mieliny, podczas gdy bardziej łagodna pula rozpuszczalnego tau całkowitego wykazywała przeciwny wzorzec.
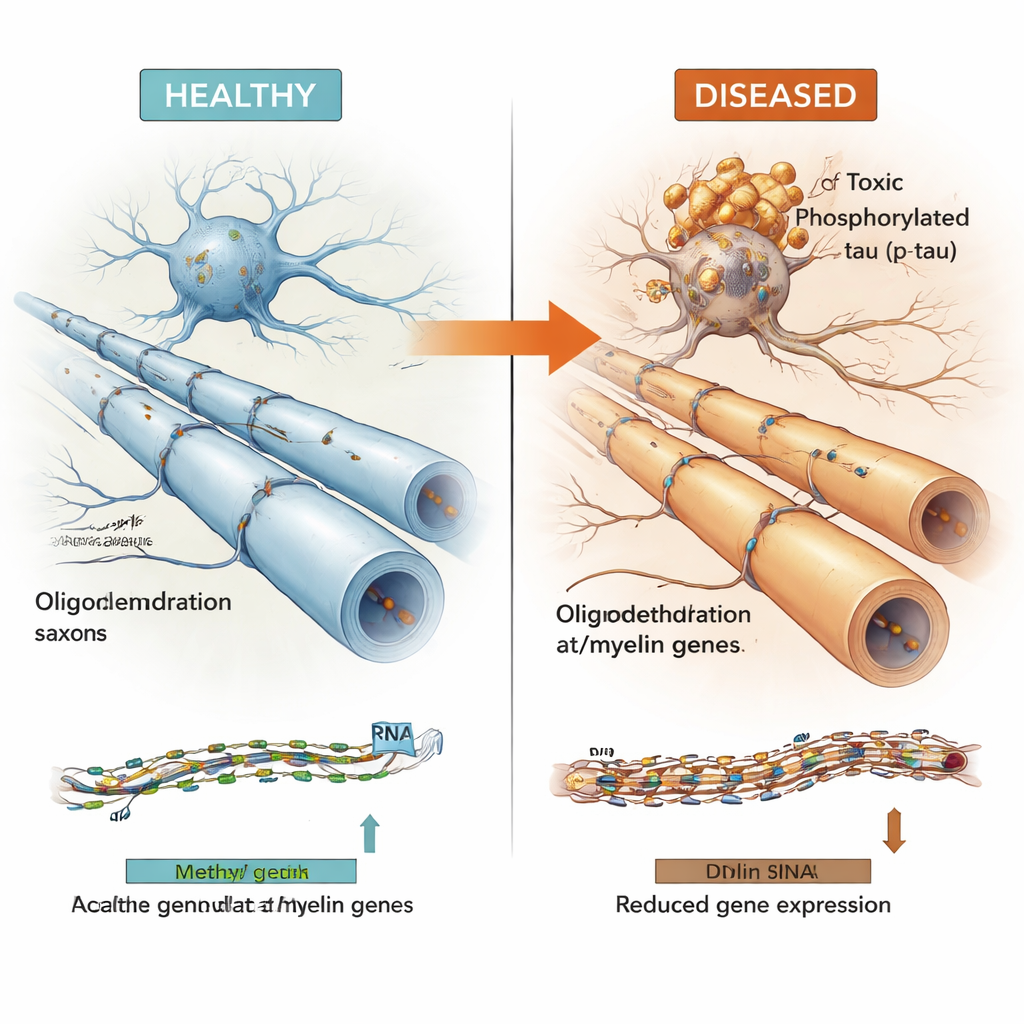
Wzorzec obserwowany w różnych chorobach mózgu
Aby sprawdzić, czy te odkrycia są solidne i uniwersalne, autorzy zbadali duże, niezależne zbiory danych z innych kolekcji mózgów chorych na Alzheimera oraz z mózgów dotkniętych pierwotnymi „tauopatiami”, takimi jak postępujące porażenie nadjądrowe i choroba Picka. Mimo że kohorty te były mierzone różnymi technologiami i często w innych obszarach mózgu, wiele tych samych regionów DNA i genów oligodendrocytów wykazywało spójne zachowanie: poziomy ich metylacji wiązały się z obciążeniem splątkami tau, a ich ekspresja była zmniejszona w mózgach chorych oraz w badaniach jednokomórkowych skupionych specyficznie na oligodendrocytach. Co ważne, wzorce te nie wydawały się być wyjaśnione jedynie genetyką lub ogólną utratą komórek, co sugeruje rzeczywistą epigenetyczną zmianę w funkcjonowaniu oligodendrocytów.
Co to oznacza dla zrozumienia Alzheimera
Podsumowując, wyniki wspierają model, w którym narastające poziomy szkodliwego tau są ściśle powiązane ze zmianami epigenetycznymi w oligodendrocytach, które tłumią geny związane z mieliną, potencjalnie osłabiając przewodzenie w mózgu i przyczyniając się do spadku funkcji poznawczych. Wciąż nie jest jasne, co następuje pierwsze — nagromadzenie tau czy zaburzenie tych genów mielinowych — ale silne, powtarzalne skojarzenia na tysiącach próbek i w kilku chorobach wskazują na wspólny mechanizm. Mapując te przełączniki DNA i integrując je w publicznym „Atlazie Multiomicznym”, praca ta podkreśla oligodendrocyty i ich regulację epigenetyczną jako obiecujące cele przyszłych terapii ukierunkowanych na stabilizację obwodów mózgowych, zamiast skupiania się wyłącznie na neuronach czy blaszkach amyloidowych.
Cytowanie: Oatman, S.R., Reddy, J.S., Atashgaran, A. et al. Integrative epigenomic landscape of Alzheimer’s Disease brains reveals oligodendrocyte molecular perturbations associated with tau. Nat Commun 17, 2116 (2026). https://doi.org/10.1038/s41467-026-68864-9
Słowa kluczowe: choroba Alzheimera, białko tau, metylacja DNA, oligodendrocyty, mielina