Clear Sky Science · pl
Podstawy strukturalne ludzkiego kanału aktywowanego cynkiem (ZAC) — przekazywanie sygnału i modulacja
Jak pierwiastek śladowy pomaga komórkom nerwowym się porozumiewać
Cynk jest najbardziej znany jako składnik odżywczy w tabletkach multiwitaminowych, ale w organizmie ten metal pełni także funkcję szybkiego chemicznego przekaźnika w mózgu. Opisane tu badanie odsłania, w rozdzielczości atomowej, jak mało znane białko zwane kanałem aktywowanym cynkiem (ZAC) wykrywa cynk poza komórkami i zamienia ten sygnał na odpowiedź elektryczną. Zrozumienie tej specyficznej bramy w błonie komórkowej może wyjaśnić, w jaki sposób cynk kształtuje aktywność mózgu i zasugerować nowe sposoby precyzyjnego modulowania sygnałów nerwowych w zdrowiu i chorobie.
Specjalna brama dla sygnałów cynkowych
Wiele szybkich komunikatów między komórkami nerwowymi jest przenoszonych przez dobrze znane związki, takie jak serotonina czy acetylocholina, które otwierają pierścieniowe kanały w błonie komórkowej. ZAC jest odległym krewnym tych receptorów, ale zamiast reagować na cząsteczkę organiczną, ulega aktywacji przez jony metali, takie jak cynk, miedź czy protony. ZAC występuje w wielu ludzkich tkankach, w tym w mózgu, lecz brak go u standardowych zwierząt laboratoryjnych, jak myszy i szczury, co spowolniło postęp badań. W pracy wykorzystano wysokorozdzielczą krio‑elektronową mikroskopię, aby uzyskać kilka trójwymiarowych „migawek” ludzkiego ZAC: w stanie spoczynkowym, z przyłączonym cynkiem oraz z dwoma różnymi lekami, które zamykają kanał. Razem te struktury ujawniają, jak cynk przyczepia się do wierzchu kanału, jak jony przez niego przepływają oraz jak blokery zaciskają bramę lub klinują ją w nieprzewodzącym stanie.
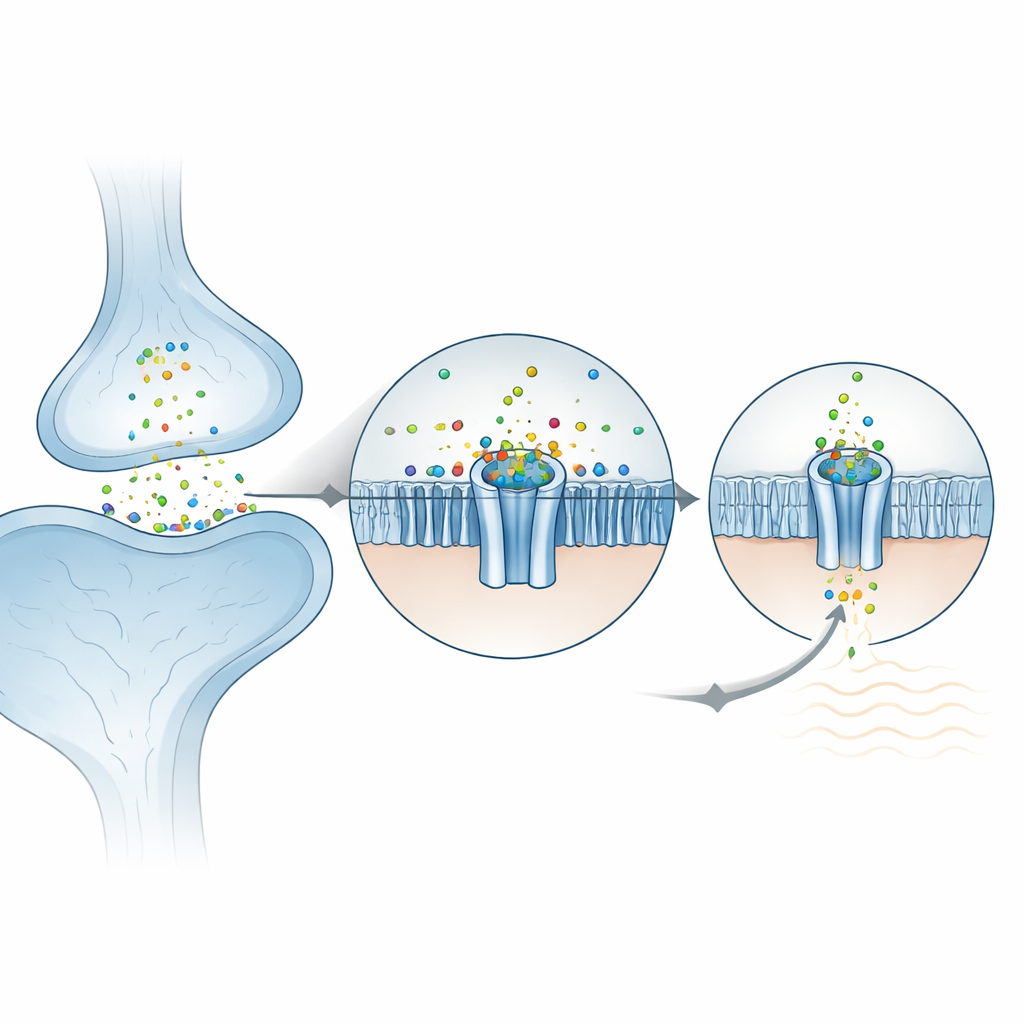
Jak cynk zatrzaskuje się w kanale
Na zewnętrznej powierzchni komórki ZAC zbudowany jest z pięciu identycznych podjednostek tworzących rozetę. Badacze odkryli, że jony cynku osiadają w pięciu równoważnych kieszeniach, zlokalizowanych każda pomiędzy dwiema sąsiednimi podjednostkami w zewnętrznej domenie. Co zaskakujące, cynk nie jest utrzymywany przez zwykłe „chwytające” aminokwasy, które często wiążą metale (takie jak histydyna czy cysteina). Zamiast tego jest on głównie okalany przez dwa pierścieniowe, aromatyczne łańcuchy boczne, które stabilizują naładowany dodatnio jon poprzez tzw. oddziaływania kation–π. Gdy kluczowe reszty zostały zmienione w komórkach jajowych żaby używanych do pomiarów elektrycznych, kanał przestał reagować na cynk, co potwierdziło ich zasadniczą rolę. Otoczenie jest już wstępnie ułożone, co pomaga wyjaśnić, dlaczego ZAC wykazuje znaczącą spontaniczną aktywność nawet bez cynku: białko znajduje się blisko progu przełączenia między zamknięciem a otwarciem, a cynk jedynie przesuwa równowagę.
Ścieżka jonów i powszechny wariant genetyczny
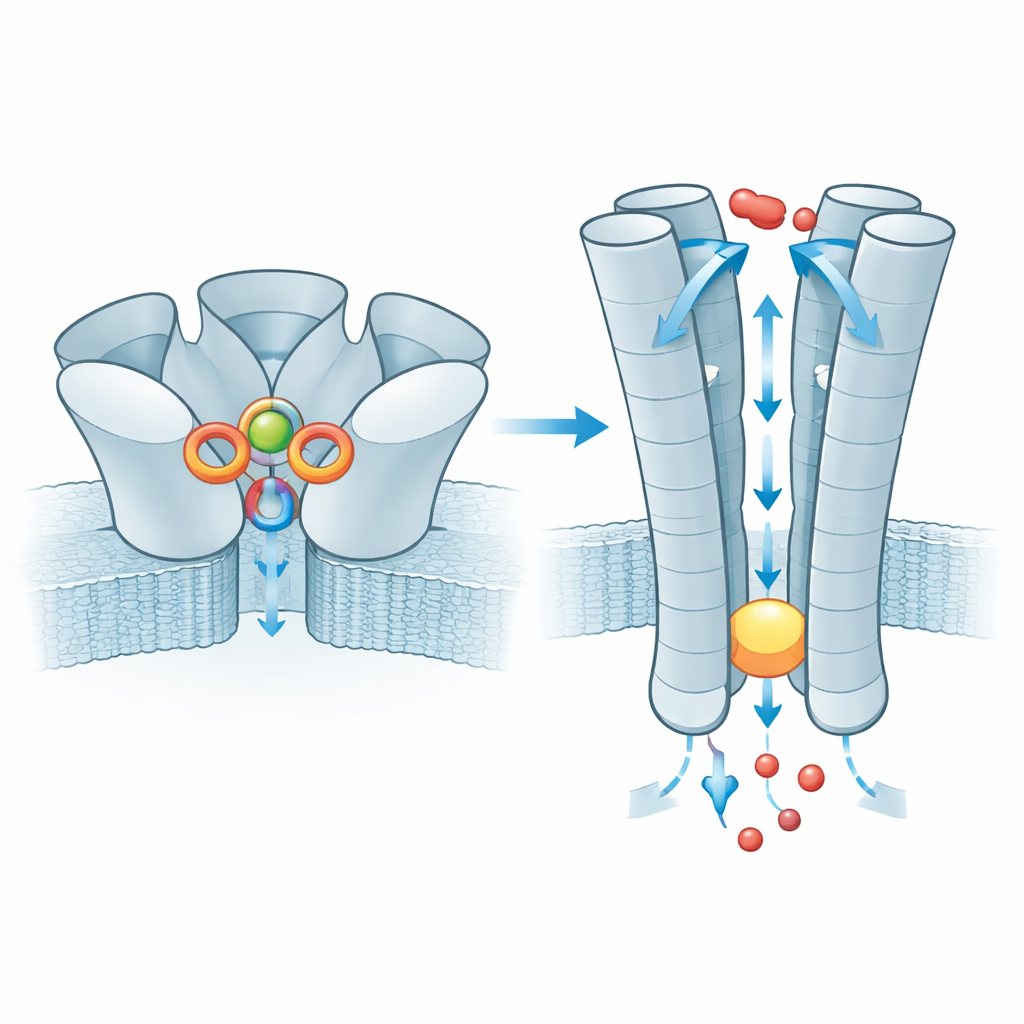
Gdy cynk się przyłączy, efekt jest przekazywany dalej do części ZAC przechodzącej przez błonę, gdzie pięć wewnętrznych helis tworzy por. W stanie spoczynkowym ten tunel zwęża się przy pierścieniu reszt leucyny, tworząc hydrofobowy korek, który blokuje ruch jonów. Po związaniu cynku korek rozszerza się na tyle, że pozwala małym kationom, takim jak sód i potas, przecisnąć się, podczas gdy naładowane wnętrze poru pomaga selekcjonować te jony. Zespół przebadał także bardzo powszechny wariant ludzkiego ZAC, w którym pojedynczy aminokwas (treonina) jest zastąpiony alaniną w krótkim odcinku nad korkiem. Ta drobna zmiana osłabia sieć oddziaływań między sąsiednimi podjednostkami, która normalnie przekazuje przyłączenie cynku do bramy, a pomiary elektryczne pokazują, że kanały zbudowane z tego wariantu przewodzą znacznie mniejsze prądy. Wariant ten działa więc jako mniej efektywny przetwornik sygnału, chociaż jego wpływ na fizjologię człowieka pozostaje nieznany.
Jak dwa leki wyciszają kanał
Poza cynkiem, badanie bada również, jak dwa antyagoniści, TTFB i d‑tubokuraryna (d‑TC), wyłączają ZAC. TTFB to zaprojektowana mała cząsteczka, która okazuje się osadzać głęboko w obszarze błonowym, wsuwając się między dwie helisy tworzące por tuż nad bramą. Tam oddziałuje z dopasowaną hydrofobową kieszenią i pobliskimi resztami polarnymi, skutecznie usztywniając helisy, aby nie mogły przejść do w pełni otwartego stanu przewodzącego. d‑TC, starszy lek niegdyś stosowany jako środek zwiotczający mięśnie, działa szerzej. Jedna cząsteczka d‑TC wiąże się w tej samej zewnętrznej kieszeni, która normalnie gości cynk, naśladując dodatni ładunek cynku, ale blokując prawidłowe przyłączenie rzeczywistego cynku. Druga cząsteczka d‑TC siedzi we wlocie poru, fizycznie zatykając tunel. W połączeniu te wiązania uwięziły ZAC w zdesensytyzowanej, nieprzewodzącej konformacji, podczas gdy kształt białka pozostaje relatywnie otwarty.
Co wyniki oznaczają dla cynku i zdrowia
Ta strukturalna praca ukazuje w jasnych, molekularnych szczegółach, że ZAC jest prawdziwym sensorem cynku, wykorzystującym niezwykłą aromatyczną „miseczkę” do wykrywania metalu w tym samym typie miejsca, gdzie inne członki rodziny wiążą neuroprzekaźniki. Identyfikuje też konkretne sieci oddziaływań, które regulują łatwość otwierania i zamykania kanału, oraz mapuje dwa odrębne miejsca wiązania leków, które mogą albo dosuwać bramę do zamknięcia, albo zacementować por. Dla osób niezwiązanych z dziedziną kluczowy przekaz jest taki, że cynk to nie tylko statyczny składnik odżywczy, lecz aktywny sygnał, a ZAC jest jednym z jego dedykowanych odbiorników. W miarę jak naukowcy poszukują ról ZAC w ludzkim organizmie i w zaburzeniach neurologicznych związanych z zaburzeniem równowagi cynku, te plany na poziomie atomowym stanowią mapę drogową do projektowania precyzyjniejszych cząsteczek modulujących ten kanał i potencjalnie korygujących zaburzoną sygnalizację cynkową.
Cytowanie: Zhou, Z., Long, Y., Chao, Y. et al. Structural basis of human zinc-activated channel (ZAC) signaling and modulation. Cell Discov 12, 23 (2026). https://doi.org/10.1038/s41421-026-00878-5
Słowa kluczowe: sygnalizacja cynkowa, kanały jonowe bramkowane ligandem, neuronauka, struktura cryo-EM, modulacja kanału