Clear Sky Science · pl
Palmitylacja ASCT2 regulowana przez oś JNK1–ZDHHC14 koordynuje metabolizm glutaminy i progresję NSCLC
Napędzanie pożaru raka płuca
Wiele szybko rosnących nowotworów płuca jest „uzależnionych” od glutaminy — powszechnego aminokwasu pełniącego rolę ważnego paliwa i materiału budulcowego. W badaniu tym odkryto, jak komórki nowotworowe precyzyjnie regulują główne „wrota” dla glutaminy na swojej powierzchni i jak zakłócenie tego systemu może spowolnić wzrost guza. Zrozumienie tego ukrytego zaworu paliwowego pomaga wyjaśnić, dlaczego niektóre guzy tak trudno „zagłodzić”, i wskazuje na nowe kombinacje leków, które skuteczniej odcinają ich dopływ energii.
Komórkowe wrota dla glutaminy
Glutamina wnika do komórek głównie przez białkowy transporter ASCT2, zlokalizowany w błonie zewnętrznej i przenoszący glutaminę do wnętrza. Niedrobnokomórkowy rak płuca (NSCLC), najczęstsza postać raka płuca, często silnie polega na glutaminie, aby wspierać szybkie podziały i przetrwanie. Wysokie poziomy ASCT2 w guzach wiążą się z agresywnym przebiegiem choroby i gorszym rokowaniem. Jednak ASCT2 jest nieustannie syntetyzowany, modyfikowany i degradowany, co rodzi pytanie: co decyduje o tym, ile tego strażnika pozostaje na powierzchni komórki w danym momencie?
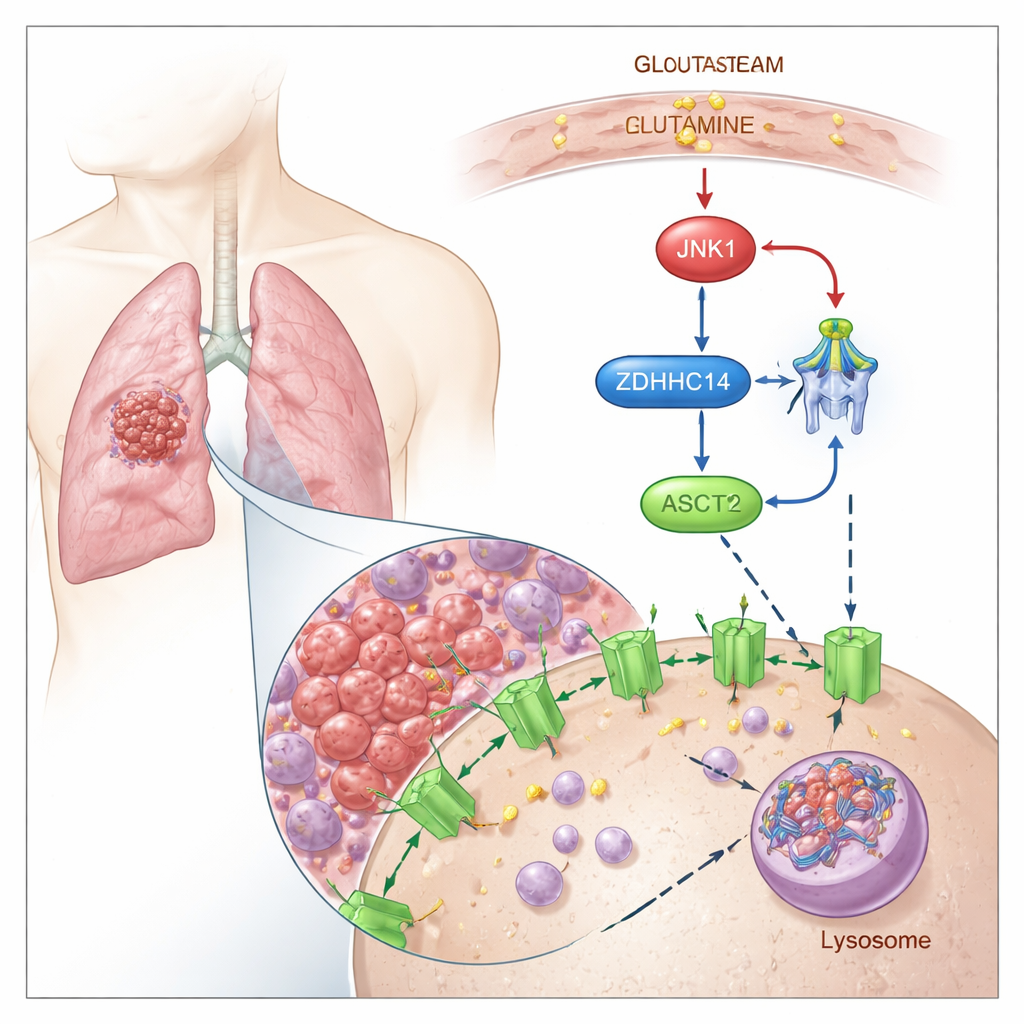
Oznaczanie ASCT2 do rozkładu
Naukowcy wykazali, że ASCT2 jest kontrolowany przez chemiczny „znacznik” zwany palmitoylacją, w którym do określonych reszt cysteiny w białku przyłączany jest kwas tłuszczowy. Stwierdzili, że enzym ZDHHC14 dodaje tę lipidową grupę w dwóch zachowanych miejscach ASCT2 (Cys39 i Cys48). Po oznakowaniu ASCT2 jest przekierowywany z powierzchni komórki do komórkowych centrów recyklingu zwanych lizosomami, gdzie ulega rozkładowi. Blokowanie palmitoylacji uniemożliwia oznaczanie i degradację ASCT2, prowadząc do zwiększenia poziomu białka ASCT2 i wzrostu wychwytu glutaminy, przy braku zmian aktywności genu.
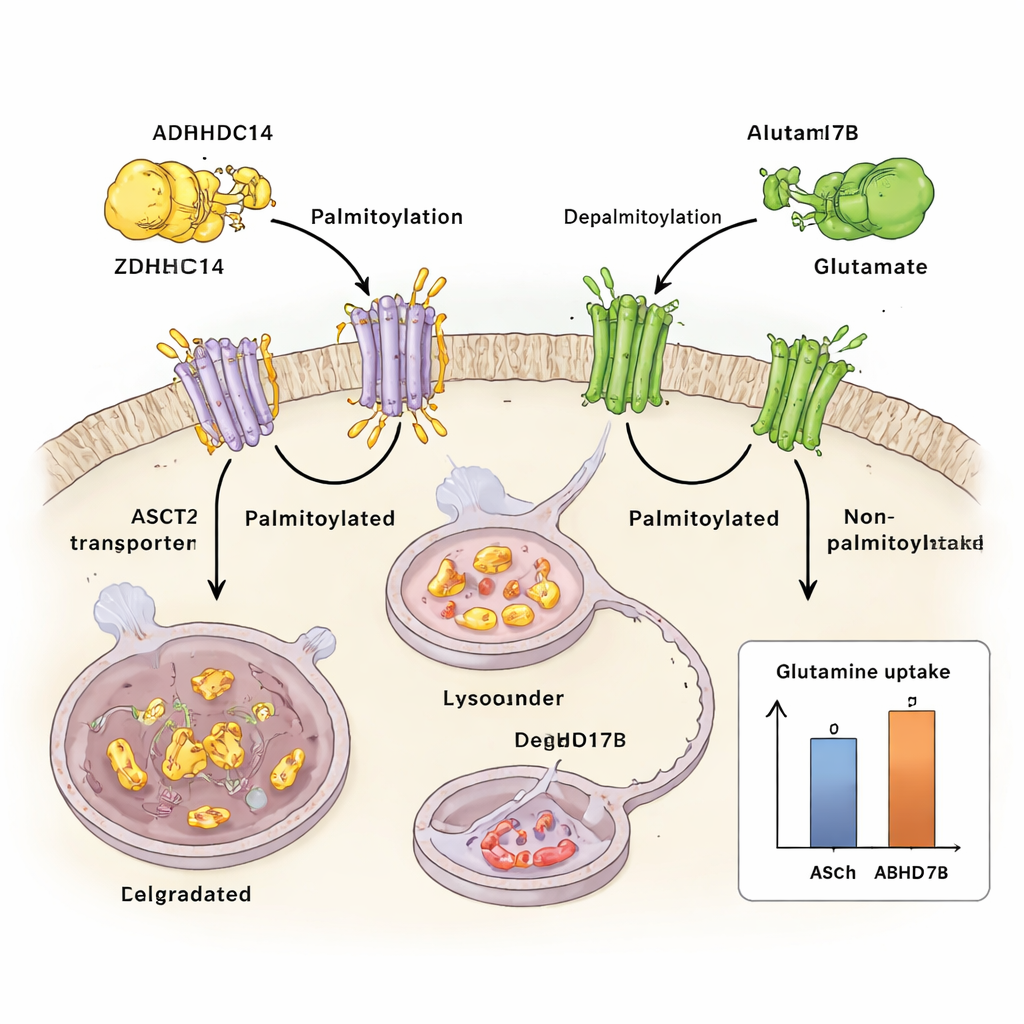
Enzym przeciwstawny, który chroni wrota
Przeciwstawnie do ZDHHC14 działa inny enzym, ABHD17B, który usuwa lipidowy znacznik z ASCT2. Gdy ABHD17B jest aktywny, ASCT2 jest mniej palmitoylowany, bardziej stabilny i częściej jest regenerowany na powierzchnię komórki zamiast trafiać do lizosomu. To wzajemne znakowanie i odznaczanie działa jak precyzyjny regulator przepływu glutaminy: ZDHHC14 kieruje ASCT2 ku degradacji, podczas gdy ABHD17B ratuje go i podtrzymuje transport glutaminy. W komórkach raka płuca przesunięcie tej równowagi w stronę mniejszej palmitoylacji zwiększa wychwyt glutaminy i sprzyja wzrostowi guza w hodowlach i u myszy.
Jak stres odżywczy przeprogramowuje system
Zespół zbadał następnie, co się dzieje, gdy komórki nowotworowe doświadczają niedoboru glutaminy. Podczas pozbawienia glutaminy włącza się białko sygnalizacyjne wrażliwe na stres, JNK1. JNK1 fizycznie wiąże się z ZDHHC14 i dodaje grupę fosforanową w konkretnym miejscu (Thr440), znakując ZDHHC14 do własnej lizosomalnej degradacji. W miarę jak poziomy ZDHHC14 spadają, ASCT2 otrzymuje mniej palmitylowych znaków, unika rozkładu i gromadzi się na powierzchni komórki — dokładnie wtedy, gdy komórka najbardziej potrzebuje wyłapywać ograniczoną glutaminę. Zmiana tego pojedynczego miejsca wrażliwego na JNK1 stabilizuje ZDHHC14, przywraca znakowanie ASCT2 i zmniejsza wychwyt glutaminy, podkreślając, jak ściśle stres odżywczy jest wbudowany w tę pętlę kontrolną.
Przekładanie mechanizmu na terapię
Ponieważ ASCT2 ma kluczowe znaczenie dla metabolizmu nowotworu, badane są leki, które go blokują, takie jak eksperymentalny związek V9302. Badanie to ujawnia, że sygnalizacja JNK1 może przeciwdziałać degradacji ASCT2, skutecznie chroniąc „wrota” glutaminy. W modelach komórkowych i mysich NSCLC połączenie inhibitora JNK z V9302 silniej zmniejszało wychwyt glutaminy, wzrost komórek nowotworowych i rozmiar guza niż którykolwiek z leków stosowanych osobno. Próbki pacjentów i publiczne zestawy danych dodatkowo pokazują, że niskie poziomy ZDHHC14 i wysokie poziomy ASCT2 są powszechne w NSCLC i wiążą się z gorszym przeżyciem, sugerując, że ten wzorzec molekularny mógłby pomóc zidentyfikować pacjentów najbardziej podatnych na terapię ukierunkowaną na tę ścieżkę.
Co to oznacza dla pacjentów
Mówiąc prostym językiem, praca ta pokazuje, że niektóre raki płuca kontrolują swoje ulubione paliwo poprzez regulację molekularnego zaworu na powierzchni komórki. Trio białek — JNK1, ZDHHC14 i ABHD17B — decyduje, czy bramka glutaminy ASCT2 zostanie oznaczona do zniszczenia, czy pozostawiona otwarta. Gdy glutamina jest rzadka, system przesuwa się, by zachować ASCT2 i utrzymać dopływ paliwa, pomagając guzom przetrwać w trudnych warunkach. Wspólne blokowanie ASCT2 i szlaku JNK, który go chroni, umożliwiło skuteczniejsze „zagłodzenie” komórek nowotworowych w modelach laboratoryjnych i zwierzęcych. Chociaż potrzebne są dalsze badania, oś fosforylacja–palmitoylacja stanowi obiecujący nowy punkt uchwytu dla terapii mających odciąć żywieniowe linie życia guzów glutationożernych (glutamine-hungry) w raku płuca.
Cytowanie: Chen, X., Ke, Z., Wei, S. et al. ASCT2 palmitoylation regulated by JNK1-ZDHHC14 axis orchestrates glutamine metabolism and NSCLC progression. Cell Discov 12, 13 (2026). https://doi.org/10.1038/s41421-026-00870-z
Słowa kluczowe: metabolizm glutaminy, niedrobnokomórkowy rak płuca, transporter ASCT2, palmitoylacja białek, sygnalizacja JNK