Clear Sky Science · pl
Mechanizmy molekularne i potencjalne implikacje terapeutyczne dialogu między metylacją DNA a przeprogramowaniem metabolizmu w raku tarczycy
Dlaczego te badania mają znaczenie poza laboratorium
Rak tarczycy jest jednym z najszybciej rosnących nowotworów na świecie. Choć wiele przypadków da się leczyć, najbardziej agresywne postacie często przestają odpowiadać na terapię jodem radioaktywnym, będącą jednym z podstawowych zabiegów, co pozostawia pacjentów z niewieloma dobrymi opcjami. Artykuł przeglądowy wyjaśnia, jak dwie niewidoczne siły w komórkach — chemiczne znaczniki na DNA oraz zmiany w sposobie, w jaki komórki nowotworowe pozyskują i wykorzystują paliwo — współdziałają, napędzając wzrost raka tarczycy i oporność na leczenie. Zrozumienie tej ukrytej współpracy może otworzyć drogę do bardziej precyzyjnych i trwałych terapii.
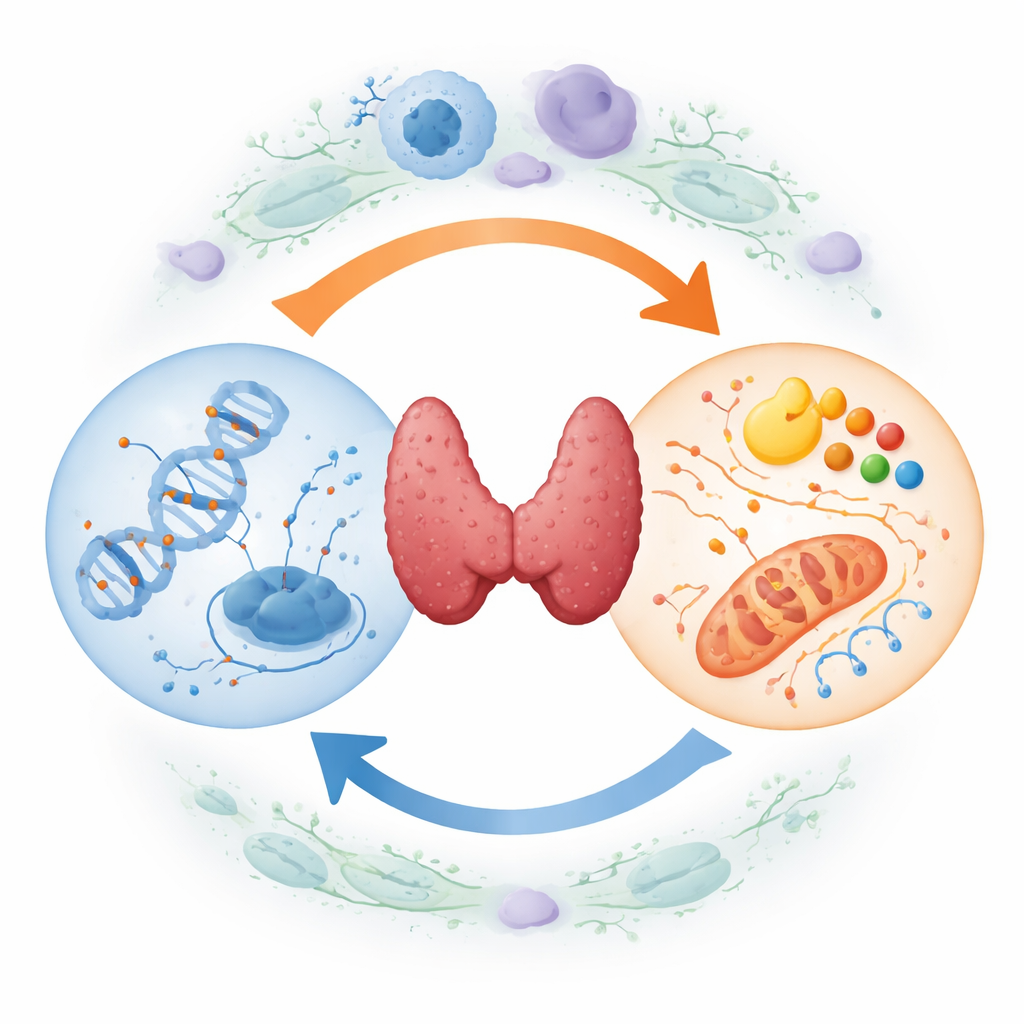
Jak komórki nowotworowe przepisują swoją instrukcję
Każda komórka nosi to samo DNA, ale chemiczne znaczniki zwane grupami metylowymi potrafią włączać lub wyłączać geny bez zmiany samego kodu genetycznego. W raku tarczycy ten „markup” DNA jest głęboko zaburzony. Duże fragmenty genomu tracą znaczniki metylowe, co może destabilizować chromosomy, podczas gdy kluczowe hamulce wzrostu i funkcji tarczycy stają się nadmiernie oznakowane i uciszone. Należą do nich geny supresorowe oraz geny specyficzne dla tarczycy, które normalnie pomagają komórkom pobierać jod. Efektem jest podręcznik genetyczny, w którym wiele rozdziałów dotyczących bezpieczeństwa jest zaciemnionych, sprzyjając niekontrolowanemu wzrostowi i utracie normalnej tożsamości tarczycowej.
Jak komórki nowotworowe przebudowują swoje linie paliwowe
Równocześnie komórki guza tarczycy przeprojektowują sposób zdobywania i wykorzystania energii. Zamiast głównie efektywnie spalać paliwo w mitochondriach, silnie opierają się na szybkim, lecz nieefektywnym rozkładzie cukrów, generując kwaśne produkty uboczne, które pomagają im unikać układu odpornościowego. Zwiększają także syntezę i utlenianie tłuszczów oraz przekierowują aminokwasy, takie jak seryna i glutamina, by wspierać szybkie dzielenie się. Te zmiany nie są przypadkowe: kierują nimi sygnały napędzające nowotwór i tworzą elastyczną sieć metaboliczną, która pozwala komórkom guza przetrwać niski poziom tlenu, opierać się lekom i rozrastać w nowych miejscach.
Dwukierunkowy ruch między znacznikami DNA a metabolizmem komórkowym
Głównym przesłaniem artykułu jest to, że znakowanie DNA i wykorzystanie paliwa nie są odrębnymi wątkami — tworzą samonapędzającą się pętlę. Z jednej strony zmieniony metabolizm komórek nowotworowych produkuje specyficzne małe cząsteczki, które działają jak przełączniki dla enzymów dodających lub usuwających grupy metylowe z DNA. Gdy poziomy tych metabolitów się zmieniają, mogą przesunąć genom w kierunku większej lub mniejszej metylacji w wrażliwych miejscach. Z drugiej strony metylacja DNA może bezpośrednio uciszać lub wzmacniać geny kontrolujące użycie cukrów, obrót tłuszczów i transport aminokwasów. Z czasem ten dwukierunkowy ruch utrwala stan sprzyjający nowotworowi, w którym nieprawidłowe oznaczenia DNA i zniekształcony metabolizm wzajemnie się wzmacniają.
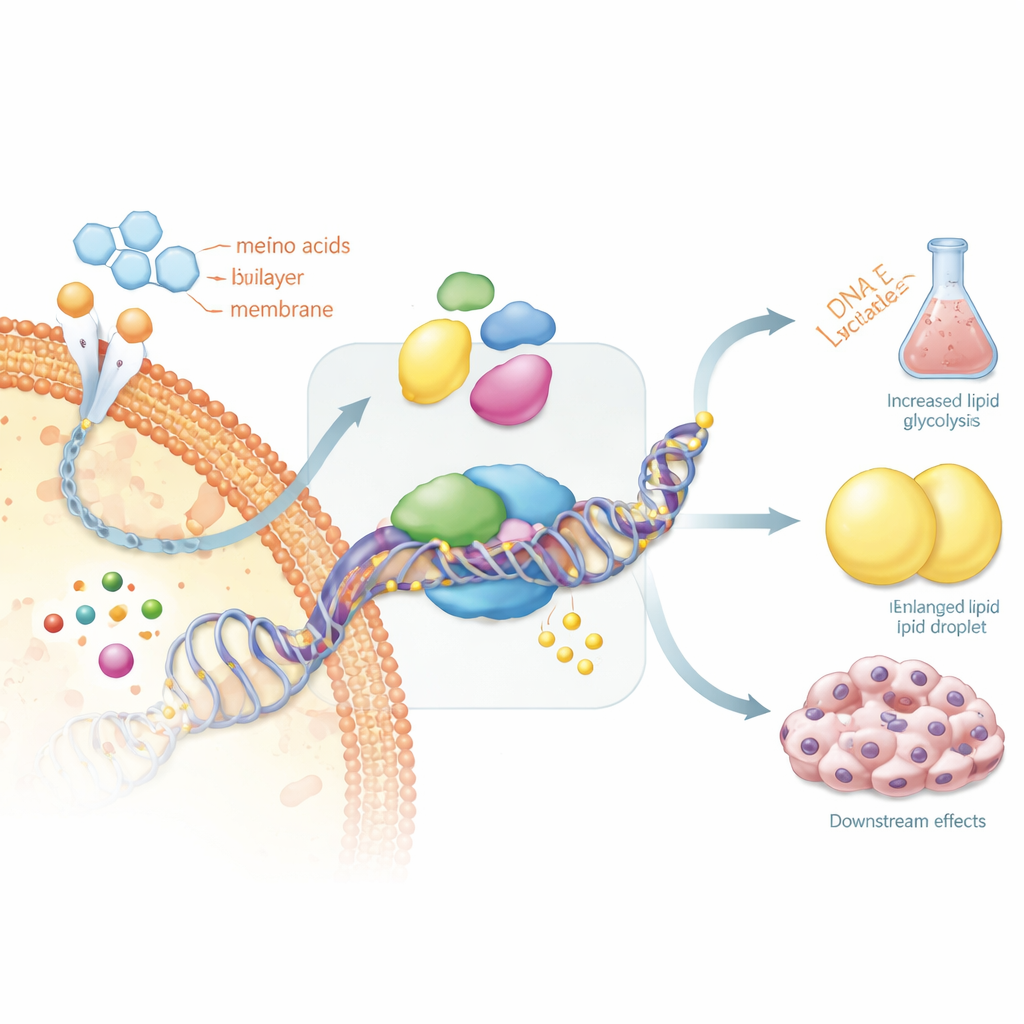
Dlaczego niektóre raki tarczycy przestają wchłaniać jod
Ta pętla sprzężenia zwrotnego ma bardzo praktyczne konsekwencje dla pacjentów. Terapia jodem radioaktywnym działa tylko wtedy, gdy komórki nowotworowe zachowują molekularny mechanizm umożliwiający pobieranie jodu. Przegląd podkreśla, że kluczowe geny tarczycowe odpowiedzialne za to, w tym receptor dla hormonu stymulującego tarczycę (TSH) oraz transporter sodowo-jodkowy, są często wyłączane przez silne metylowanie ich regionów kontrolnych. Gdy to następuje, komórki nowotworowe „zapominają”, że są komórkami tarczycy i przestają wchłaniać jod, co sprawia, że standardowa terapia zawodzi. Autorzy sugerują, że ostrożne odwrócenie tych oznaczeń DNA lub blokowanie szlaków metabolicznych, które je podtrzymują, mogłoby przywrócić pobieranie jodu i reaktywność na leczenie.
Nowe pomysły terapeutyczne oparte na zintegrowanym spojrzeniu
Postrzeganie raka tarczycy jako choroby osi „metylacja DNA–metabolizm” prowadzi do nowych strategii terapeutycznych. Zamiast polegać na pojedynczych lekach, autorzy opowiadają się za podejściami kombinowanymi, które jednocześnie uderzają w kilka elementów pętli — leki epigenetyczne luzujące szkodliwe oznaczenia DNA, leki metaboliczne blokujące kluczowe szlaki paliwowe oraz leki hamujące sygnały napędzające nowotwór. Dodanie nowoczesnych immunoterapii i zaawansowanych systemów podawania leków, takich jak inteligentne nanocząstki, mogłoby dodatkowo przechylić równowagę przez przekształcenie mikrośrodowiska immunologicznego guza przy jednoczesnym ograniczeniu działań niepożądanych. Wczesne dane z laboratoriów i badań klinicznych sugerują, że takie skoordynowane ataki mogą spowolnić chorobę, przywrócić wchłanianie jodu u niektórych pacjentów i opóźnić rozwój oporności.
Co to oznacza dla przyszłej opieki
Dla czytelnika niebędącego specjalistą wniosek jest taki, że agresywne nowotwory tarczycy mogą stać się uleczalne nie przez znalezienie pojedynczego cudownego leku, lecz przez zrozumienie i przerwanie błędnego koła między oznaczeniami DNA a metabolizmem komórkowym. Mapując tę oś szczegółowo i śledząc zmiany we krwi oraz próbkach guza, lekarze mogą kiedyś dopasowywać pacjentów do spersonalizowanych kombinacji terapii epigenetycznych, metabolicznych, celowanych i immunologicznych. Jeśli to się uda, takie zintegrowane podejście mogłoby zamienić dzisiejsze najbardziej oporne raki tarczycy w choroby ponownie poddające się leczeniu — a być może zapobiec ich przekształceniu się w tak agresywne postacie od samego początku.
Cytowanie: Zhang, T., Han, H., Zhang, Y. et al. The molecular mechanisms and potential therapeutic implications of the crosstalk between DNA methylation and metabolic reprogramming in thyroid cancer. Cell Death Discov. 12, 110 (2026). https://doi.org/10.1038/s41420-026-02981-8
Słowa kluczowe: rak tarczycy, metylacja DNA, metabolizm nowotworu, oporność na jod radioaktywny, terapia celowana