Clear Sky Science · pl
Oś AdipoR1–AMPK hamuje raka piersi we wszystkich podtypach molekularnych poprzez wielomodalne szlaki śmierci komórkowej, w tym ferroptozę i apoptozę
Dlaczego komórki tłuszczowe mają znaczenie w raku piersi
Większość z nas myśli o tkance tłuszczowej jako o biernym magazynie energii, ale komórki tłuszczowe są aktywnymi „fabrykami”, które uwalniają hormony i cząsteczki sygnałowe do krwi. W tym badaniu analizowano, jak jeden z tych sygnałów pochodzących z tkanki tłuszczowej, działający przez cząsteczkę AdipoR1 na komórkach raka piersi, może spowolnić wzrost guza. Praca jest istotna, ponieważ sugeruje nowy sposób leczenia wielu postaci raka piersi przez wykorzystanie komunikacji między tkanką tłuszczową a nowotworem, co może wzmocnić działanie istniejących leków.
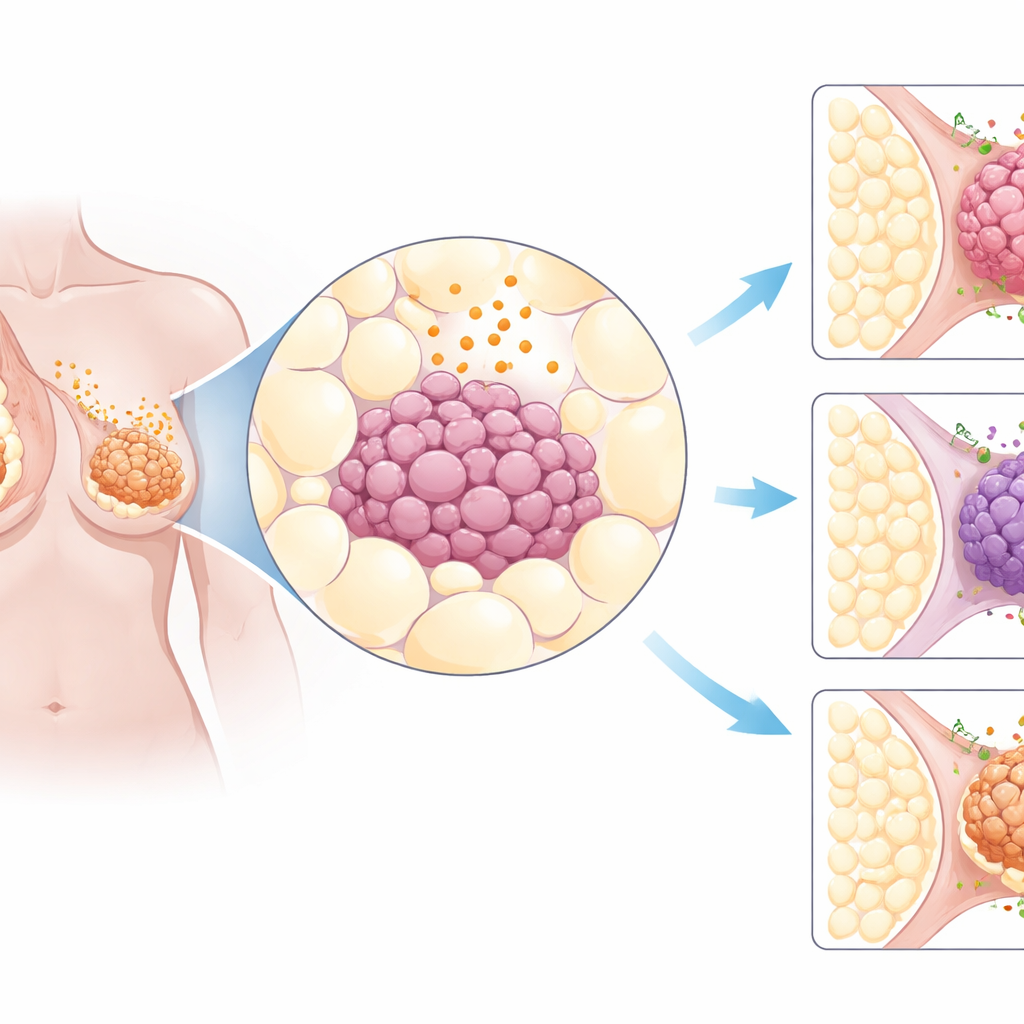
Przegląd wielu nowotworów
Naukowcy zaczęli od przeszukania dużych publicznych baz danych nowotworowych zawierających informacje genetyczne tysięcy guzów pacjentów. Skupili się na około trzech tuzinach genów zaangażowanych w sygnały pochodzące z tkanki tłuszczowej oraz struktur komórkowych odbierających te sygnały. Porównując guzy z 31 różnych narządów z tkanką zdrową, wyłonił się jeden wzorzec: nowotwory piersi wykazywały szczególnie silne zmiany związane z tymi signalami tłuszczowymi. W szczególności receptor AdipoR1 był często obecny na poziomach wyższych niż normalnie w guzach piersi, niezależnie od tego, czy były napędzane hormonami, HER2‑pozytywne, czy bardziej agresywne typu potrójnie negatywnego. Próbki tkankowe z ponad 600 raków piersi potwierdziły szeroką obecność białka AdipoR1 w komórkach nowotworowych.
Testowanie leku sygnalizującego z tłuszczu na komórkach nowotworowych
Aby sprawdzić, co AdipoR1 robi wewnątrz guzów, zespół użył hodowanych w laboratorium linii komórkowych raka piersi reprezentujących kilka powszechnych podtypów. Leczyli te komórki AdipoRonem, małą cząsteczką aktywującą AdipoR1. AdipoRon szybko uruchomił znany przełącznik wykrywający poziom energii w komórkach zwany AMPK, co pokazało, że sygnał dociera do wnętrza komórki. W miarę zwiększania dawki AdipoRonu komórki nowotworowe dzieliły się wolniej, poruszały się mniej w testach gojenia rany, a wiele z nich ulegało zaprogramowanej autodestrukcji. Gdy naukowcy celowo obniżyli poziom AdipoR1 w komórkach, AdipoRon stracił dużą część swojej skuteczności, natomiast zwiększenie poziomu AdipoR1 uczyniło lek bardziej efektywnym, ściśle wiążąc efekt z tym receptorem.
Wielokrotne sposoby skłaniania komórek nowotworowych do śmierci
Analizując aktywność genów po leczeniu, naukowcy stwierdzili, że AdipoRon uruchamia reakcje stresowe wewnątrz komórek raka piersi. Aktywował geny powiązane z klasyczną zaprogramowaną śmiercią komórkową oraz te zaangażowane w niedawno rozpoznany rodzaj żelazozależnej destrukcji komórek zwany ferroptozą. Kluczowe markery tego procesu wzrastały zarówno na poziomie RNA, jak i białka, szczególnie w hormonozależnych komórkach raka piersi, a chemiczne wskaźniki uszkodzenia lipidów komórkowych potwierdzały to odkrycie. Jednocześnie AdipoRon obniżał poziomy białek, które normalnie pomagają komórkom nowotworowym przetrwać, w tym pomocników naprawy DNA (BRCA1 i BRCA2), receptora estrogenowego napędzającego wzrost w wielu guzach oraz TROP2, cząsteczki powierzchniowej powiązanej z agresywnym zachowaniem.
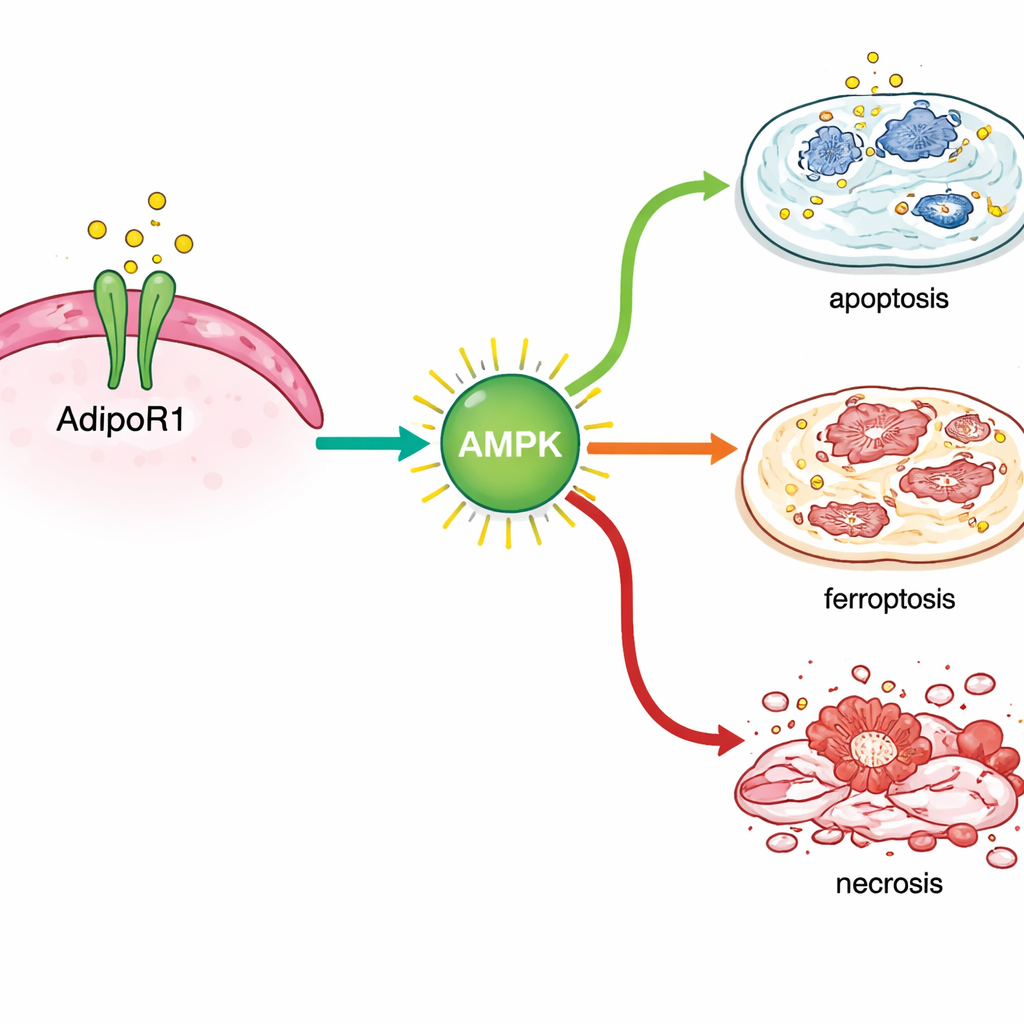
Współpraca z obecnymi terapiami, a nie przeciwko nim
Zespół zapytał następnie, czy aktywacja AdipoR1 może uzupełniać standardowe leki. W hormonozależnych komórkach raka piersi AdipoRon w połączeniu z tamoksyfenem wywołał większe zahamowanie wzrostu niż którykolwiek z leków stosowany osobno. W liniach potrójnie negatywnych AdipoRon wzmocnił efekty powszechnie stosowanych chemioterapeutyków, takich jak paklitaksel i doksorubicyna. Przechodząc do modeli mysich z hormonozależnymi guzami piersi, badacze podawali AdipoRon doustnie. Guzy u leczonych zwierząt rosły wolniej i zawierały większe obszary martwicy w badaniu mikroskopowym. Co ważne, myszy nie wykazywały oczywistych skutków ubocznych w zachowaniu, masie ciała ani zdrowiu wątroby w czasie leczenia.
Co to może znaczyć dla pacjentów
Podsumowując, wyniki sugerują, że uruchomienie AdipoR1 w komórkach raka piersi angażuje kilka nakładających się dróg prowadzących do śmierci komórkowej przy jednoczesnym osłabieniu kluczowych systemów przetrwania i że podejście to działa w różnych genetycznych formach choroby. Zamiast zastępować obecne terapie, leki celujące w AdipoR1, takie jak AdipoRon, mogłyby działać jako dodatki, które czynią guzy bardziej podatnymi na terapię hormonalną, chemioterapię lub przyszłe leki celowane. Zanim ta strategia trafi do kliniki, będzie trzeba opracować silniejsze i bardziej selektywne aktywatory AdipoR1, określić, w których guzach pacjentów receptor jest najsilniej eksprymowany, oraz dokładnie ocenić bezpieczeństwo. Mimo to praca wskazuje intrygujący pomysł: sygnały z naszej własnej tkanki tłuszczowej można by przekierować, aby pomagały w walce z rakiem piersi zamiast go napędzać.
Cytowanie: Sato, S., Yamanaka, T., Komori, Y. et al. AdipoR1–AMPK axis suppresses breast cancer across molecular subtypes via multimodal cell death pathways, including ferroptosis and apoptosis. Cell Death Dis 17, 384 (2026). https://doi.org/10.1038/s41419-026-08583-7
Słowa kluczowe: rak piersi, adipokiny, AdipoR1, szlaki śmierci komórkowej, metabolizm nowotworów