Clear Sky Science · pl
Rola tratw lipidowych w onkogennym sygnalizowaniu przez FGFR2c z udziałem kanału TRPA1 w komórkach gruczolakoraka przewodów trzustkowych
Dlaczego małe wyspy w błonach komórkowych mają znaczenie
Rak trzustki jest jednym z najgroźniejszych nowotworów, częściowo dlatego, że jego komórki wyjątkowo sprawnie odrywają się od pierwotnego guza i wnikają w sąsiednie tkanki. W tym badaniu przyglądamy się mikroskopijnym „wyspom” w zewnętrznej warstwie komórek nowotworowych, zbudowanym z cholesterolu i tłuszczów, i stawiamy proste pytanie o daleko idących konsekwencjach: czy te wyspy pomagają włączyć sygnał wzrostowy, który zwiększa agresywność raka trzustki, i czy ich naruszenie może spowolnić ten proces?
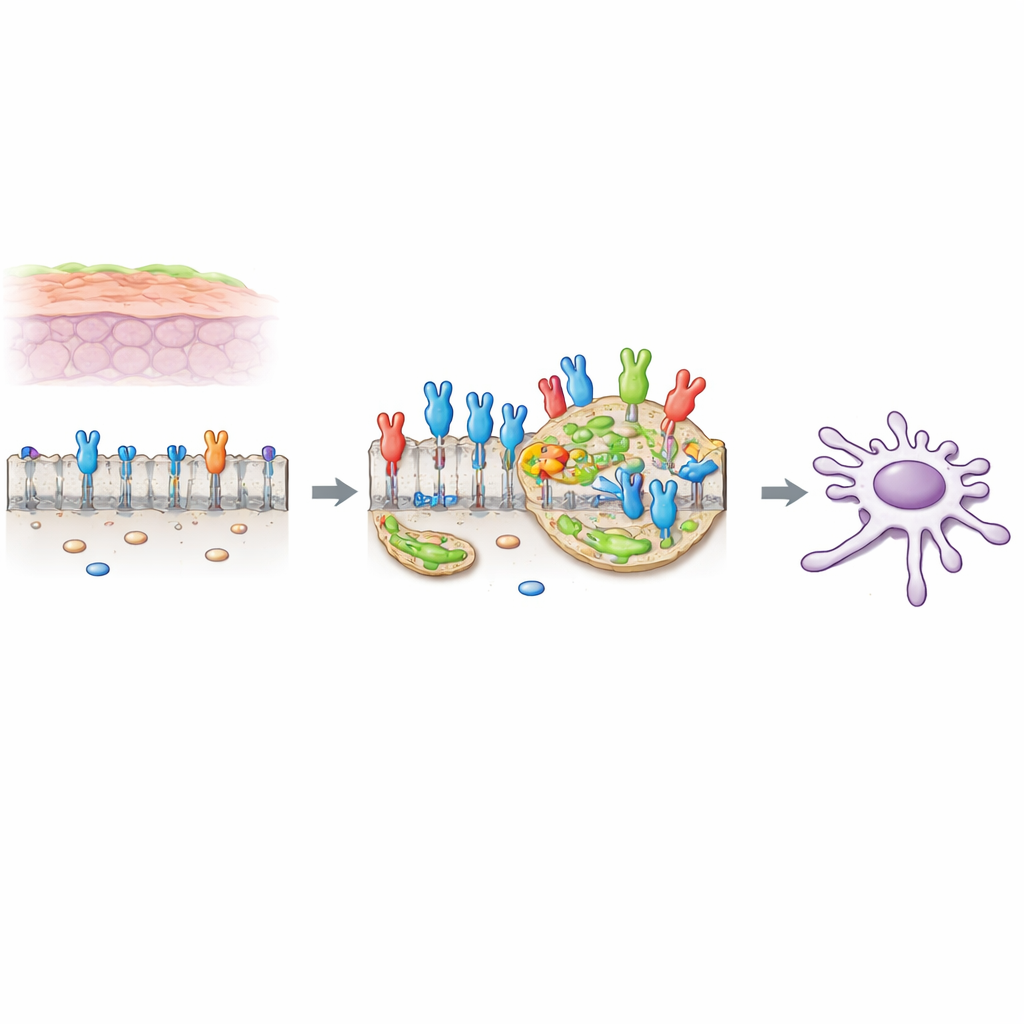
Przełącznik sprzyjający nowotworowi na powierzchni komórki
Wiele komórek ma na powierzchni przełączniki reagujące na sygnały wzrostu. Jednym z nich jest FGFR2c — wariant zwykle występujący w komórkach bardziej elastycznych i ruchomych, który jednak staje się nadmiernie obecny w komórkach gruczolakoraka przewodów trzustkowych (PDAC). Gdy ten przełącznik zostaje uruchomiony przez swój zewnętrzny ligand, wywołuje zmiany znane jako przejście epitelialno-mezenchymalne (EMT), które czynią komórki mniej przylegające i bardziej zdolne do ruchu i inwazji. Wcześniejsze badania autorów wykazały, że w komórkach PDAC FGFR2c aktywuje kaskadę wewnętrznych przekaźników z udziałem białka PKCε i kilku klasycznych szlaków wzrostowych, zwiększając przeżywalność, ruchliwość i inwazyjność komórek.
Wyspy bogate w cholesterol jako wzmacniacze sygnału
Zewnętrzna błona komórkowa nie jest jednorodna. Zawiera małe, bogate w cholesterol fragmenty zwane tratwami lipidowymi, które działają jak miniaturowe platformy, gdzie cząsteczki sygnałowe mogą się grupować i komunikować efektywniej. Badacze stwierdzili, że po aktywacji FGFR2c przez zewnętrzny sygnał większa część receptorów przemieszcza się do tych tratw lipidowych. Przy użyciu znaczników fluorescencyjnych i frakcjonowania biochemicznego pokazali, że aktywowany FGFR2c koncentruje się w tych obszarach, podczas gdy jego rozmieszczenie poza tratwami zmienia się z gładkiego na kropkowany, co odpowiada klasteryzacji receptorów na tych wyspach.
Rozbicie wysp osłabia cechy nowotworowe
Aby sprawdzić, czy te lipidowe wyspy są niezbędne dla onkogennych efektów FGFR2c, zespół zastosował związek (metyl-β-cyklodekstrynę), który selektywnie usuwa cholesterol z błony i destabilizuje tratwy lipidowe bez zabijania komórek. W komórkach PDAC bogatych w FGFR2c zakłócenie tratw silnie zmniejszyło aktywację kluczowych białek przekaźnikowych znajdujących się poniżej receptora oraz stłumiło program EMT: geny i białka związane ze stanem ruchliwym i inwazyjnym uległy obniżeniu, podczas gdy cechy epitelialne zostały częściowo przywrócone. To samo leczenie obniżyło też poziomy białek związanych z inwazją, takich jak MCL-1, SRC i enzymy degradujące macierz, oraz zmniejszyło zdolność komórek nowotworowych do przemieszczania się i penetrowania żelu imitującego otaczającą tkankę. Komórki z bardzo małą ilością FGFR2c niemal nie reagowały, co podkreśla, jak kluczowe jest to partnerstwo receptor–tratwa w tych guzach.
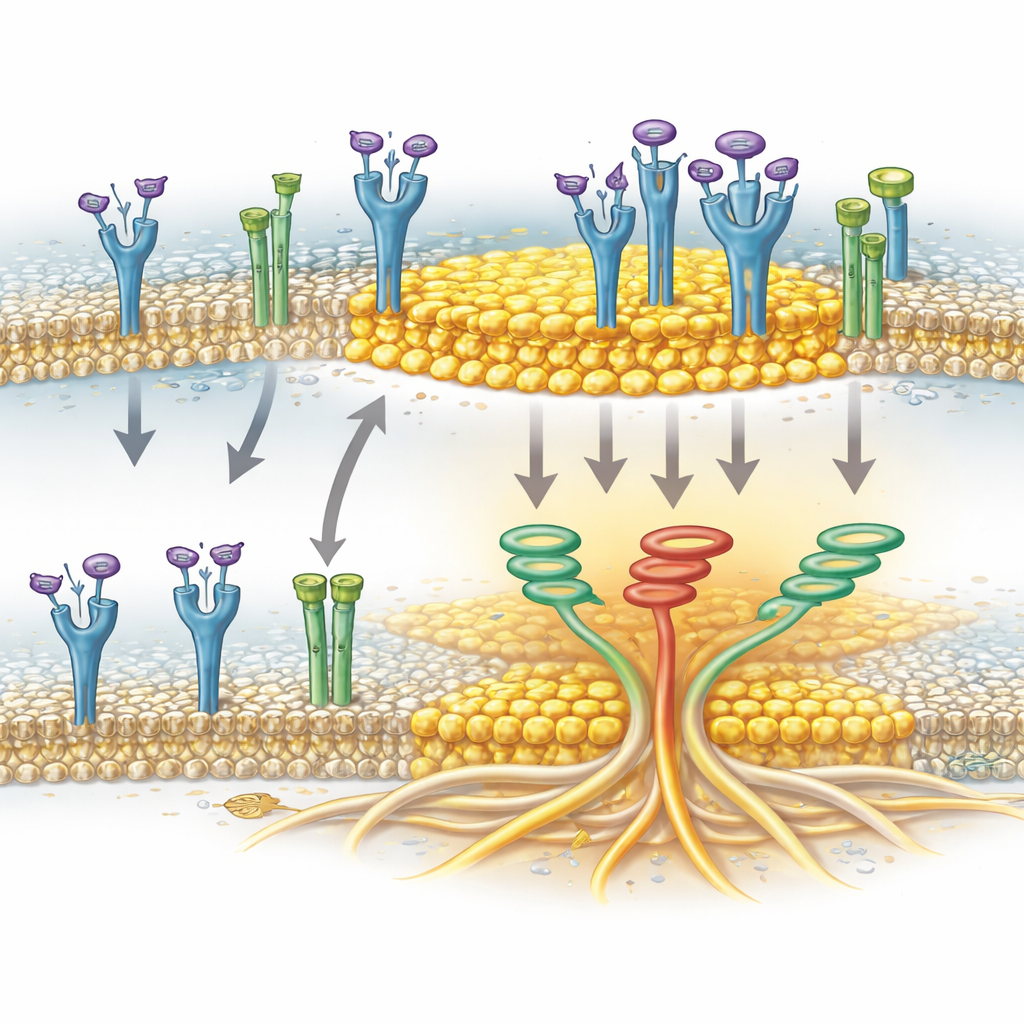
Kanał jonowy jako pomocnik skupiania receptorów
Badanie identyfikuje także zaskakującego pomocnika: TRPA1, białkowy kanał znany przede wszystkim z wykrywania drażniących substancji i stresu oksydacyjnego w nerwach. W komórkach raka trzustki TRPA1 występuje w błonie i może lokalizować się w tratwach lipidowych. Autorzy pokazali, że TRPA1 fizycznie kojarzy się z FGFR2c, gdy receptor jest aktywowany, i że to skojarzenie zbiega się z wzbogaceniem FGFR2c w frakcjach tratw. Po zmniejszeniu poziomów TRPA1 aktywowany FGFR2c przestał efektywnie gromadzić się w obszarach tratw, mimo że same tratwy pozostały nienaruszone. Wskazuje to, że TRPA1 nie jest jedynie biernym pasażerem, lecz aktywnie pomaga eskortować lub stabilizować FGFR2c w tych cholesterolowych platformach, gdzie receptor może skuteczniej uruchamiać sieć sygnałów sprzyjających inwazji.
Co to oznacza dla przyszłych terapii
Podsumowując, praca przedstawia obraz, w którym FGFR2c, TRPA1 i tratwy lipidowe tworzą współpracującą jednostkę wzmacniającą inwazyjne zachowanie komórek raka trzustki. FGFR2c dostarcza sygnał wzrostu, tratwy lipidowe zapewniają fizyczną scenę, na której montują się kompleksy sygnałowe, a TRPA1 pomaga przyprowadzić receptor na tę scenę. Dla czytelnika niebędącego specjalistą kluczowy wniosek jest taki, że nie tylko same cząsteczki powodujące raka, lecz także drobne krajobrazy błonowe, które zajmują, mogą determinować, jak niebezpieczny stanie się guz. Celowanie w FGFR2c, TRPA1 lub stabilność tych bogatych w cholesterol wysp — osobno lub łącznie — może w przyszłości umożliwić osłabienie mechanizmów inwazyjnych komórek raka trzustki w sposób bardziej precyzyjny i specyficzny dla guza.
Cytowanie: Mancini, V., Manganelli, V., Garofalo, T. et al. Role of lipid rafts in the FGFR2c-mediated oncogenic signaling by involvement of TRPA1 channel in pancreatic ductal adenocarcinoma cells. Cell Death Dis 17, 259 (2026). https://doi.org/10.1038/s41419-026-08513-7
Słowa kluczowe: rak trzustki, tratwy lipidowe, FGFR2c, kanał TRPA1, inwazja komórek