Clear Sky Science · pl
Ukierunkowanie na mutacje p53 w raku Y220C, Y220N i Y220S za pomocą małocząsteczkowego stabilizatora rezatapopt
Dlaczego to ma znaczenie dla przyszłych terapii onkologicznych
Nowotwory często unieszkodliwiają p53, białko nazywane czasem „strażnikiem” komórki, przez mutacje, które uniemożliwiają mu kontrolowanie niebezpiecznych komórek. Jedna konkretna zmiana w p53, znana jako Y220C, występuje często w nowotworach litych i stała się polem testowym dla leków mających naprawiać uszkodzone p53 zamiast zabijać komórki bezpośrednio. W tym badaniu zadano praktyczne, ukierunkowane na pacjenta pytanie: czy obiecujący eksperymentalny lek rezatapopt, już testowany klinicznie w przypadku Y220C, mógłby też pomagać osobom, których guzy noszą pokrewne, lecz rzadsze mutacje w tym samym miejscu p53?
Lek zaprojektowany, by załatać pęknięcie w p53
Wiele mutacji p53 powoduje, że białko „rozchyla się” i traci precyzyjny kształt. W mutacji Y220C zmiana tworzy małą wnękę na powierzchni białka — defekt, który chemicy zrozumieli jako możliwy do „zablokowania” dopasowanymi małymi cząsteczkami stabilizującymi p53. Rezatapopt jest jedną z takich cząsteczek, zaprojektowaną w oparciu o wcześniejsze serie chemiczne wiążące się w tej wnęce i działające jak molekularne usztywnienie. Autorzy koncentrują się na dwóch innych mutacjach w tym samym reszcie aminokwasowym, Y220S i Y220N, które także tworzą podobny kieszonkowy defekt, ale destabilizują p53 jeszcze bardziej niż Y220C. Jeśli rezatapopt mógłby także załatać te warianty, podejście medycyny precyzyjnej mogłoby objąć każdego roku tysiące dodatkowych pacjentów. 
Pomiary zdolności rezatapopt do chwytania i usztywniania mutantów p53
Aby to sprawdzić, zespół oczyszczał rdzeń p53 wiążący DNA zawierający zmiany Y220C, Y220S lub Y220N i wystawiał każdy wariant na działanie rezatapopt (oraz bliskich krewnych chemicznych). Przy użyciu testów opartych na temperaturze wykazali, że wszystkie trzy mutacyjne formy białka stają się bardziej stabilne po związaniu leku, przy czym Y220C i Y220S odzyskują praktycznie wytrzymałość podobną do dzikiego typu. Dla kontrastu Y220N odzyskał tylko część utraconej stabilności. Druga technika mierząca wydzielane ciepło przy wiązaniu wyjaśniła dlaczego: rezatapopt przyłącza się bardzo silnie do Y220C (w przybliżeniu dziesiątki nanomoli), nieco słabiej do Y220S i jeszcze słabiej do Y220N, choć wszystkie te wartości mieszczą się w zakresach uznawanych przez chemików medycznych za obiecujące.
Widok molekularnej łaty w atomowych szczegółach
Struktury krystalograficzne o wysokiej rozdzielczości dostarczyły wizualnego wyjaśnienia. We wszystkich trzech mutantach rezatapopt wsuwa się w utworzoną przez mutację szczelinę w zachowanym ułożeniu: jego centralny szkielet wypełnia wnękę, jeden koniec sięga głęboko do kieszeni z klastrem atomów fluoru, a drugi oddziałuje z pobliską pętlą białka. Lek nawiązuje sieć kontaktów, w tym strategicznie umieszczony atom fluoru, który wchodzi w interakcję z łańcuchem głównym białka. W Y220S te interakcje są zachowane z jedynie drobnymi przesunięciami, co pozwala na silną stabilizację. W przypadku Y220N jednak wiązanie leku wymusza skierowanie bocznego łańcucha asparaginy w oleistą część rdzenia białka w sposób energetycznie niekorzystny, a część kontaktów z fluorynowym „kotwiczeniem” leku zostaje utracona. To napięte dopasowanie tłumaczy zarówno słabsze wiązanie, jak i niepełne przywrócenie stabilności. 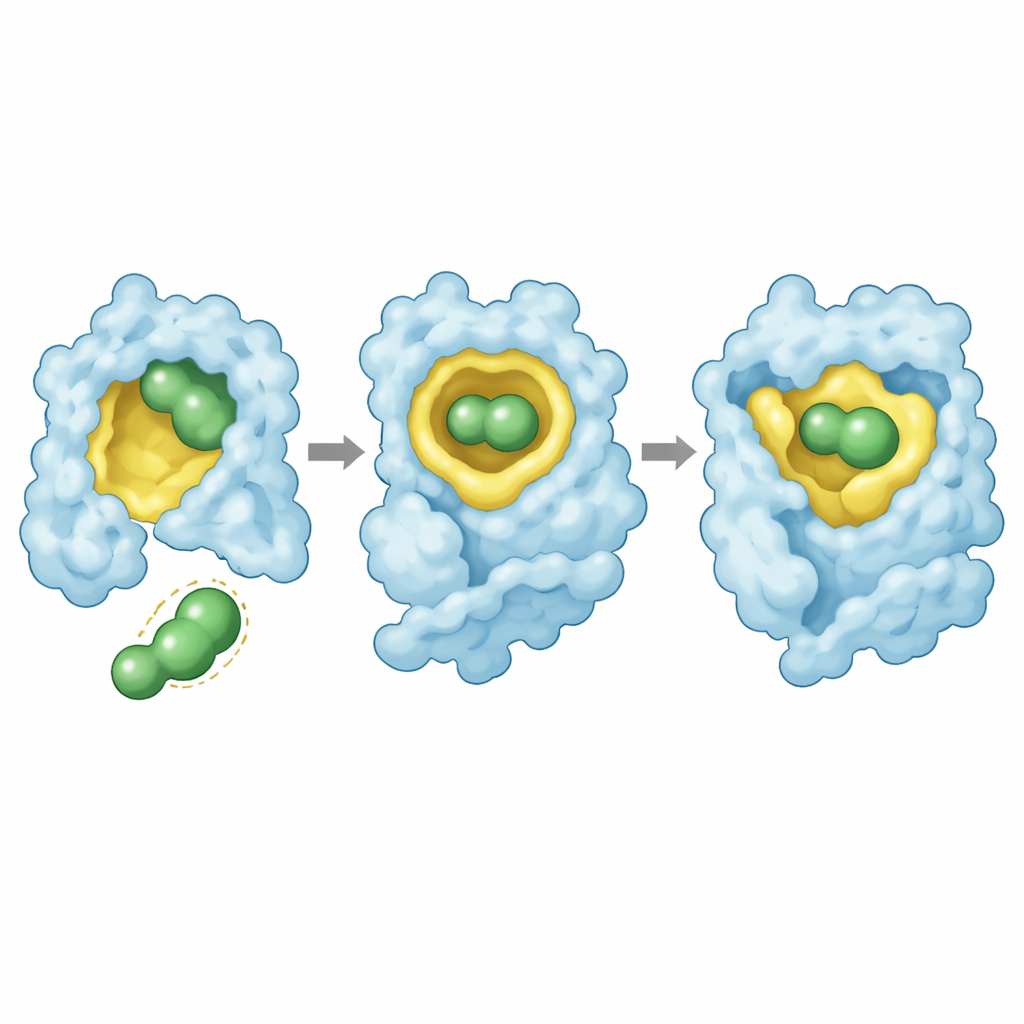
Od naprawy białka do zachowania komórek
Kluczowy test to, czy taka stabilizacja przywraca ochronną rolę p53 wewnątrz żywych komórek. Badacze zmodyfikowali komórki raka płuca pozbawione naturalnego p53, by ekspresjonowały warianty Y220C, Y220S, Y220N lub Y220H. Po leczeniu rezatapoptem komórki niosące Y220C wykazały silną aktywację klasycznych genów docelowych p53 związanych z zatrzymaniem cyklu komórkowego i indukcją śmierci komórkowej. Komórki Y220S wykazały bardzo podobny wzorzec — odzyskanie sfałdowanej, aktywnej formy p53, silna aktywacja genów, spowolnienie proliferacji i zwiększona śmierć komórek — lecz dopiero przy stężeniach leku ponad dziesięciokrotnie wyższych niż te konieczne dla Y220C. Komórki Y220N, w porównaniu, nie wykazywały wyraźnej aktywacji genów docelowych przy tolerowanych dawkach i pozostawały w dużej mierze w stanie nieprawidłowego sfałdowania, chociaż drobne późne efekty wzrostowe sugerują jedynie częściową funkcjonalną naprawę.
Co to oznacza dla pacjentów i przyszłego projektowania leków
Dla osób z guzami niosącymi mutację Y220S wyniki te są ostrożnie zachęcające: rezatapopt może zasadniczo przywrócić ochronne funkcje p53, lecz jedynie przy znacząco wyższych dawkach, co może być trudne do osiągnięcia bezpiecznie u pacjentów. W przypadku Y220N obecny lek wydaje się niewystarczający do pełnej naprawy p53 w realistycznych warunkach. Mimo to strukturalne plany zawarte w tej pracy wskazują, dlaczego obecny projekt działa słabiej i jak przyszłe cząsteczki mogłyby zostać zmodyfikowane, by angażować wszystkie trzy boczne łańcuchy mutantów bez wymuszania ich w niekorzystne pozycje. Innymi słowy, stworzenie prawdziwego leku „pan‑Y220” naprawiającego p53 wygląda na wyzwanie, ale wykonalne, i mogłoby umiarkowanie zwiększyć liczbę pacjentów, którzy skorzystaliby z tej rozwijającej się strategii naprawiania, zamiast zastępowania, własnego supresora nowotworów organizmu.
Cytowanie: Mavridi, D., Funk, J.S., Balourdas, DI. et al. Targeting the p53 cancer mutants Y220C, Y220N, and Y220S with the small-molecule stabilizer rezatapopt. Cell Death Dis 17, 268 (2026). https://doi.org/10.1038/s41419-026-08492-9
Słowa kluczowe: reaktywacja p53, rezatapopt, mutacja Y220C, precyzyjna medycyna onkologiczna, stabilizacja białka