Clear Sky Science · pl
Deubikwitynacja przez OTUD4 stabilizuje EGFR i aktywuje szlak PI3K/AKT, promując inwazyjność potrójnie ujemnego raka piersi
Dlaczego te badania są ważne dla raka piersi
Potrójnie ujemny rak piersi to jedna z najtrudniejszych do leczenia postaci raka piersi, ponieważ brakuje mu typowych markerów hormonalnych i wzrostowych, na które ukierunkowane są liczne leki. W tym badaniu odkryto ukryty „opiekun” — cząsteczkę, która pomaga komórkom nowotworowym utrzymać włączony potężny przełącznik wzrostu. Zrozumienie tego niewidocznego systemu wspierającego może pozwolić naukowcom znaleźć nowe sposoby odcięcia sygnałów napędzających wzrost i rozprzestrzenianie się guza.
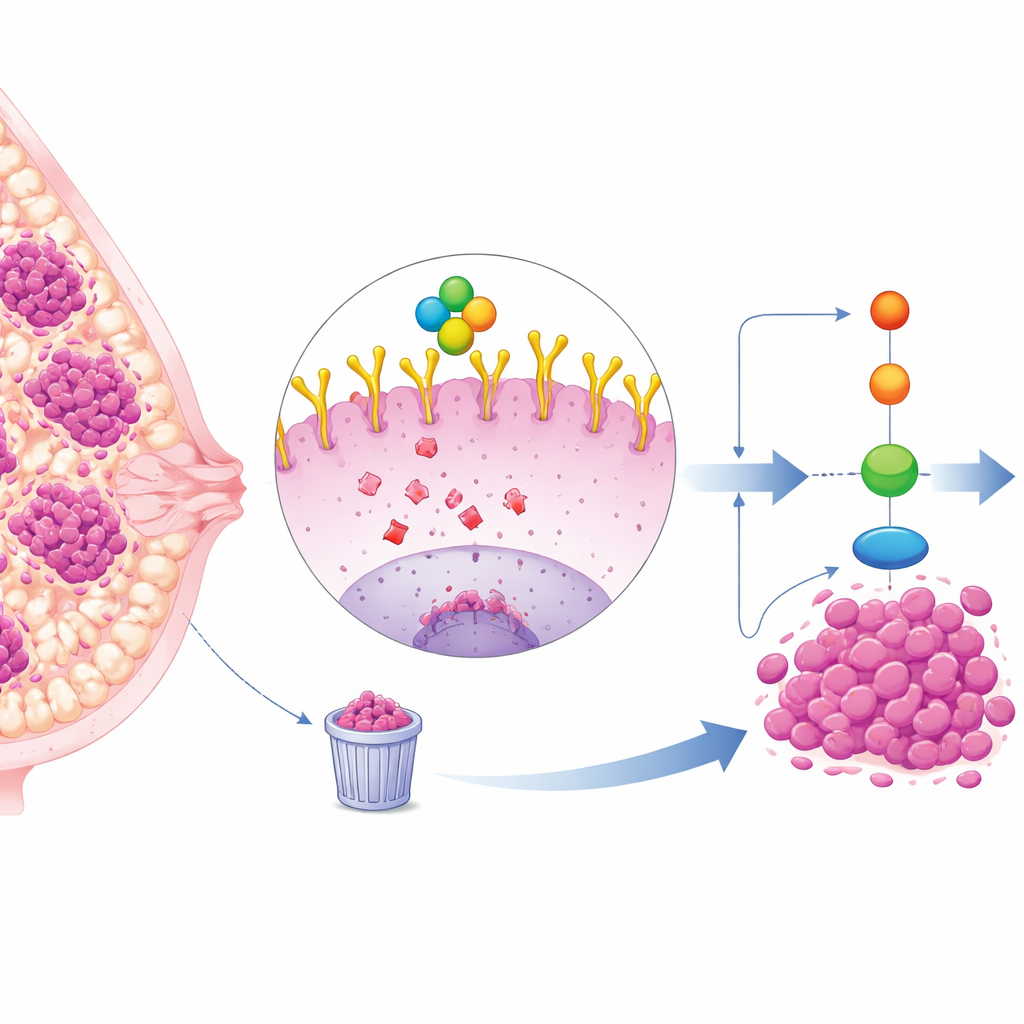
Trudna do leczenia podjednostka raka piersi
Potrójnie ujemny rak piersi (TNBC) stanowi około ćwierci przypadków raka piersi i zwykle rośnie oraz daje przerzuty szybciej niż inne podtypy. Ponieważ komórki TNBC nie wykazują receptorów estrogenowych, progesteronowych ani HER2, standardowe terapie ukierunkowane są mniej skuteczne, pozostawiając chemioterapię i chirurgię jako główne opcje. Wiele guzów TNBC wykazuje jednak wysokie poziomy białka powierzchniowego zwanego EGFR, które działa jak antena odbierająca sygnały wzrostu i przeżycia. Wysoki poziom EGFR wiąże się z gorszymi wynikami, ale leki bezpośrednio blokujące EGFR dawały rozczarowujące rezultaty w praktyce klinicznej, co sugeruje istnienie głębszych warstw regulacji.
Odkrycie ukrytego pomocnika wzrostu guza
Naukowcy skupili się na OTUD4, enzymie usuwającym małe znaczniki białkowe zwane ubikwityną z innych białek. Znaczniki te często działają jak sygnały do usunięcia, oznaczając białka do rozkładu, więc ich usuwanie może stabilizować i chronić oznakowane białko. Korzystając z dużych baz danych dotyczących raka i próbek tkanek od pacjentów, zespół wykazał, że OTUD4 występuje na wyższym poziomie w guzach i liniach komórkowych TNBC niż w normalnej tkance piersi. Pacjenci, których guzy miały więcej OTUD4, mieli gorsze przeżycie, co sugeruje, że OTUD4 zachowuje się jak onkogen — gen wspierający rozwój nowotworu.
Jak OTUD4 nasila złośliwość komórek nowotworowych
Aby sprawdzić, co OTUD4 faktycznie robi w komórkach TNBC, naukowcy obniżyli jego poziom w dwóch powszechnie badanych liniach komórkowych TNBC. Po wyciszeniu OTUD4 komórki nowotworowe rosły wolniej, tworzyły mniej kolonii i były mniej zdolne do migracji w testach gojenia ran i Transwell, co są znaki zmniejszonej agresywności. Gdy natomiast OTUD4 był nadekspresjonowany, obserwowano przeciwne efekty: komórki proliferowały szybciej i poruszały się łatwiej, co wzmacniało wniosek, że OTUD4 napędza złośliwe zachowanie. U myszy guzy powstające z komórek pozbawionych OTUD4 rosły wolniej i wykazywały zmniejszone markery podziału oraz sygnały wzrostowe, potwierdzając te efekty in vivo.
Molukularna tarcza chroniąca EGFR
Zagłębiając się w mechanizm, zespół zastosował przesiewy interakcji białko–białko i testy biochemiczne, aby zidentyfikować EGFR jako bezpośredniego partnera wiążącego OTUD4. Stwierdzono, że OTUD4 przyłącza się do specyficznego regionu EGFR i usuwa łańcuchy ubikwityny typu K48, czyli typ znacznika, który zwykle oznacza białka do zniszczenia przez komórkowe mechanizmy recyklingu. Gdy OTUD4 było zmniejszone, EGFR ulegał szybszej degradacji, podczas gdy aktywność genu EGFR pozostawała bez zmian, co pokazuje, że OTUD4 działa po syntezie EGFR, a nie na poziomie DNA czy RNA. Zablokowanie układu degradacji białek przywracało poziomy EGFR, podkreślając, że kluczowym krokiem jest ochrona przed rozpadem. Dzięki stabilniejszemu EGFR na powierzchni komórki główny wewnątrzkomórkowy szlak sygnałowy PI3K/AKT/mTOR pozostaje aktywny, napędzając wzrost i przeżycie komórek.
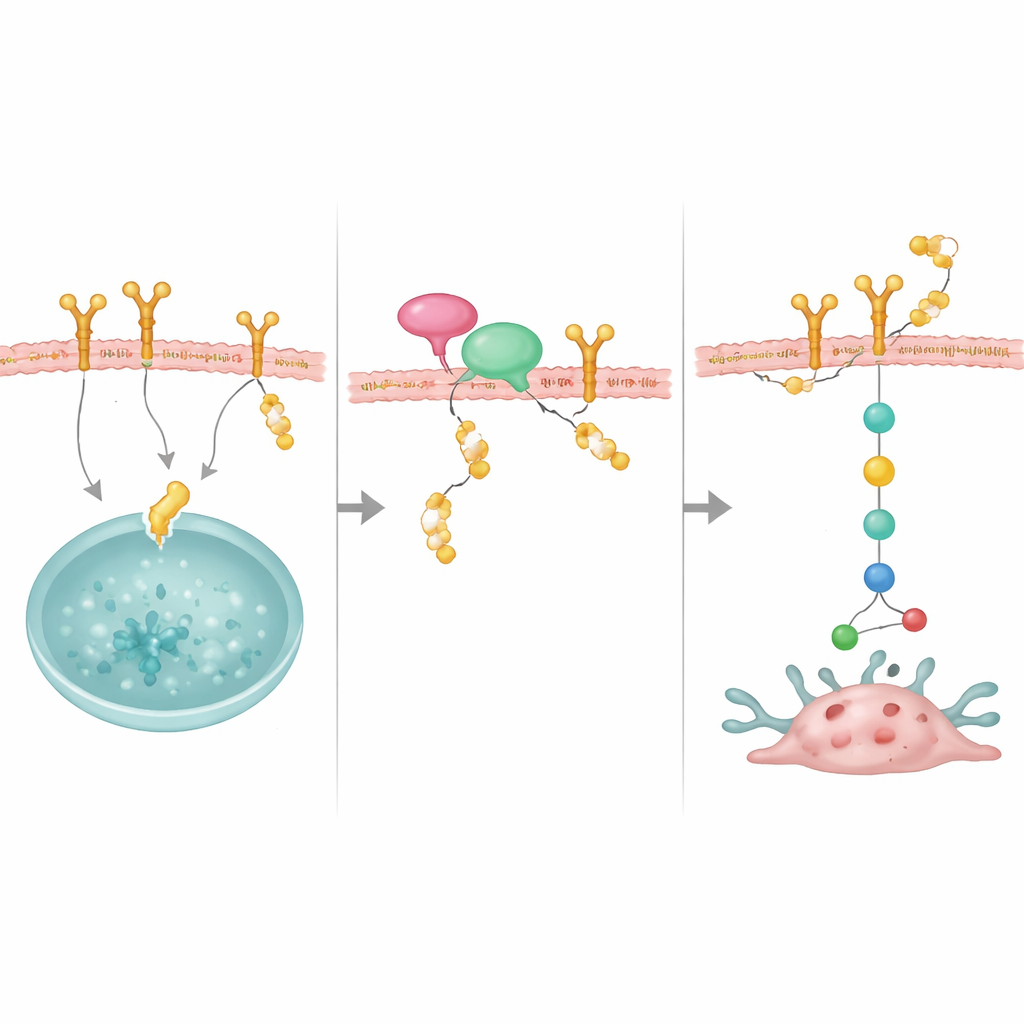
Adaptor przyprowadzający opiekuna do celu
Badanie ujawniło także ważnego partnera, NRP1, białko błonowe wcześniej powiązane z agresywnymi rakami piersi. NRP1 wiąże zarówno OTUD4, jak i EGFR, i pomaga umiejscowić OTUD4 tak, by ratowało EGFR przed zniszczeniem. Gdy NRP1 było zredukowane, EGFR stawał się mniej stabilny, a jego sygnały wzrostowe osłabły, mimo że poziomy OTUD4 nie ulegały zmianie. Nadprodukcja OTUD4 mogła częściowo skompensować utratę NRP1, co sugeruje, że NRP1 działa jak platforma dokująca, rekrutująca OTUD4 do EGFR. Te molekuły razem tworzą stabilizujący kompleks, który utrzymuje obfitość EGFR na powierzchni komórki.
Co to oznacza dla przyszłych terapii
Ujawniając, jak OTUD4 i NRP1 współdziałają, by osłonić EGFR przed degradacją, badanie identyfikuje nowy punkt kontroli kluczowego sygnału wzrostowego w potrójnie ujemnym raku piersi. Zamiast próbować bezpośrednio blokować aktywność EGFR w jego miejscu aktywnym, przyszłe terapie mogą dążyć do zakłócenia ochronnych działań OTUD4 lub jego rekrutacji przez NRP1, obniżając poziom EGFR i osłabiając szlak PI3K/AKT, który napędza wzrost guza. Choć potrzebne są dalsze prace nad znalezieniem bezpiecznych i skutecznych inhibitorów OTUD4 oraz zrozumieniem możliwych dróg ucieczki używanych przez komórki nowotworowe, wyniki otwierają obiecujące drogi do bardziej precyzyjnych terapii przeciwko temu trudnemu podtypowi raka piersi.
Cytowanie: Ren, Y., Zhou, F., Tan, Z. et al. OTUD4 deubiquitination stabilizes EGFR and activates the PI3K/AKT pathway to promote the invasiveness of triple-negative breast cancer. Cell Death Dis 17, 245 (2026). https://doi.org/10.1038/s41419-026-08482-x
Słowa kluczowe: potrójnie ujemny rak piersi, sygnalizacja EGFR, OTUD4, szlak PI3K AKT, degradacja białek