Clear Sky Science · pl
Celowanie w fused in sarcoma (FUS): nowa strategia antysensowna w leczeniu idiopatycznego włóknienia płuc
Dlaczego bliznowacenie płuc ma znaczenie
Idiopatyczne włóknienie płuc (IPF) to nieuchronna choroba płuc, w której delikatne pęcherzyki oddechowe stopniowo zamieniają się w sztywną tkankę bliznowatą, utrudniając każdy oddech. Dostępne leki mogą spowolnić ten proces, ale nie potrafią go zatrzymać ani odwrócić. W tej pracy badano nowy cel — FUS, białko uczestniczące w przetwarzaniu informacji genetycznej w komórce — oraz sprawdzono, czy wyłączenie go za pomocą zaprojektowanego łańcucha podobnego do DNA może złagodzić bliznowacenie i wspomóc naprawę uszkodzonych płuc.
Kontroler ruchu komórkowego, który zawodzi
FUS to białko, które zazwyczaj znajduje się w jądrze komórkowym, gdzie pomaga zarządzać przetwarzaniem i wykorzystaniem RNA — roboczej kopii naszych genów. W chorobach mózgu, takich jak ALS, FUS może zachowywać się nieprawidłowo: opuszcza jądro, aglomeruje w obszarach zewnątrzjądrowych i zaburza prawidłowe funkcje komórki. Autorzy zastanawiali się, czy podobne zaburzenie mogłoby napędzać bliznowacenie w IPF. Badali fibroblasty płucne — komórki tkanki łącznej, które odkładają materiał bliznowaty — od pacjentów z IPF i od zdrowych dawców. W komórkach IPF poziomy FUS były ogólnie wyższe i, co kluczowe, znacznie więcej FUS znajdowało się w cytoplazmie niż w komórkach zdrowych. Przy użyciu mikroskopii elektronowej o wysokiej rozdzielczości potwierdzili, że to białko występuje nieprawidłowo poza jądrem, co sugeruje, że jego normalna kontrola nad RNA może być zaburzona w płucach włókniejących. 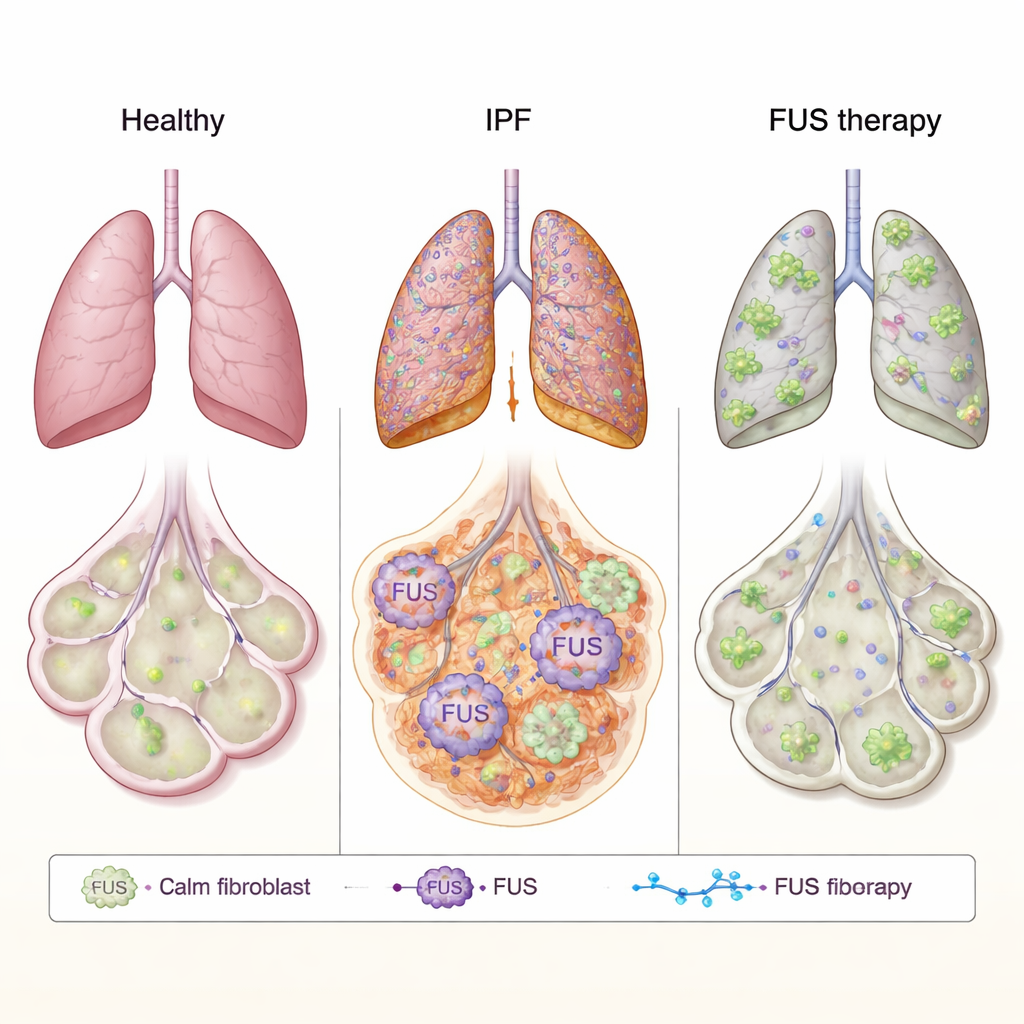
W jaki sposób FUS napędza komórki bliznowate
Aby sprawdzić, co to źle zachowujące się białko robi w praktyce, badacze zwiększyli ekspresję FUS w zdrowych fibroblastach i zmniejszyli ją w fibroblastach z IPF. Dodatkowy FUS pobudzał zdrowe komórki do szybszego dzielenia się, podczas gdy redukcja FUS w komórkach IPF spowalniała ich wzrost i migrację — dwa zachowania kluczowe dla tworzenia blizn. Zespół zastosował następnie technikę, która „zamraża” interakcje białko–RNA i odczytuje, które RNA są związane z FUS. W fibroblastach IPF FUS był związany z wieloma komunikatami genetycznymi promującymi włóknienie, w tym kodującymi kolagen, czynniki wzrostu takie jak TGF‑β, oraz sygnały zapalne. Innymi słowy, FUS działał jako węzeł łączący sieć pro‑bliznowatych komunikatów.
Wyciszenie sygnału precyzyjnym lekiem
W badaniu przetestowano oligonukleotyd antysensowny o nazwie ION363 — krótki, chemicznie zmodyfikowany łańcuch zaprojektowany tak, by wiązać RNA FUS i uruchamiać jego degradację. Po potraktowaniu fibroblastów IPF ION363 poziomy FUS spadły, komórki zmniejszyły proliferację i migrację, a kluczowe geny budujące bliznę ucichły. Co ważne, efekt ten nie wynikał z zabijania komórek ani z wymuszenia ich starzenia; wydawał się raczej resetować ich zachowanie. Gdy ten sam zabieg zastosowano na cienkich przekrojach tkanki płucnej z IPF utrzymywanych przy życiu w laboratorium, grupy genów związane z macierzą zewnątrzkomórkową, zapaleniem i nieprawidłowym nabłonkiem zostały stłumione, podczas gdy geny związane z produkcją surfaktantu i funkcją pęcherzykową zostały wzmocnione. Leczenie zmniejszyło także barwienie kolagenu i zwiększyło markery funkcjonalnych komórek powierzchni płuc, co sugeruje przesunięcie od bliznowacenia w kierunku naprawy.
Pomaganie odrastaniu uszkodzonych pęcherzyków
Ponieważ drobne komórki wyściełające pęcherzyki — znane jako komórki pęcherzykowe typu II — są kluczowe dla naprawy płuc, badacze stworzyli trójwymiarowe „alveolosfery” z komórek pacjentów, aby naśladować miniaturowe jednostki płucne. W hodowlach z pacjentów z IPF te struktury zwykle słabo przetrwały. Po leczeniu ION363 powstało więcej alveolosfer, rosły one większe i wykazywały większą aktywność lizosomalną — cechę aktywnej odnowy. Szczegółowe barwienia ujawniły więcej komórek noszących markery dojrzałych komórek odpowiedzialnych za wymianę gazową, co wskazuje, że wyciszenie FUS nie tylko osłabiło aktywność fibroblastów, ale także zachęciło uszkodzony nabłonek do odbudowy zdrowszej powierzchni. 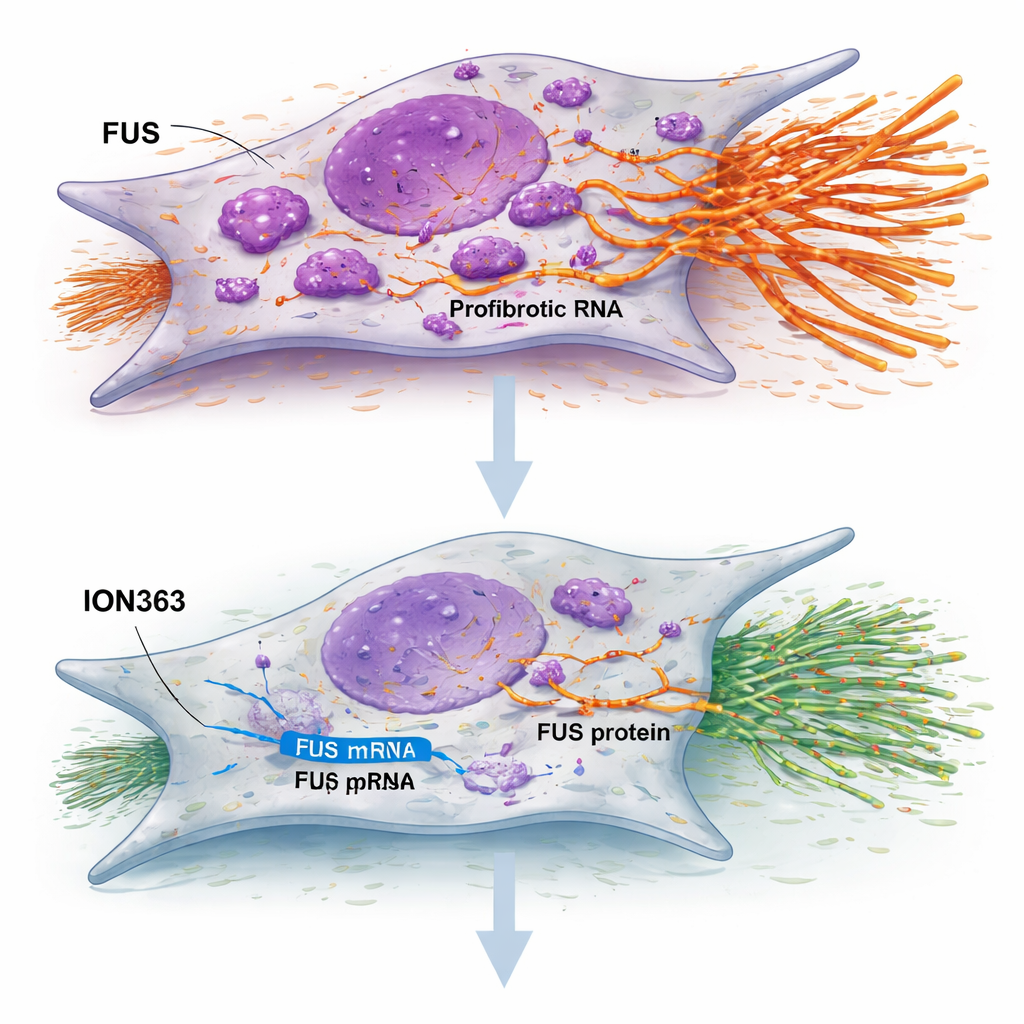
Co to może znaczyć dla pacjentów
W podsumowaniu praca przedstawia FUS jako główny przełącznik w IPF, łączący nadaktywne, tworzące blizny fibroblasty z zawodzącą naprawą delikatnych pęcherzyków. Dzięki wyciszeniu FUS ukierunkowanym lekiem antysensownym badacze mogli osłabić programy genetyczne sprzyjające włóknieniu, zmniejszyć akumulację kolagenu i wspierać regenerację w modelach płuc pochodzących od pacjentów. Chociaż podejście to znajduje się wciąż na etapie laboratoryjnym i będzie wymagać ostrożnych badań na modelach zwierzęcych oraz w badaniach klinicznych, sugeruje, że IPF mogłoby być kiedyś leczone nie tylko przez spowalnianie bliznowacenia, lecz przez bezpośrednie przywracanie równowagi programów komórkowych kontrolujących uraz i naprawę płuc.
Cytowanie: Katariya, B.B., Chillappagari, S., Arnold, L. et al. Targeting fused in sarcoma (FUS): a novel antisense strategy for treating idiopathic pulmonary fibrosis. Sig Transduct Target Ther 11, 70 (2026). https://doi.org/10.1038/s41392-026-02585-9
Słowa kluczowe: idiopatyczne włóknienie płuc, oligonukleotyd antysensowny, białko FUS, włóknienie płuc, naprawa pęcherzyków płucnych