Clear Sky Science · pl
Onkogen HPV16 E7 zwiększa cechy komórek macierzystych poprzez regulację osi APC2/SPIN4/β-katenina w raku szyjki macicy
Dlaczego to badanie ma znaczenie
Rak szyjki macicy nadal jest jedną z głównych przyczyn zgonów kobiet na świecie, zwłaszcza tam, gdzie dostęp do badań przesiewowych i szczepień jest ograniczony. Naukowcy wiedzą, że niektóre typy wirusa brodawczaka ludzkiego (HPV), w szczególności HPV16, są kluczowymi czynnikami tej choroby, jednak szczegółowe mechanizmy, dzięki którym wirus utrzymuje nowotwory w stanie agresywnym i skłonnym do nawrotów, są wciąż odkrywane. To badanie opisuje, w jaki sposób jeden z białek HPV, zwany E7, pomaga podtrzymywać niewielką, ale potężną populację „nowotworowych komórek macierzystych”, które napędzają wzrost guza, jego rozprzestrzenianie się i oporność na terapię — co daje wskazówki do opracowania nowych, bardziej precyzyjnych terapii.
Od powszechnego wirusa do niebezpiecznego nowotworu
Większość zakażeń HPV ustępuje samoistnie, ale przewlekłe zakażenie typami wysokiego ryzyka może przekształcić zdrowe komórki szyjki macicy w nowotworowe. Białko wirusowe E7 odgrywa w tym procesie kluczową rolę: unieszkodliwia istotne mechanizmy zabezpieczające, które normalnie kontrolują podział komórek. Wcześniejsze prace tej grupy badawczej wykazały, że HPV16 E7 wzmacnia cechy podobne do komórek macierzystych w komórkach raka szyjki macicy, co utrudnia ich eliminację. W obecnym badaniu zespół postanowił odwzorować sieci genów kontrolowane przez E7, aby zrozumieć dokładnie, w jaki sposób utrzymuje on przy życiu i sprzyja rozwojowi tych niebezpiecznych komórek.
Śledzenie wpływu E7 wewnątrz komórek nowotworowych
Aby zbadać wpływ E7, badacze użyli linii komórkowych raka szyjki macicy hodowanych w laboratorium i zmniejszyli poziomy E7 za pomocą małych interferujących RNA, narzędzia, które tymczasowo wycisza konkretne geny. Następnie zmierzyli, które geny zmieniły aktywność w całym genomie. Połączyli to z serią testów funkcjonalnych: tempo wzrostu komórek, zdolność do migracji i inwazji przez sztuczne membrany oraz łatwość tworzenia kulistych skupisk w hodowli — cecha charakterystyczna komórek nowotworowych o właściwościach macierzystych. Badali także guzy hodowane u myszy oraz analizowali obszerne publiczne bazy danych nowotworowych, aby sprawdzić, jak ich obserwacje korelują ze wzorcami w próbkach pacjentów.
Zaskakująca rola znanego szlaku
Eksperymenty mapujące geny silnie wskazały na szlak Wnt/β-katenina, dobrze znany regulator normalnych komórek macierzystych i wielu nowotworów. Po wyciszeniu E7 poziomy β-kateniny spadały, co sugerowało wyłączenie tego szlaku. Jednocześnie zespół zaobserwował istotne zmiany w genie APC2. W wielu innych nowotworach białka związane z APC działają jak hamulec sygnalizacji Wnt, pomagając kontrolować wzrost komórek. W tym przypadku komórki raka szyjki macicy wydawały się jednak wykorzystać APC2 w niespodziewany sposób: gdy APC2 było zmniejszone, komórki nowotworowe rosły wolniej, miały mniejszą zdolność do poruszania się i inwazji oraz utraciły cechy podobne do komórek macierzystych. U myszy guzy z długotrwałym wyciszeniem APC2 były znacznie mniejsze, a jednocześnie zwierzęta pozostały w dobrym stanie zdrowia, co sugeruje potencjalnie bezpieczne okno terapeutyczne.
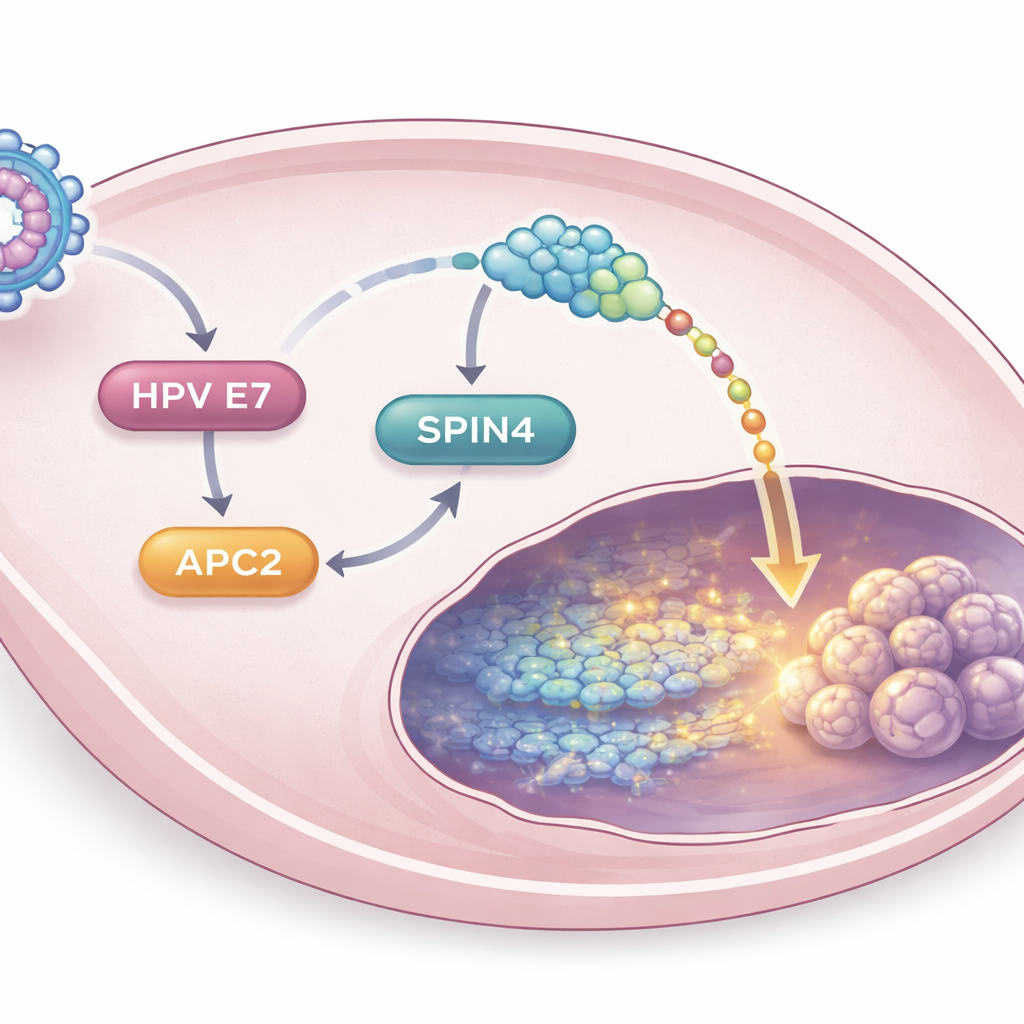
Odkrycie nowego łańcucha sprzyjającego nowotworowi
Zagłębiając się dalej, naukowcy wykazali, że HPV16 E7 zwiększa poziomy APC2 pośrednio przez inne białko o nazwie E2F1, które pomaga włączaniu zestawów genów związanych z wzrostem. Gdy APC2 jest podwyższone, z kolei zwiększa aktywność mniej znanego białka SPIN4. Analiza danych ludzkich guzów wykazała, że SPIN4 jest bardziej obfite w raku szyjki macicy niż w tkance prawidłowej, a wyższe poziomy korelują z gorszym przeżyciem. W badaniach laboratoryjnych wyłączenie SPIN4 osłabiało zdolność APC2 do napędzania wzrostu komórek, inwazji, aktywności Wnt/β-katenina i zachowań przypominających komórki macierzyste. W eksperymentach na mysich guzy pozbawione SPIN4 były mniejsze i wykazywały obniżone markery związane z „macierzystością”. Razem te odkrycia przedstawiają etapowy łańcuch — HPV16 E7 do APC2 do SPIN4 do Wnt/β-katenina — który wspólnie utrzymuje komórki raka szyjki macicy w stanie agresywnym i macierzystym.
W kierunku inteligentniejszych terapii
Dla czytelników niebędących specjalistami kluczowy wniosek jest taki, że to badanie identyfikuje dotąd nieuznaną sieć połączeń wewnątrz nowotworów napędzanych przez HPV. Zamiast działać jak prosty wyłącznik, wirusowe białko E7 przejmuje kontrolę nad konkretną sekwencją białek gospodarza — APC2 i SPIN4 — aby podtrzymywać niebezpieczną pulę komórek-nasion nowotworu poprzez szlak Wnt/β-katenina. Ta oś nie tylko pomaga wyjaśnić, dlaczego niektóre guzy są tak uporczywe, ale także uwypukla kilka nowych celów, do których mogą być ukierunkowane leki lub terapie łączone, szczególnie u pacjentów, których nowotwory opierają się standardowemu leczeniu. Skupienie się na wirusowo ukształtowanej architekturze, która utrzymuje komórki „zarodowe” guza, może uczynić przyszłe terapie skuteczniejszymi w zapobieganiu odrastaniu i poprawie długoterminowych wyników.
Cytowanie: Shen, T., Ma, Y., Wu, T. et al. Human papillomavirus16 E7 enhances cell stemness by regulating the APC2/SPIN4/β-catenin axis in cervical cancer. Oncogenesis 15, 10 (2026). https://doi.org/10.1038/s41389-026-00602-8
Słowa kluczowe: rak szyjki macicy, ludzki wirus brodawczaka, komórki nowotworowe macierzyste, szlak Wnt beta-katenina, sygnalizacja onkogenna