Clear Sky Science · nl
Multimodale sensortechnologieën voor HPAI-biosurveillance in pluimveeproductiesystemen
Waarom vogelgriep op boerderijen ons allemaal aangaat
Hoogpathogene aviaire influenza, vaak HPAI of vogelgriep genoemd, is niet langer alleen een probleem voor kippen op afgelegen boerderijen. Recente golven van de H5N1-stam hebben meer dan 168 miljoen vogels in de Verenigde Staten uitgeroeid, de eierprijzen sterk opgedreven en zich zelfs verspreid naar melkvee en mensen. Dit overzichtsartikel legt uit hoe nieuwe “slimme” sensortechnologieën—luisteren naar dierengeluiden, luchtmonsters in stallen nemen en snelle genetische tests ter plaatse uitvoeren—uitbraken eerder kunnen opsporen, voedselvoorraden kunnen beschermen en het risico kunnen verkleinen dat een gevaarlijk influenzavirus zich aanpast om zich gemakkelijk onder mensen te verspreiden.
De groeiende dreiging op boerderijen en bij mensen
In de afgelopen jaren heeft een nieuwe tak van het H5N1-virus (clade 2.3.4.4b) zich wijd verspreid door het Amerikaanse pluimvee en meer recentelijk door melkveekuddes. Elke uitbraak dwingt boeren hun hele koppels te ruimen, wat verliezen van meer dan 1,4 miljard dollar veroorzaakt en plotselinge tekorten aan eieren en vlees met zich meebrengt. Tegelijkertijd zijn er in de Verenigde Staten meer dan 70 menselijke infecties geregistreerd, vooral onder laagbetaalde werknemers die geïnfecteerde dieren hanteren en vaak beperkte toegang tot gezondheidszorg hebben. Kaarten en surveillancedata tonen dat golven van H5N1 bij vogels vaak samenvallen met de gebruikelijke winterpieken van seizoensgriep bij mensen, wat een gedeeld risicolandschap aan de grens tussen dieren en mensen creëert. Die overlap maakt het extra belangrijk om te volgen wat er gebeurt in stallen en weiden, evenals in klinieken.
Hoe dit virus werkt en waarom het zich zo gemakkelijk verspreidt
Aviaire influenzavirussen zijn kleine, omhulde deeltjes die hun genetisch materiaal in acht afzonderlijke RNA-segmenten dragen. Twee oppervlakte-eiwitten, hemagglutinine (H) en neuraminidase (N), geven bekende aanduidingen zoals H5N1 of H3N2 en bepalen welke soorten het virus kan infecteren en hoe ernstig de ziekte kan zijn. Laagpathogene stammen blijven meestal in de darmen en luchtwegen van een vogel en veroorzaken vaak weinig zichtbare symptomen. Daarentegen hebben hoogpathogene stammen zoals het huidige H5N1 een speciale “cleavage site” op het H-eiwit waardoor het virus door het hele lichaam kan vermenigvuldigen, wat kan leiden tot plotselinge sterfte bij 90–100% van de getroffen vogels. Het gesegmenteerde genoom maakt het ook gemakkelijk voor influenzavirussen uit verschillende gastheren om stukken uit te wisselen en te evolueren, wat verklaart waarom infecties over soorten heen bij runderen, katten of wilde dieren zo zorgwekkend zijn: elke nieuwe gastheer biedt een kans voor het virus om te veranderen.
Beperkingen van de huidige biosecurity en testen
Pluimveebedrijven volgen al strikte biosecurityregels, waaronder gecontroleerde toegang, desinfectie en visuele gezondheidscontroles. Toch hebben grote HPAI-uitbraken plaatsgevonden zelfs op boerderijen die aan deze normen voldoen. Eén reden is snelheid: traditionele surveillance steunt op het opmerken van zieke vogels, het nemen van swabs en het verzenden naar een verafgelegen laboratorium voor PCR-testen, een proces dat twee of drie dagen kan duren. Omdat H5N1 een koppel in ongeveer 48 uur kan doden, laat deze vertraging een venster open voor het virus om door stallen te razen en zich tussen boerderijen te verspreiden. Genoeg vogels bemonsteren in enorme koppels is ook moeilijk, en routinematige protocollen testen zelden stof, water of oppervlakken waar het virus ongemerkt kan blijven. Als gevolg daarvan glippen vroege infecties, milde gevallen en lage niveaus van besmetting vaak door de verdediging.
Luisteren, snuffelen en zien: nieuwe manieren om uitbraken te detecteren
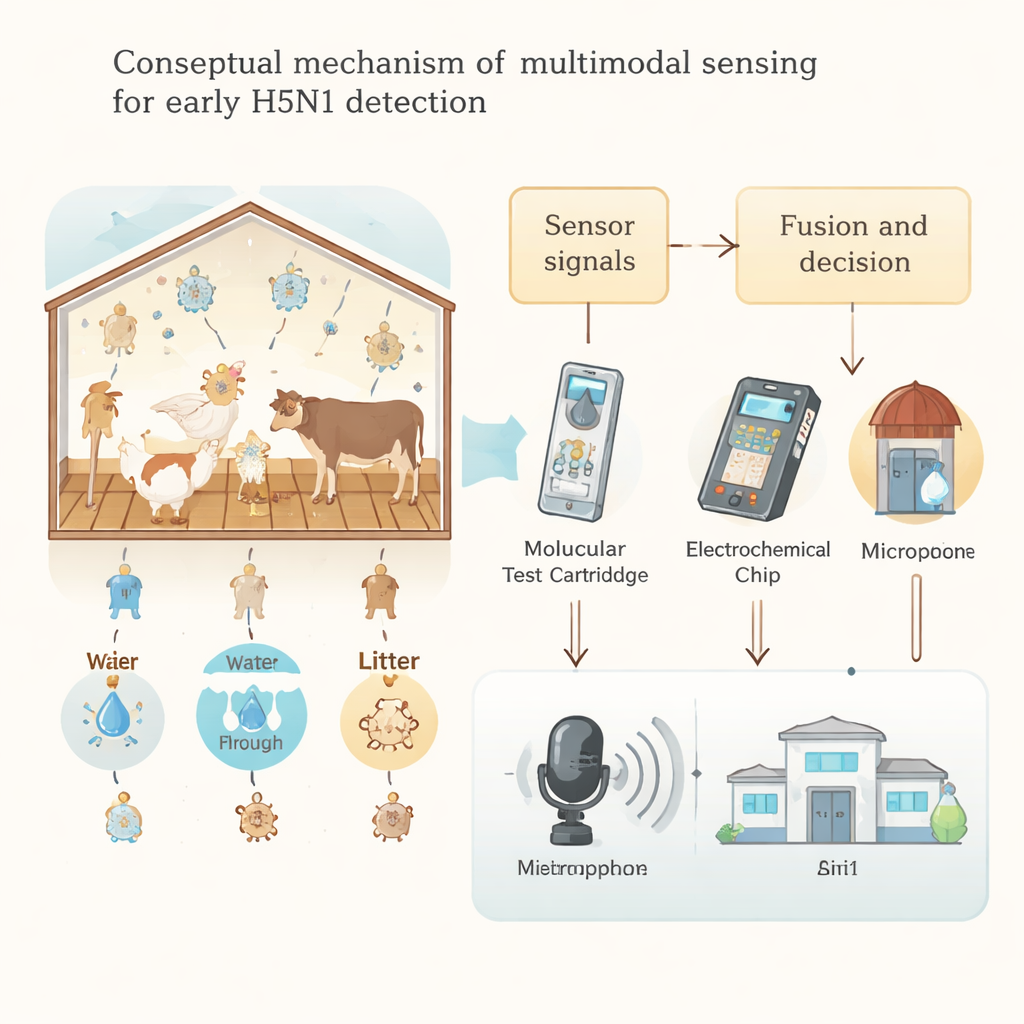
De auteurs betogen dat boerderijen multimodale sensing nodig hebben—meerdere, elkaar aanvullende manieren om op problemen te letten. Aan de gerichte kant zijn er hulpmiddelen die rechtstreeks naar het virus of zijn componenten zoeken: draagbare methoden die viraal RNA bij één temperatuur versterken, programmeerbare CRISPR-gebaseerde tests die binnen een uur resultaten geven, en compacte elektrochemische en optische biosensoren die virale eiwitten in lucht, water of swabs kunnen detecteren. Aan de niet-gerichte kant zijn er methoden die algemene ziekteverschijnselen opsporen zonder zich druk te maken over welke microbe verantwoordelijk is, zoals thermische camera’s die koorts detecteren, lasers die chemische handtekeningen van stalstof lezen, en microfoonsystemen die de geluidsprofielen van gezonde en zieke koppels leren. Bijvoorbeeld kunnen deep-learningmodellen subtiele veranderingen in kippenvocalisaties detecteren één tot twee dagen vóór zichtbare ziekte, terwijl geavanceerde lichtverstrooiingsmethoden virusgerelateerde moleculen onderscheiden in aerosolen die gemengd zijn met gewoon stalstof.
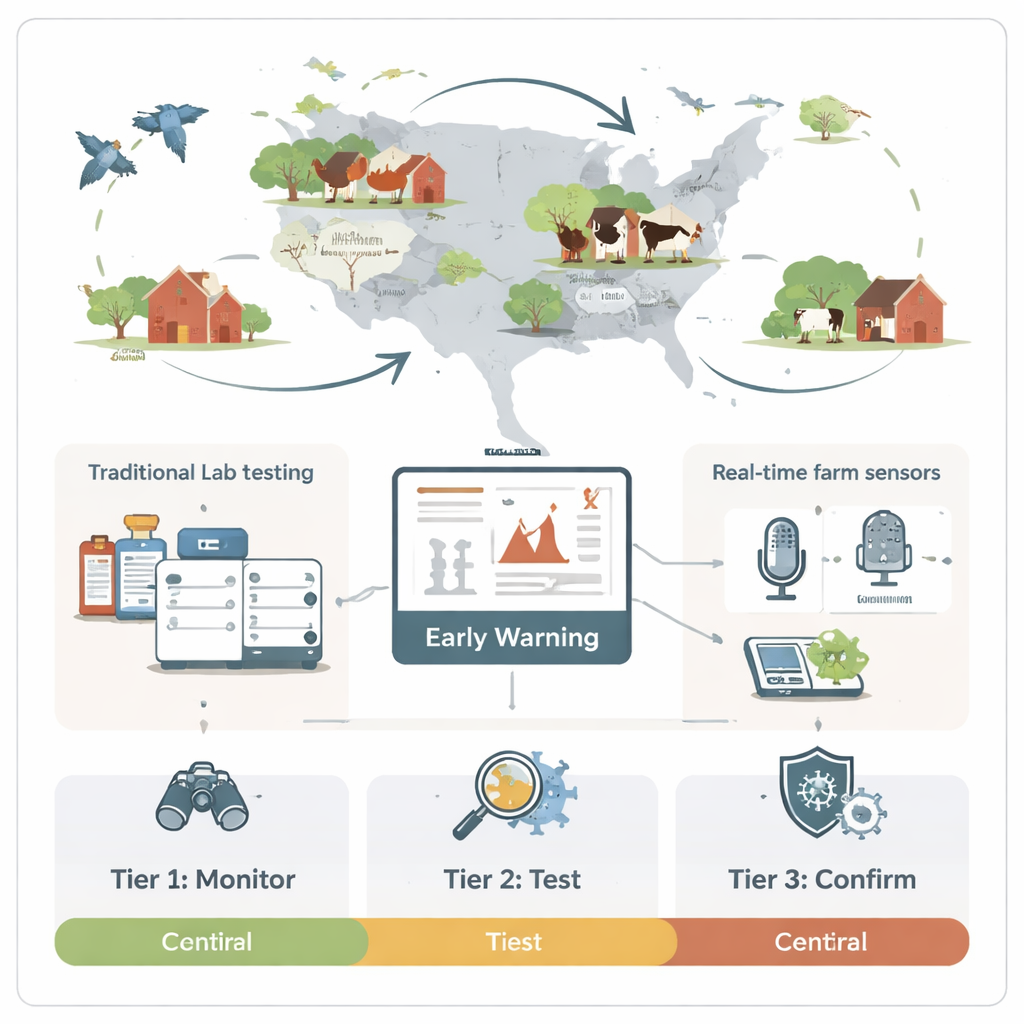
Het opbouwen van een gelaagd vroegwaarschuwingssysteem
In plaats van elk hulpmiddel overal te gebruiken, stelt de review een drielaags systeem voor. In Laag 1 draaien goedkope sensoren continu op de achtergrond, luisteren naar abnormaal hoesten, volgen zwevende deeltjes of scannen stof op verdachte chemische signalen. Als deze brede alarmen een drempel overschrijden, treedt Laag 2 in werking: snelle moleculaire tests en biosensoren op de boerderij controleren gerichte monsters zoals luchtconcentraten of swabs, typisch binnen 30–60 minuten. Alleen wanneer deze snellere screens daadwerkelijk gevaar suggereren, begint Laag 3 met bevestigende labtests zoals volledige PCR-pakketten of virusisolatie die een dag of langer duren. Deze stapsgewijze aanpak balanceert snelheid en betrouwbaarheid, vermindert paniek over valse alarmen en wint toch kostbare tijd vergeleken met wachten tot vogels sterven of werknemers duidelijk ziek worden.
Wat dit betekent voor voedsel- en gezondheidsveiligheid
Kort gezegd concludeert het artikel dat het bestrijden van moderne vogelgriep vereist dat boerderijen zich meer als slimme fabrieken gedragen en minder als geïsoleerde schuren. Door oren (akoestische monitoring), neuzen (chemische en moleculaire sensoren) en hersenen (data-fusie-algoritmen) te combineren over dier-, milieu- en menselijke gezondheidssectoren, kan de landbouw verschuiven van reageren op rampen naar het voorspellen ervan. Vroegere detectie betekent minder massa-slachtingen, stabielere prijzen voor eieren, vlees en melk, en lagere kansen dat H5N1 de juiste mutaties oppikt om een menselijke pandemie te starten. Er blijven obstakels—technologiekosten, de behoefte aan training van werknemers en de uitdaging om rumoerige data van zeer verschillende sensoren te combineren—maar multimodale sensing biedt een realistisch pad naar veiligere boerderijen en sterkere One Health-surveillance voor iedereen.
Bronvermelding: Ali, M.A., Ataei Kachouei, M., Jacobs, L. et al. Multimodal sensing technologies for HPAI biosurveillance in poultry production systems. npj Biosensing 3, 11 (2026). https://doi.org/10.1038/s44328-025-00075-6
Trefwoorden: aviary influenza, biosensoren, boerderij surveillance, CRISPR-diagnostiek, akoestische monitoring