Clear Sky Science · nl
Leiding voor percutane nefrostomie met een optische-coherentie-tomografie-endoscoop op basis van convolutionele neurale netwerken
Waarom veiliger toegang tot de nier belangrijk is
Niersteenziekte komt steeds vaker voor, en veel patiënten hebben een klein buisje nodig dat direct in de nier wordt geplaatst om urine af te voeren of stenen te verwijderen. Deze ingreep, percutane nefrostomie genoemd, wordt uitgevoerd door een naald vanaf de rug van de patiënt in het holle centrum van de nier te leiden. Hoewel de punctie klein is, kan het kiezen van het verkeerde pad delicate nierstructuren scheuren of bloedvaten beschadigen, wat tot bloedingen en andere complicaties leidt. Deze studie introduceert een nieuwe hoogresolutie‑beeldvormingssonde, gecombineerd met kunstmatige intelligentie, die in de naaldtip rijdt om artsen te helpen precies te zien waar ze heen gaan en schade te vermijden.
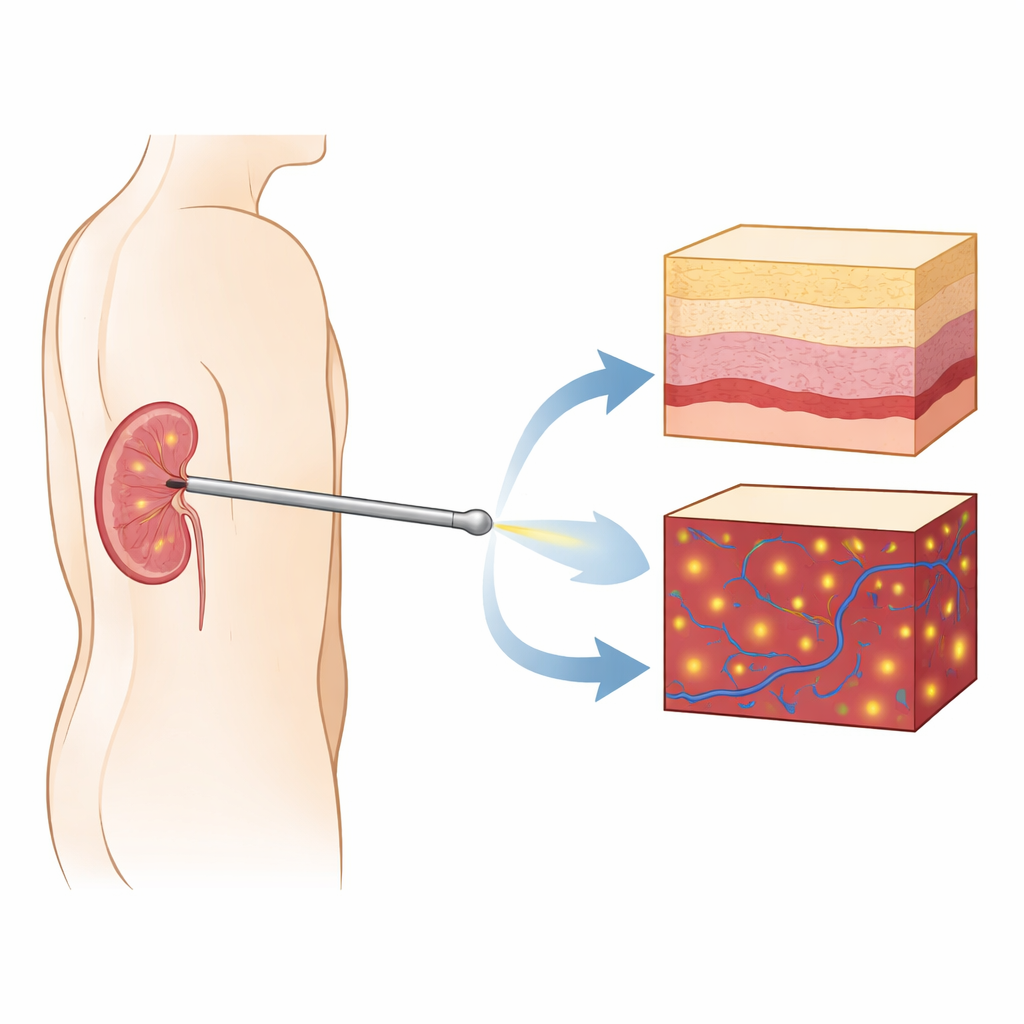
Een piepkleine camera in de naald
De onderzoekers bouwden een vooruitkijkende beeldvormingssonde gebaseerd op optische coherentie‑tomografie (OCT), een lichtgebaseerde methode die dwarsdoorsnede‑“plakjes” van weefsel kan vastleggen met micrometerresolutie—ongeveer tien keer scherper dan standaard medische echografie. Ze plaatsten een dunne gradient‑indexlens in een standaard nefrostomie‑naald zodat de sonde tijdens het inbrengen recht vooruit in de nier kan kijken. In tegenstelling tot gewone endoscopen die vooral oppervlaktebeelden geven, levert dit systeem dieptegerelateerde beelden die laten zien hoe structuren onder de punt veranderen. Dezelfde sonde kan ook in een Doppler‑modus draaien, die bewegende rode bloedcellen benadrukt en daarmee bloedvaten voor de naald onthult voordat ze doorboord worden.
Herkennen van nierlagen in real time
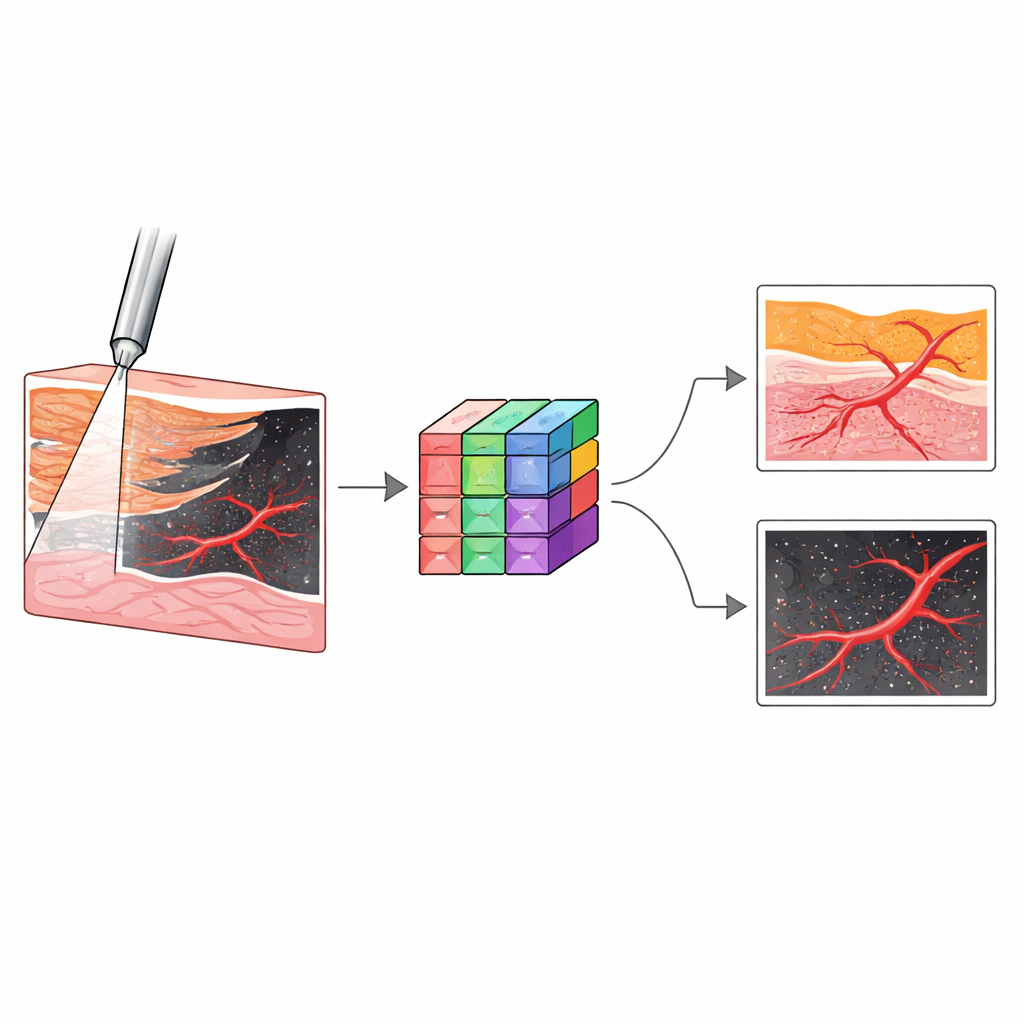
Om te testen of het systeem verschillende nierweefsels kon onderscheiden, voerde het team experimenten uit op 31 geschonken menselijke nieren die onder bijna‑normale omstandigheden werden bewaard. Bij echte procedures zou de naald door de buitenste cortex en binnenste medulla moeten passeren, vervolgens een kelkachtige regio genaamd de calyx binnengaan en tenslotte in het centrale urineverzamelgebied, het pelvis, uitkomen. Afwijken van het traject kan betekenen dat men door vetachtige ruimtes tussen structuren gaat en dunne wanden scheurt. De onderzoekers raakten systematisch met de sonde vijf weefseltypen aan—cortex, medulla, calyx, sinusvet en pelvis—en legden miljoenen OCT‑beelden vast die hun kenmerkende patronen lieten zien. Bijvoorbeeld, cortex en medulla leken glad maar verschilden in diepte; calyx toonde strookachtige overgangen; sinusvet produceerde heldere, gespoten netwerken; en het pelvis verscheen als een lege ruimte onder de sonde.
Een slim systeem leren gevaar te herkennen
Aangezien menselijke experts tijd en training nodig zouden hebben om deze nieuwe beelden tijdens een operatie te interpreteren, wendde het team zich tot deep learning. Ze trainden meerdere convolutionele neurale netwerken om elk OCT‑frame in een van de vijf weefseltypen te classificeren, en selecteerden vervolgens een architectuur genaamd Inception als beste presteerder. In interne tests identificeerde dit model weefsels met een nauwkeurigheid van ongeveer 99,6% en behield het hoge prestaties op extra nieren die het nog nooit eerder had gezien. In een aparte taak gebruikten ze een ander neurale‑netwerkontwerp, nnU‑Net, om bloedvaten in Doppler‑OCT‑beelden te omlijnen. Dit model leerde stromend bloed van het achtergrondweefsel te onderscheiden met zeer grote overlap ten opzichte van door experts handmatig getekende labels, zelfs voor vaten kleiner dan 0,2 millimeter die moeilijk te zien zijn met standaardinstrumenten.
Hoe het zich verhoudt tot de huidige hulpmiddelen
Momenteel vertrouwen artsen meestal op echografie of röntgen‑gebaseerde fluoroscopie om nefrostomie‑naalden te begeleiden. Deze technieken tonen de algemene positie van de nier en het algemene pad van de naald, maar hun relatief grove resolutie maakt het moeilijk precies te weten welk weefsel zich bij de punt bevindt of hoe dicht een bloedvat ligt. In controlexperimenten hadden ervaren radiologen die structurele en Doppler‑echografie gebruikten moeite om het precieze weefsel bij de naaldpunt te identificeren en konden zij kleine vaten niet betrouwbaar visualiseren. Daartegenover bood het OCT‑systeem een gedetailleerd lokaal beeld plus geautomatiseerde analyse die in een fractie van een seconde op moderne grafische processors draait, snel genoeg om feedback te geven terwijl de naald vordert.
Wat dit voor patiënten zou kunnen betekenen
De studie suggereert dat het combineren van een naaldgemonteerde OCT‑sonde met deep learning niertoegangsprocedures zowel veiliger als efficiënter kan maken. In de toekomst zou een arts de gebruikelijke naald met de sonde erin kunnen inbrengen, fijnmazige beelden in real time kunnen bekijken en op de software kunnen vertrouwen om aan te geven wanneer de punt de juiste holte heeft bereikt of een bloedvat nadert. Minder punctiepogingen betekent minder weefseltrauma, lager risico op bloedingen en mogelijk kortere procedures en ziekenhuisverblijven. Hoewel het werk op geschonken nieren in plaats van levende patiënten is gedaan, legt het de basis voor klinische systemen die ook andere naaldgebaseerde ingrepen kunnen begeleiden, van biopsieën en anesthesieblokken tot gerichte medicijnafgifte.
Bronvermelding: Wang, C., Calle, P., Yan, F. et al. Percutaneous nephrostomy guidance by a convolutional-neural-network-based optical coherence tomography endoscope. Commun Eng 5, 47 (2026). https://doi.org/10.1038/s44172-026-00613-8
Trefwoorden: niersteenkirurgie, naaldgeleiding, optische coherentie tomografie, medische beeldvorming AI, detectie van bloedvaten