Clear Sky Science · nl
Kwantisering van micronuclei in hele-scan hematologiebeelden met AI als overdraagbare farmacodynamische biomarker voor remmers van de DNA-schade-respons
Waarom piepkleine vlekjes in bloed grote verhalen kunnen vertellen
Artsen en wetenschappers zoeken voortdurend naar eenvoudige manieren om te zien of een kankermedicijn doet wat het in het lichaam moet doen. Deze studie toont aan dat piepkleine stipjes in rode bloedcellen, micronuclei genoemd, kunnen fungeren als natuurlijke indicatoren van DNA-schade veroorzaakt door bepaalde kankerbehandelingen. Door microscoopachtige hele-scan beeldvorming te combineren met kunstmatige intelligentie (AI) veranderden de onderzoekers een paar druppels bloed in een rijke, geautomatiseerde aflezing van hoe sterk DNA-richtende geneesmiddelen werken.
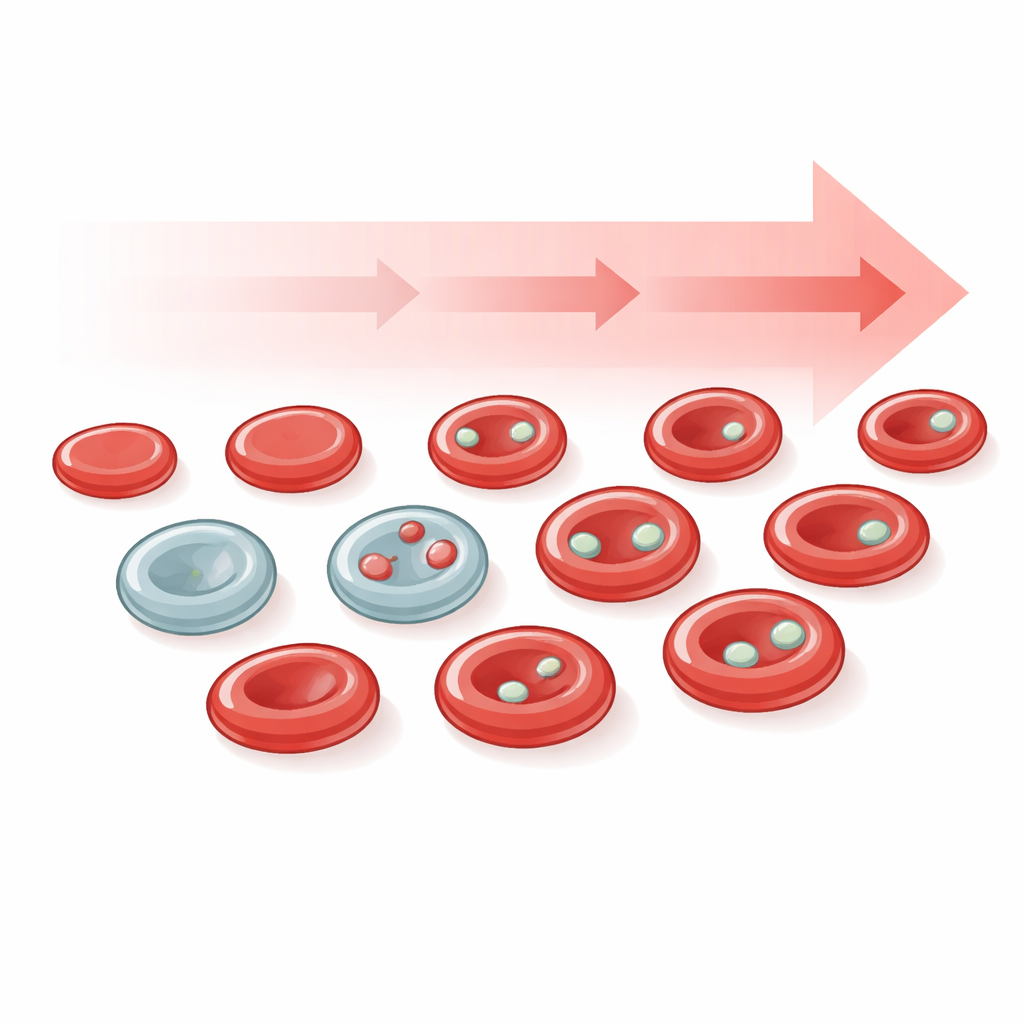
Kleine eilandjes DNA in rode bloedcellen
Micronuclei zijn kleine blaasjes van DNA die los van de hoofdcelkern liggen. Ze ontstaan wanneer chromosomen breken of verkeerd worden verdeeld tijdens celdeling, gebeurtenissen die veel voorkomen bij kanker en na blootstelling aan DNA-schadende middelen. In de meeste weefsels is het lastig om echte micronuclei onder de microscoop te herkennen omdat dunne weefselsneden het zicht kunnen misleiden. Rode bloedcellen bieden een oplossing: tijdens rijping stoten ze normaal gesproken hun hoofdkerndoorsprong uit, maar eventuele eerder gevormde micronuclei kunnen als kleine, goed afgebakende stipjes achterblijven. Deze al lang bekende structuren, historisch aangeduid als Howell–Jolly-lichaampjes, zijn dus handige, echte micronuclei die in de bloedbaan circuleren en kunnen aangeven hoeveel DNA-schade recentelijk heeft plaatsgevonden.
Bloeduitstrijkjes omzetten in data met AI
Het team bouwde een geautomatiseerde pijplijn die begint met standaard bloeduitstrijkjes van muizen, gekleurd met een fluorescerende DNA-dye of met de veelgebruikte May–Grünwald Giemsa-kleurstoffen die in ziekenhuislaboratoria worden toegepast. Hele sneden werden op hoge resolutie gescand en gesuperviseerde deep-learningmodellen werden getraind om rode bloedcellen te herkennen, micronuclei te selecteren en onrijpe reticulocyten te onderscheiden van rijpe erytrocyten op basis van subtiele verschillen in grootte en kleur. Vanuit één afbeelding kon het systeem meer dan 100.000 cellen analyseren, die met micronuclei markeren en zelfs cellen tellen die meer dan één micronucleus bevatten—iets wat conventionele flowcytometrie niet gemakkelijk kan doen.
Kleine veranderingen in bloed koppelen aan medicijnsterkte
De onderzoekers vroegen vervolgens of de frequentie van micronucleus-positieve rode bloedcellen overeenkwam met blootstelling aan DNA-schadende chemotherapie en aan middelen die de DNA-schade-respons blokkeren, zoals PARP-remmers. Bij muizen behandeld met cisplatine of paclitaxel registreerden de AI-gebaseerde tellingen de verwachte stijgingen in micronucleated cellen. Bij tumordragende muizen die behandeld werden met de PARP-remmers olaparib of saruparib, leverden hogere doses grotere toenames op van cellen met micronuclei en sterkere tumorkrimping. Gedurende meerdere weken dagelijkse dosering maakten kleine seriële bloedmonsters (slechts ongeveer 5 microliter elk) het team mogelijk om te volgen hoe micronuclei langzaam opbouwden en vervolgens afnamen nadat de behandeling stopte. Toen ze hun methode op basis van slides vergeleken met standaard flowcytometrie, kwamen de twee benaderingen nauw overeen, wat laat zien dat de nieuwe workflow zowel nauwkeurig als robuust is.
Inzoomen op jonge bloedcellen voor scherpere signalen
Aangezien jonge rode bloedcellen (reticulocyten) vooral waarschijnlijk verse micronuclei bevatten, trainden de onderzoekers hun algoritmen om de rodecelpopulatie op routinegekleurde slides in onrijpe en rijpe cellen te splitsen. Deze verfijning liet zien dat micronuclei veel meer verrijkt en dynamischer waren in reticulocyten dan in oudere cellen, wat een gevoeliger en sneller veranderend signaal van medicijneffect opleverde. De hele-scan afbeeldingen maakten het ook mogelijk om de monstervoorwaarde zelf te monitoren—bijvoorbeeld het detecteren van rode cellen die vervormd waren geraakt door slechte opslag—zodat ondermaatse slides vóór analyse konden worden gemarkeerd, een belangrijke stap voor uiteindelijk klinisch gebruik.
Wat dit zou kunnen betekenen voor toekomstige kankerzorg
De studie toont aan dat een klein bloedmonster, een standaard kleuring van een slide en een AI-gestuurde beeldverwerkingspijplijn samen een schaalbare, minimaal invasieve maat kunnen leveren voor hoe sterk DNA-richtende middelen het lichaam beïnvloeden. Hoewel het werk in muizen is uitgevoerd en rode bloedcellen slechts een afspiegeling zijn van wat er in tumoren gebeurt, suggereert de sterke koppeling tussen micronucleus-signalen en tumorreductie dat deze aanpak een praktisch hulpmiddel kan worden in geneesmiddelenontwikkeling en uiteindelijk in klinische onderzoeken. Simpel gezegd: het tellen van deze microscopische DNA-"stipjes" in bloed kan onderzoekers en clinici helpen doses af te stemmen, nieuwe geneesmiddelen te vergelijken en behandelingseffecten in de tijd te volgen—zonder herhaalde, invasieve biopsieën.
Bronvermelding: Yong, K.H.R., Robak, W.S., Mulderrig, L. et al. Micronucleus quantification from whole-slide haematology images using AI serves as a translatable pharmacodynamic biomarker for DNA damage response inhibitors. Sci Rep 16, 11437 (2026). https://doi.org/10.1038/s41598-026-41458-7
Trefwoorden: micronuclei, rode bloedcellen, PARP-remmers, digitale pathologie, DNA-schade-respons