Clear Sky Science · nl
Potentieel gonadaal gunstig effect van sitagliptine tegen paclitaxel-geïnduceerde testiculaire disfunctie via modulatie van het PERK/CHOP/NLRP3/Sestrin2-signaleringspad
Waarom deze studie belangrijk is voor kankerpatiënten
Chemotherapie redt levens, maar kan onopgemerkt de vruchtbaarheid beschadigen, vooral bij mannen. Een veelgebruikt kankerremmend middel, paclitaxel, staat erom bekend de testes te schaden en de zaadkwaliteit te verminderen. Deze studie in ratten stelt een praktische vraag met duidelijke relevantie voor mensen: kan een al goedgekeurd diabetesmedicijn, sitagliptine, worden hergebruikt om het mannelijke voortplantingssysteem te beschermen tegen de bijwerkingen van paclitaxel zonder de antikankerwerking te belemmeren?
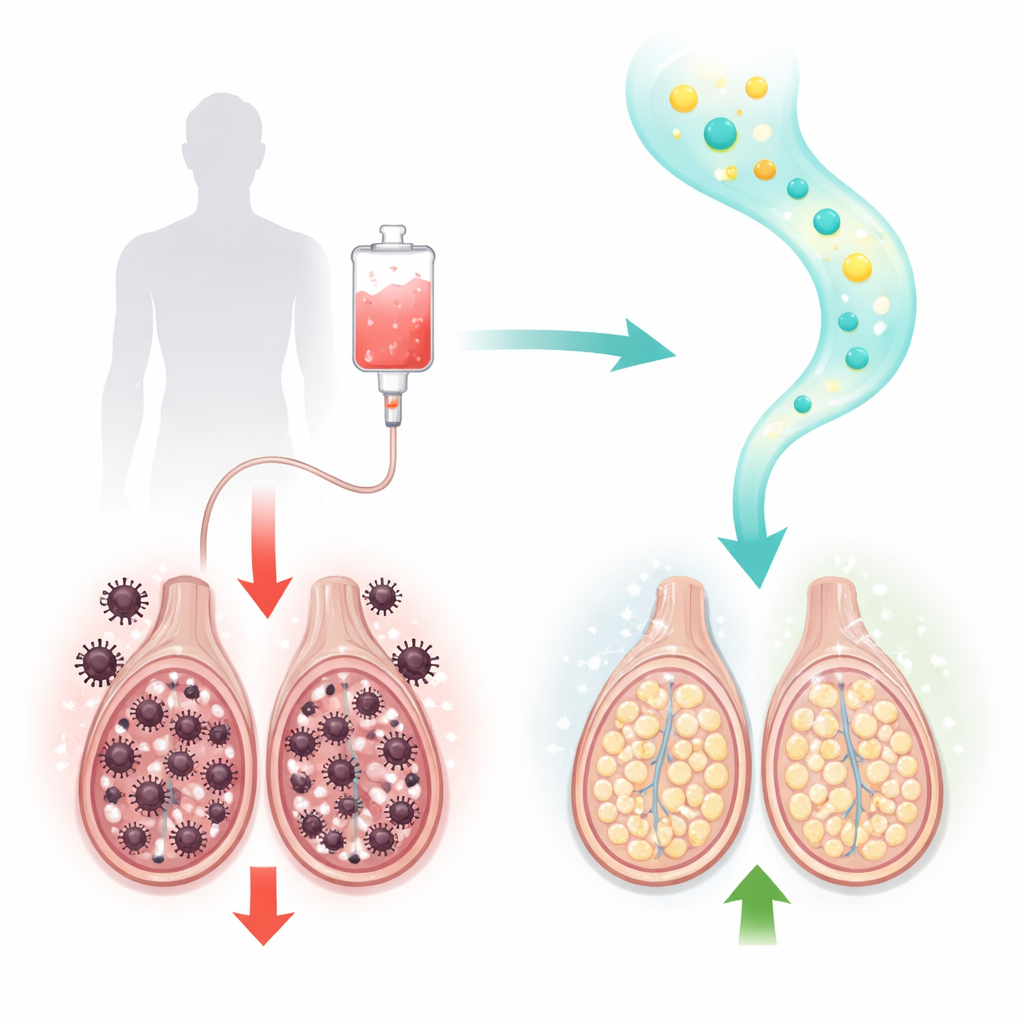
Een veelgebruikt kankermiddel met een verborgen prijs
Paclitaxel is een pijlerbehandeling voor borst-, eierstok-, long- en andere solide tumoren. Het werkt door het celdelingsmechanisme van snelgroeiende kankercellen te bevriezen. Helaas zijn ook delende cellen in gezonde organen kwetsbaar. Bij mannelijke ratten veroorzaakte behandeling met paclitaxel klassieke tekenen van testiculaire schade: zaadconcentraties, bewegelijkheid en levensvatbaarheid daalden sterk, terwijl misvormde zaadcellen toenamen. Onder de microscoop zagen de onderzoekers beschadigde seminiferous tubuli (waar zaadcellen worden gevormd) en beschadigde hormoonproducerende Leydig-cellen, samen met verschrompelde weefsellagen. Bloedonderzoek bevestigde dat testosteron en een sleutelenzym voor de aanmaak ervan, 17β-hydroxysteroiddehydrogenase, sterk verminderd waren.
Een diabetesmiddel als onverwachte beschermer
Sitagliptine wordt veel voorgeschreven om de bloedsuiker te reguleren bij mensen met type 2-diabetes. Eerder onderzoek suggereerde dat sitagliptine, naast zijn metabole effecten, schadelijke oxidatieve stress, ontsteking en celdood in organen zoals de lever, nier en hersenen kan verminderen. Voortbouwend op dit inzicht verdeelden de onderzoekers mannelijke ratten in vier groepen: onbehandelde controles, een paclitaxel‑alleengroep en twee groepen die paclitaxel ontvingen plus een lagere of hogere dosis sitagliptine gedurende twee weken. Daarna vergeleken ze zaadkwaliteit, hormoonspiegels, weefselstructuur en een reeks moleculaire “alarmsystemen” in de testes die stress signaleren en ontsteking en geprogrammeerde celdood activeren.
Hoe sitagliptine cellulaire stress en ontsteking temperde
Paclitaxel duwde de testes in een toestand van oxidatieve en interne stress: niveaus van schadelijke bijproducten (gemeten als malondialdehyde) stegen, terwijl natuurlijke verdedigingen zoals gereduceerd glutathion en het enzym catalase daalden. Diep binnenin de cellen schakelde het eiwitvouwwerk, het endoplasmatisch reticulum, een gevarenspoor in dat PERK–CHOP wordt genoemd — een signaal dat aanhoudende stress cellen richting celdood duwt. Tegelijkertijd werd een inflammatoir eiwitcomplex (NLRP3) sterk geactiveerd, wat ontstekingsboodschappers zoals interleukine‑1β deed toenemen en een cascade van celdoodseiwitten activeerde, waaronder cytochroom c en caspase‑3. Sitagliptine keerde veel van dit effect om. Beide dosissen verminderden oxidatieve schade en herstelden antioxiderende verdedigingen. Ze verlaagden opvallend de activatie van de PERK–CHOP-stressroute en dempten NLRP3‑gedreven ontsteking en apoptose. Een beschermend eiwit genaamd Sestrin2, dat helpt reactieve deeltjes op te ruimen en gekoppeld is aan gezondere zaadcellen, werd door sitagliptine zowel op gen- als op proteïneniveau verhoogd.
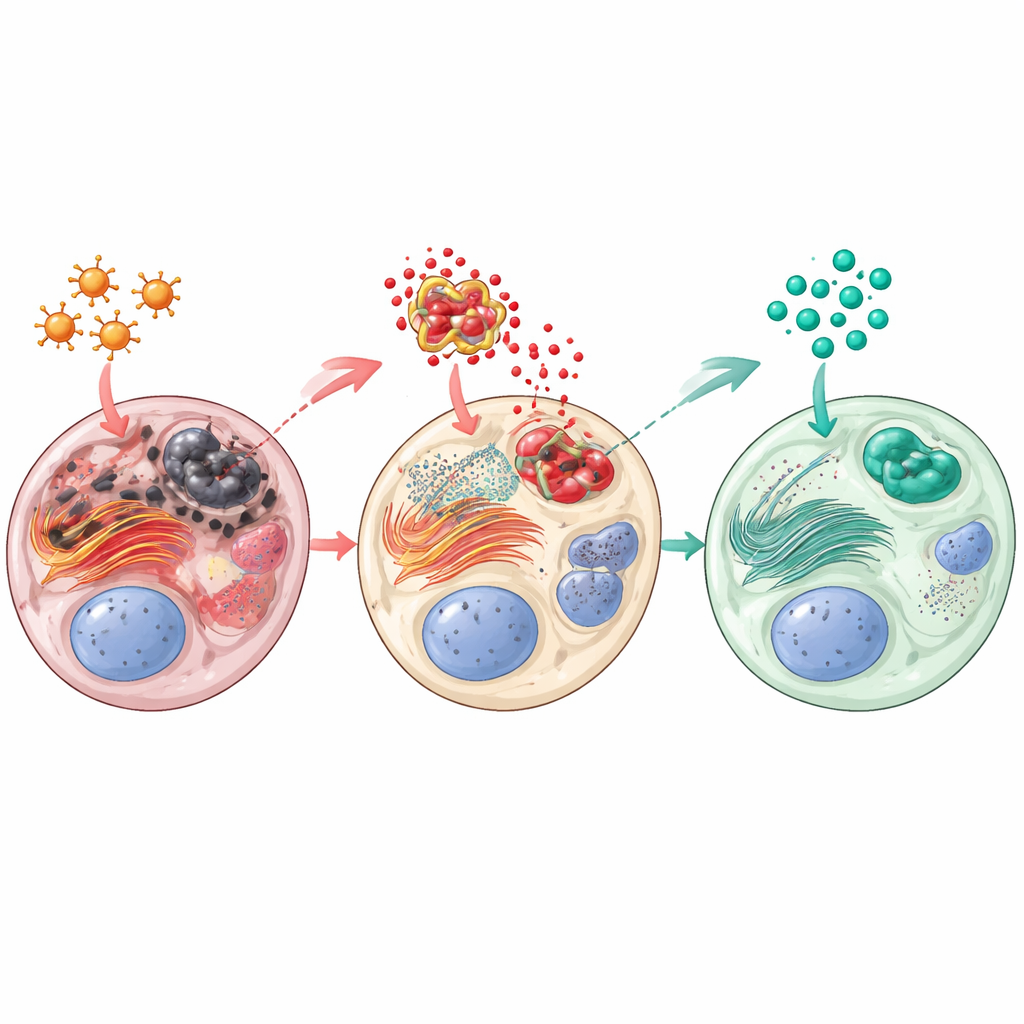
Betere zaadkwaliteit, gezonder weefsel, sterkere hormonen
De biochemische verbeteringen vertaalden zich naar tastbare functionele voordelen. Ratjes die na paclitaxel sitagliptine kregen, hadden hogere zaadconcentraties, betere bewegelijkheid en minder abnormale zaadcellen dan dieren die alleen paclitaxel kregen, waarbij de hogere sitagliptinedosis het dichtst bij normaal kwam. Testosteron en 17β‑hydroxysteroiddehydrogenase herstelden zich, wat suggereert dat de aanmaak van steroïdehormonen door Leydig-cellen aan het herstellen was. Zowel bij licht- als elektronenmicroscopie toonden sitagliptine‑behandelde testes meer ordelijke seminiferous tubuli, meer Leydig-cellen, dikkere en gezondere cellagen en minder structurele vervormingen. Over het geheel genomen hielp het middel de architectuur en functie die nodig zijn voor voortdurende zaadproductie te behouden.
Wat dit zou kunnen betekenen voor mannen die chemotherapie ondergaan
Dit dieronderzoek suggereert dat sitagliptine de door paclitaxel veroorzaakte schade aan de testes aanzienlijk kan verminderen door een netwerk van schadelijke signalen stil te leggen — oxidatieve stress, interne eiwitvouwhulp-stress, ontsteking en geprogrammeerde celdood — grotendeels via het verhogen van Sestrin2 en het terugschakelen van de PERK/CHOP/NLRP3-as. Omdat sitagliptine al klinisch wordt gebruikt bij diabetes, valt het op als een realistische kandidaat om te testen als vruchtbaarheidsbeschermende aanvullende behandeling bij mannen die paclitaxel krijgen, vooral bij degenen die ook diabetes hebben. De auteurs benadrukken dat menselijk onderzoek nog nodig is, maar hun bevindingen roepen een hoopvolle mogelijkheid op: een bekend pilletje zou op een dag kankerpatiënten kunnen helpen niet alleen hun leven, maar ook hun mogelijkheid om kinderen te verwekken, te behouden.
Bronvermelding: El-Beheiry, K.M., El-Shitany, N.A., El-Sayad, M.ES. et al. Potential gonadal-beneficial effect of sitagliptin against paclitaxel-induced testicular dysfunction via mediating PERK/CHOP/NLRP3/Sestrin2 signaling pathway. Sci Rep 16, 9090 (2026). https://doi.org/10.1038/s41598-026-40511-9
Trefwoorden: paclitaxel, sitagliptine, mannelijke vruchtbaarheid, oxiderende stress, testiculaire toxiciteit