Clear Sky Science · nl
Een verkennende in vitro co-cultuur van enterische neuronen en gladde spiercellen toont de neuronale bijdrage aan de vorming van de spierlaag
Waarom het kweken van nieuwe darmspier belangrijk is
Voor mensen die vanaf de geboorte grote delen van hun dunne darm missen, of die deze verliezen, kan het dagelijks leven afhangen van intraveneuze voeding omdat hun resterende darm niet genoeg voedingsstoffen kan opnemen. Transplantaties zijn riskant en falen vaak na verloop van tijd. Deze studie onderzoekt een heel ander idee: kunnen wetenschappers in het laboratorium werkende stukjes darmspier laten groeien, compleet met een ingebouwde "darmhersen" om beweging te coördineren? Als dat lukt, zou het op den duur kunnen helpen bij het maken van vervangend darmsweefsel voor patiënten met het kort-darmsyndroom.
De verborgen hersenen in de darm
De wand van de darm is meer dan een eenvoudige buis. Ze bevat lagen gladde spier die voedsel ritmisch voortduwen, aangestuurd door een dicht netwerk van zenuwen dat het enterische zenuwstelsel wordt genoemd, soms de "hersenen in de darm". Wanneer deze zenuwen ontbreken of beschadigd zijn, zoals bij de ziekte van Hirschsprung of na grote operaties, kan de spierlaag het voedsel niet correct verplaatsen. De auteurs redeneerden dat elk in het laboratorium gemaakt vervangend weefsel daarom zowel spiercellen als enterische zenuwcellen moet bevatten, niet slechts een van beide, en zetten een vereenvoudigd model op dat alleen deze twee sleutelspelers omvatte.
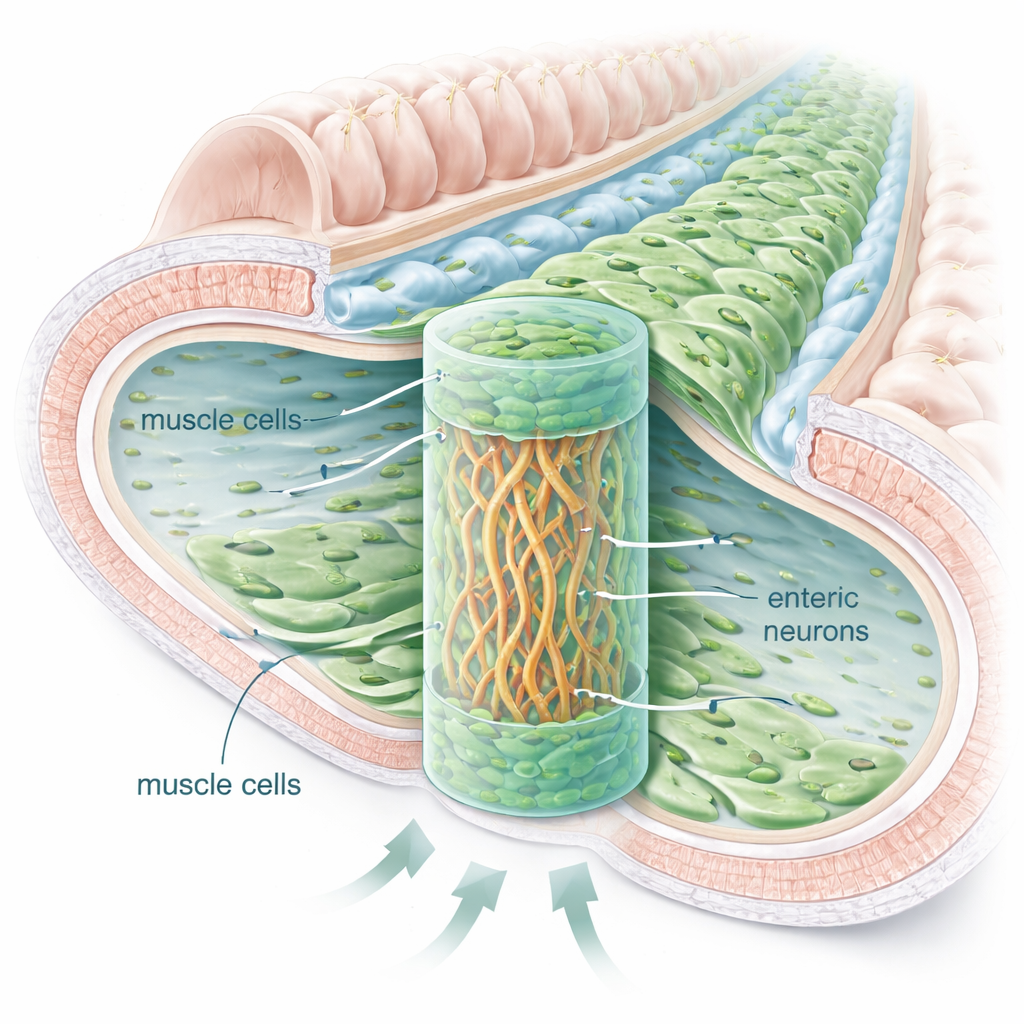
Een mini-darmwand bouwen in een gel
Het team isoleerde enterische zenuwcellen uit jonge ratten en combineerde deze met commercieel geproduceerde intestinale gladde spiercellen in een zachte, gelachtige matrix gemaakt van hyaluronzuur. Ze testten verschillende vloeibare voedingsmixen totdat ze er een vonden die beide celtypen ondersteunde, en experimenteerden vervolgens met de driedimensionale plaatsing van de cellen. De meest succesvolle opstelling leek op een sandwich: een dicht pakket zenuwcellen in de middellaag van de gel, boven en onder omgeven door gladde spiercellen. In deze opzet overleefden beide celtypen weken tot maanden en vormden ze gelaagde structuren die deden denken aan de natuurlijke darmwand.
Van willekeurige cellen naar georganiseerde, bewegende vezels
Microscopie toonde aan dat de aanwezigheid van enterische zenuwcellen het gedrag van de spiercellen drastisch veranderde. Alleen in de gel bleven gladde spiercellen bolvormig, drukten ze hun contractiele eiwitten zwak uit en slaagden ze er niet in zich uit te lijnen tot vezels. Wanneer zenuwcellen in de buurt waren of direct contact hadden, werden de spiercellen langer, lijnden ze zich uit en vormden ze lange bundels vergelijkbaar met native spierlagen. De onderzoekers zagen netwerken van zenuwvezels die zich tussen de spierbundels weefden, samen met glia-cellen die normaal neuronen ondersteunen. Met fluorescentiemarkers en elektronenmicroscopie identificeerden ze structuren die leken op synapsen — kleine contactpunten waar zenuwen met spiercellen communiceren.
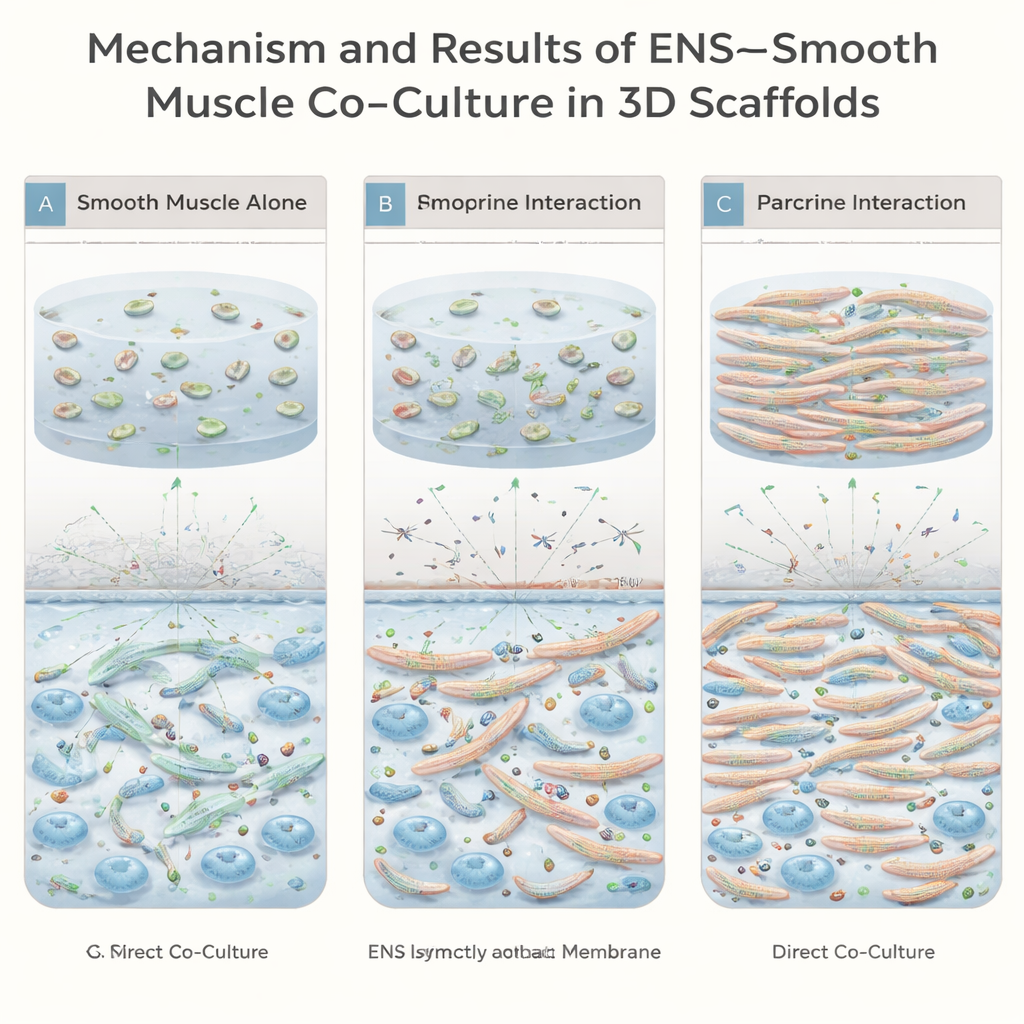
Trekt deze in het lab gekweekte vezels zich daadwerkelijk samen?
Vanaf ongeveer drie weken in cultuur begonnen de constructen die zowel spier- als enterische zenuwcellen bevatten spontane contracties te vertonen die zichtbaar waren onder een lichtmicroscoop. Dunne en dikke spierbundels trokken herhaaldelijk samen en ontspanden, wat suggereert dat het vervaardigde weefsel actief kon bewegen in plaats van alleen passief in de gel te liggen. Directe co-cultuur, waarbij zenuw- en spiercellen elkaar aanraken binnen dezelfde matrix, leverde de meest robuuste, goed uitgelijnde vezels en de rijkste zenuwnetwerken op. Ter vergelijking: wanneer de twee celtypen gescheiden waren door een membraan dat slechts oplosbare signalen doorgaf, vormden spiervezels zich wel, maar waren ze minder talrijk, zwakker en minder georganiseerd.
Wat dit betekent voor toekomstige darmreparatie
Dit werk bewijst nog niet dat de contracties volledig door de zenuwcellen worden gecontroleerd, en het reproduceert ook nog niet de volledige darmwand met slijmvlies en immuuncellen. Toch levert het een duidelijk proof-of-concept: enterische zenuwcellen kunnen gladde spiercellen helpen organiseren tot uitgelijnde, geïnnerveerde bundels die zich meer als levende darmspier gedragen. Voor patiënten met het kort-darmsyndroom zijn zulke vereenvoudigde maar functionele spierlagen een cruciale stap richting het bouwen van vervangende darmlenzen. Toekomstige studies die deze neuromusculaire constructen combineren met het darmslijmvlies en meer gedetailleerde tests van zenuwgestuurde bewegingen uitvoeren, kunnen de weefseltechnische darm dichter bij klinische toepasbaarheid brengen.
Bronvermelding: Khasanov, R., Tapia-Laliena, M.Á., Schulte, S. et al. An exploratory in vitro co-culture of enteric neurons and smooth muscle cells demonstrates neuronal contribution to muscle layer formation. Sci Rep 16, 7732 (2026). https://doi.org/10.1038/s41598-026-39409-3
Trefwoorden: kort-darmsyndroom, intestinale weefseltechniek, enterisch zenuwstelsel, gladde spier, 3D co-cultuur