Clear Sky Science · nl
Ontregeling van neutrofielhomeostase geassocieerd met functionele veranderingen in mitochondriën van kritiek zieke COVID-19-patiënten
Waarom dit belangrijk is voor COVID-19-patiënten
De meeste mensen weten inmiddels dat COVID-19 meer is dan alleen een longinfectie, maar hoe het virus precies het eigen afweersysteem tegen het lichaam keert, wordt nog ontrafeld. Deze studie bekijkt neutrofielen, een veelvoorkomende soort witte bloedcel, bij patiënten met levensbedreigende COVID-19 op de intensive care. Door te onderzoeken hoe deze cellen leven, sterven en hun interne "energiecentrales" (mitochondriën) gebruiken, onthullen de onderzoekers een patroon van hardnekkige, overactieve neutrofielen dat kan helpen de aanhoudende ontsteking, bloedschade en orgaanschade bij ernstige ziekte te verklaren.
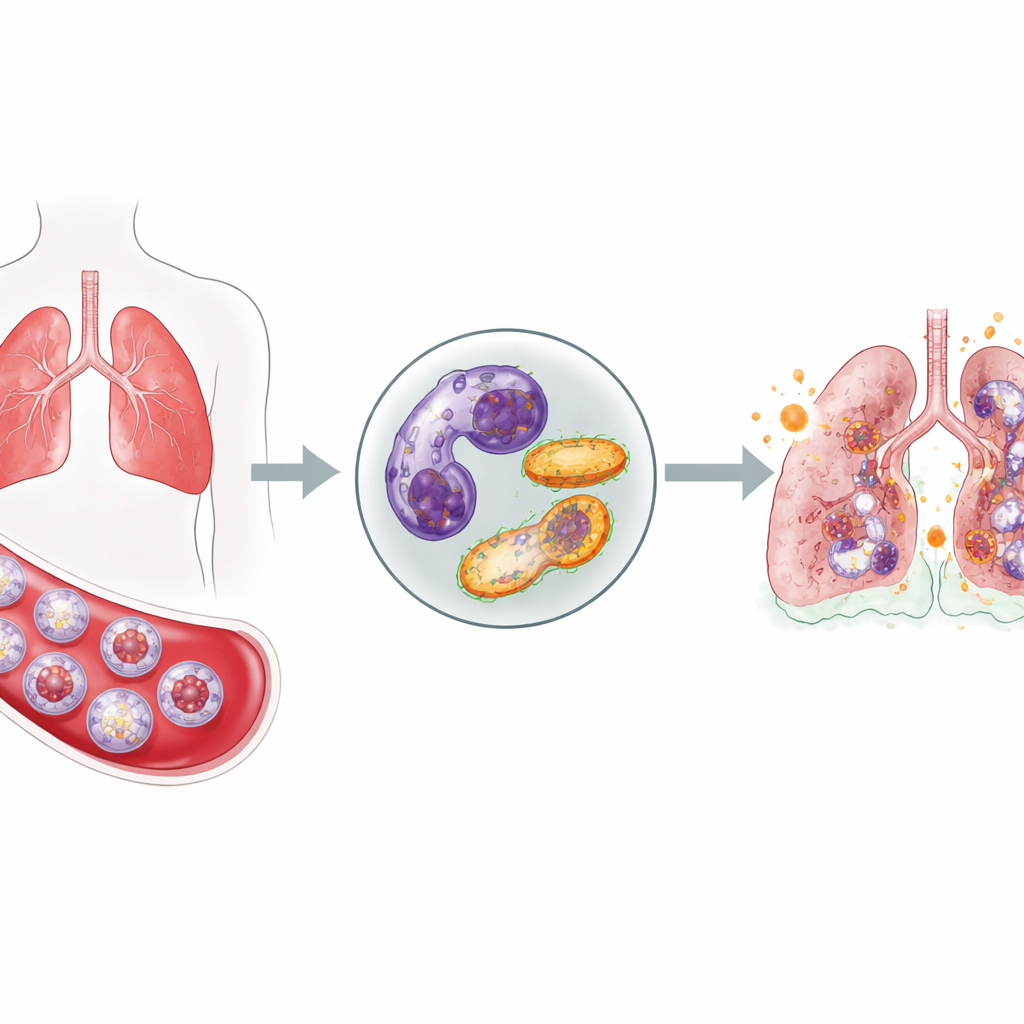
Frontlijncellen die niet achterover gaan leunen
Neutrofielen zijn een van de eerste verdedigers van het lichaam tegen infectie: ze stromen in het bloed, bewegen zich naar weefsels en geven giftige moleculen af om binnendringende microben te doden. Gewoonlijk, nadat ze hun werk hebben gedaan, gaan ze stilletjes zelften en worden ze opgeruimd, wat voorkomt dat ze gezond weefsel beschadigen. Bij kritiek zieke COVID-19-patiënten vond het team een heel ander beeld. In vergelijking met gezonde vrijwilligers hadden deze patiënten een sterke toename van neutrofielen in hun bloed en, belangrijker, veel daarvan waren onrijpe cellen die voortijdig uit het beenmerg waren vrijgegeven. Tegelijkertijd lieten meerdere tests zien dat minder neutrofielen hun normale geprogrammeerde celdood ondergingen, wat suggereert dat deze agressieve cellen langer blijven dan ze zouden moeten.
Subtiele genetische signalen maar een duidelijk overlevingspatroon
De onderzoekers onderzochten ook kleine regelmoleculen genaamd microRNA's in neutrofielen van overlevers en niet-overlevers op de intensive care. Sommige van deze moleculen waren veranderd op manieren die, op papier, wijzen op verstoorde routes die celdood en calciumbalans reguleren. Toen ze echter directe merkers van celdood maten, zagen ze geen grote verschillen tussen overlevers en niet-overlevers—beide groepen vertoonden vergelijkbaar gereduceerde neutrofielzelfdoding vergeleken met gezonde mensen. Dit betekent dat de microRNA-patronen meer aanzetten tot toekomstig onderzoek zijn dan harde aanwijzingen wie zal overleven, en ze benadrukken dat het algemene falen van neutrofielen om uit te schakelen een gedeelde eigenschap is van ernstige COVID-19.
Calciumverschuivingen en te geladen energiecentrales
Om te begrijpen waarom neutrofielen niet op schema stierven, richtte het team zich op twee nauw verbonden systemen binnen de cellen: calciumsignalen en mitochondriën. Calciumionen fungeren als kleine aan/uit-schakelaars voor veel celbeslissingen, waaronder wanneer tezelfdertijd te treden. De onderzoekers vonden dat neutrofielen van patiënten met ernstige COVID-19 minder vrij calcium binnenin hadden, samen met verlaagde niveaus van sleutelproteïnen die normaal calcium naar mitochondriën helpen transporteren en een veiligheidsklep openen die celdood kan triggeren. Tegelijkertijd waren de mitochondriën zelf abnormaal "opgeladen", met een hogere elektrische gradient over hun membranen en verhoogd zuurstofverbruik, vooral via één belangrijk respiratoir pad. In plaats van uit te schakelen produceerden deze overactieve mitochondriën meer reactieve zuurstofmoleculen, die omliggend weefsel kunnen beschadigen en ontsteking kunnen aanwakkeren.
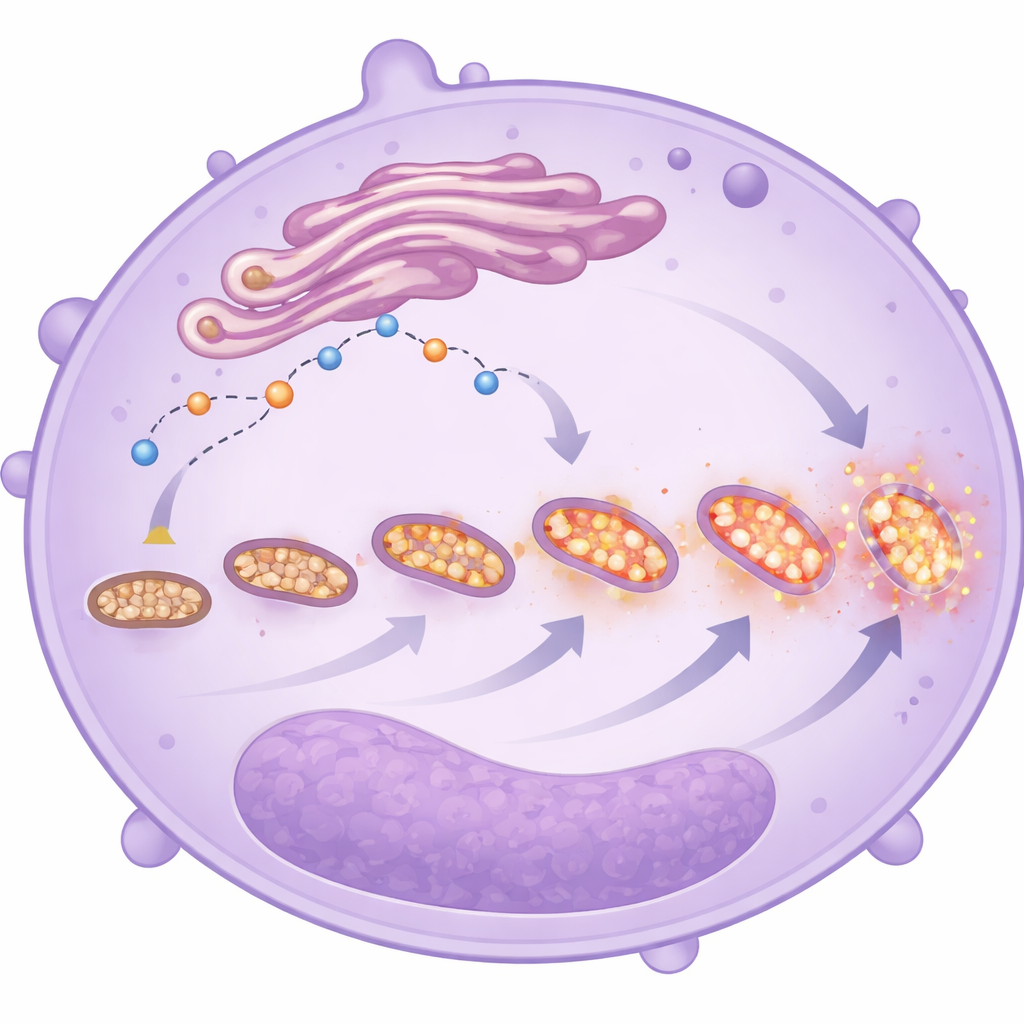
Gestreste en gefragmenteerde mitochondriën
Elektronenmicroscoopbeelden en fluorescerende kleurstoffen gaven een nadere blik op de vorm en het gedrag van deze mitochondriën. In neutrofielen van de ernstigste patiënten waren de mitochondriën talrijker maar kleiner en meer gefragmenteerd—kenmerken die vaak stress signaleren. Deze cellen vertoonden ook hogere niveaus van mitochondriale reactieve zuurstofsoorten, ongeacht of de patiënt uiteindelijk overleefde. Samen met de veranderde calciumhuishouding en vertraagde celdood schetsen deze veranderingen het beeld van neutrofielen die hun energiestrategie hebben verschoven: in plaats van hoofdzakelijk op eenvoudige suikerafbraak te vertrouwen, leunen ze meer op mitochondriale stofwisseling, vooral in onrijpe cellen. Deze omschakeling kan hun vermogen om te migreren, te blijven bestaan en schadelijke moleculen vrij te geven in de longen en andere organen versterken, ook al kan de studie niet bewijzen dat ze direct de oorzaak zijn van slechtere uitkomsten.
Wat dit kan betekenen voor toekomstige zorg
In eenvoudige bewoordingen suggereert de studie dat neutrofielen bij kritieke COVID-19 te talrijk, te jong en te moeilijk uit te schakelen worden. Hun interne calciumsignalen en mitochondriën zijn hersnoerd op een manier die ze in leven en zeer actief houdt, waarbij ze pulsen van schadelijke zuurstofgebaseerde chemicaliën produceren. Hoewel het onderzoek observationeel is en geen oorzaak en gevolg aantoont, wijst het op verschillende potentiële "regelknoppen" in deze cellen—zoals calciumregulatoren en mitochondriale controlespunten—die op den duur wellicht kunnen worden gericht om neutrofielen voorzichtig terug naar normaal gedrag te sturen. Als toekomstig onderzoek deze ideeën bevestigt, zouden behandelingen die juiste neutrofieluitschakeling herstellen of hun overbeladen mitochondriën kalmeren kunnen helpen de collaterale schade te verminderen die deze cruciale cellen veroorzaken tijdens ernstige COVID-19 en mogelijk bij andere kritieke ziekten.
Bronvermelding: Elkhodiry, A.A., Yasseen, B.A., El-sayed, H. et al. Disruption of neutrophil homeostasis is associated with functional alterations in mitochondria of critically ill COVID−19 patients. Sci Rep 16, 7838 (2026). https://doi.org/10.1038/s41598-026-38741-y
Trefwoorden: COVID-19, neutrofielen, mitochondriën, ontsteking, kritieke ziekte