Clear Sky Science · nl
Katalytische asymmetrische functionalisatie van bicyclo[1.1.0]butaan boronzuuresters mogelijk gemaakt door 1,2-zuurstofmigratie
Waarom kleine vierkante ringen ertoe doen
Schemici bouwen graag nieuwe geneesmiddelen en materialen door kleine moleculaire blokjes aan elkaar te klikken, vergelijkbaar met het bouwen met Lego. Vierledige koolstofringen, cyclobutanen genoemd, worden bijzonder gewaardeerd omdat ze veel energie en ruimtelijke vorm in een kleine structuur samenpersen, wat het gedrag van een geneesmiddel in het lichaam kan beïnvloeden. Dit artikel beschrijft een nieuwe manier om deze ringen zeer gecontroleerd in één handigheid (chiraal) te maken, gebruikmakend van een slimme reactie die een zuurstofhoudende groep dwingt om van het ene atoom naar het andere te springen. Het werk opent mogelijkheden voor het ontwerpen van complexere en preciezere moleculen voor de farmacie en geavanceerde materialen.
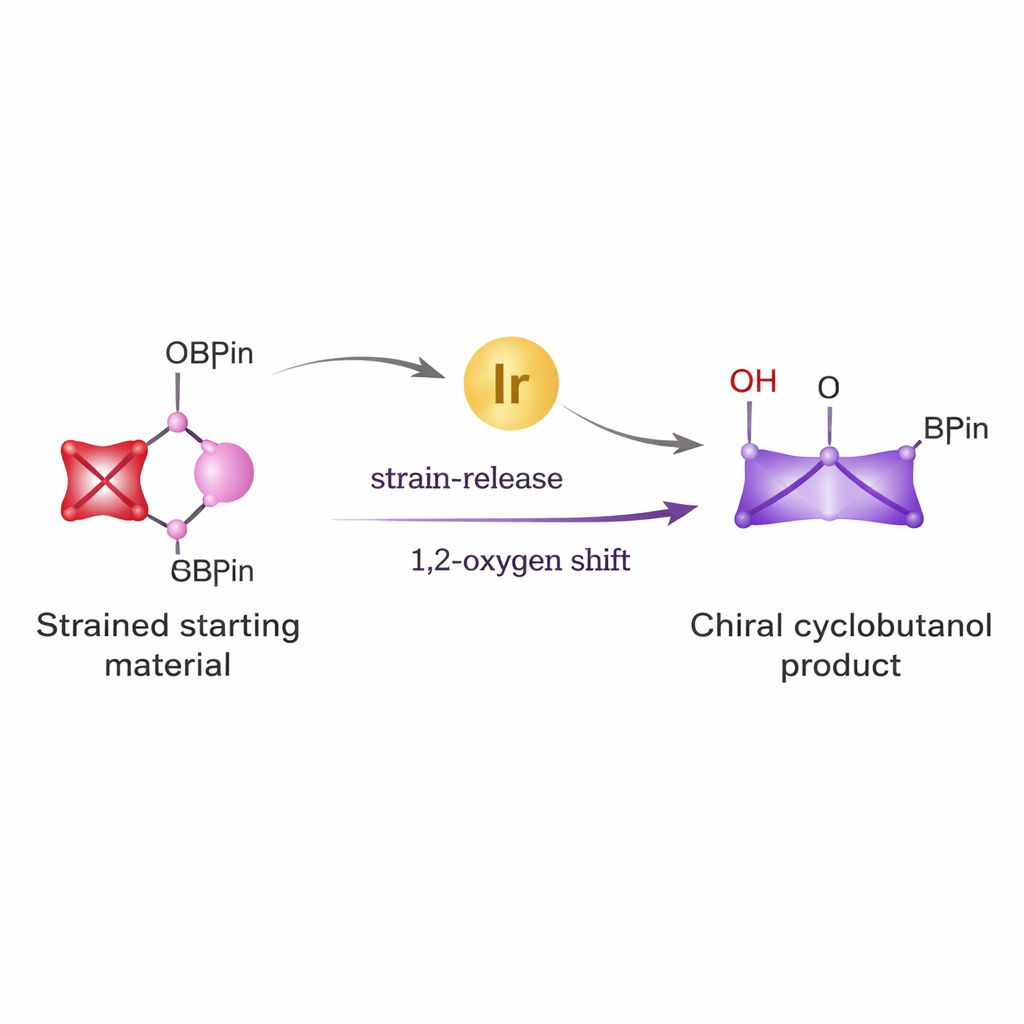
Van eenvoudige bouwstenen naar krachtige ringen
Cyclobutanen komen voor in diverse antivirale middelen, kandidaat-geneesmiddelen tegen kanker en andere bioactieve moleculen. Ze met de precies juiste driedimensionale ordening bouwen voor medicinale toepassingen is echter lastig geweest. Traditionele routes vereisen vaak agressieve reagentia en geven mengsels van spiegelbeeldproducten die moeilijk te scheiden zijn. De auteurs wilden dit probleem oplossen door twee krachtige ideeën te combineren: de ongebruikelijke reactiviteit van een klein, sterk gespannen ringetje genaamd bicyclo[1.1.0]butaan, en de veelzijdigheid van boronzuuresters, een bekende reagentiafamilie die veel wordt gebruikt in cross-couplingchemie om koolstof–koolstofbindingen te vormen.
Een nadeel omzetten in een nieuw reactiepád
In standaard metaalgekatalyseerde koppelingen vormen boronzuuresters een intermediair complex met een alkoxide (een zuurstofgebaseerde base). Dit complex volgt vrijwel altijd een bekend pad dat transmetallatie wordt genoemd, wat vervolgens direct leidt tot nieuwe koolstof–koolstof- of koolstof–halogeenbindingen. Dat "standaard" pad maakte het moeilijk om andere mogelijkheden te verkennen, zoals het verschuiven van de zuurstofgroep zelf. Het team realiseerde zich dat als ze startten vanuit een ring-gespannen bicyclo[1.1.0]butaan boronzuurester, de ingebouwde spanning van de kleine ring gebruikt kon worden om het gebruikelijke proces te overrulen. Door dit gespannen systeem te combineren met een iridiumkatalysator en een zorgvuldig gekozen chirale ligand, hoopten ze de zuurstof gecontroleerd te laten migreren terwijl de ring opende en opnieuw sloot tot een cyclobutaan.
Een stapsgewijze dans gestuurd door spanning
Experimenten bevestigden dat deze strategie werkt. Met behulp van lithiumalkoxiden gemaakt uit een breed scala aan alcoholen — waaronder suikers, terpenen, steroïden en eenvoudige alifatische alcoholen — zetten de auteurs bicyclo[1.1.0]butaan boronzuuresters om in cis-cyclobutanolen met zowel hoge opbrengst als uitstekende controle over chiraliteit. De iridiumkatalysator vormt eerst een reactief allylcomplex uit een allylcarbonaatpartner. Dit complex valt vervolgens het gespannen bicyclo[1.1.0]butaan-systeem aan en vormt een nieuwe koolstof–koolstofbinding terwijl de kleine ring opent. Belangrijk is dat het resulterende boronhoudende intermediair, in plaats van direct de gebruikelijke transmetallatieroute te volgen, een subtiele rotatie van de koolstof–boorbinding ondergaat, waardoor de gebonden zuurstofgroep zo gepositioneerd wordt dat deze schoon kan verschuiven naar een aangrenzend koolstofatoom. Deze 1,2-zuurstofmigratie vergrendelt de gewenste cis-arrangering op de nieuwe cyclobutaanring.
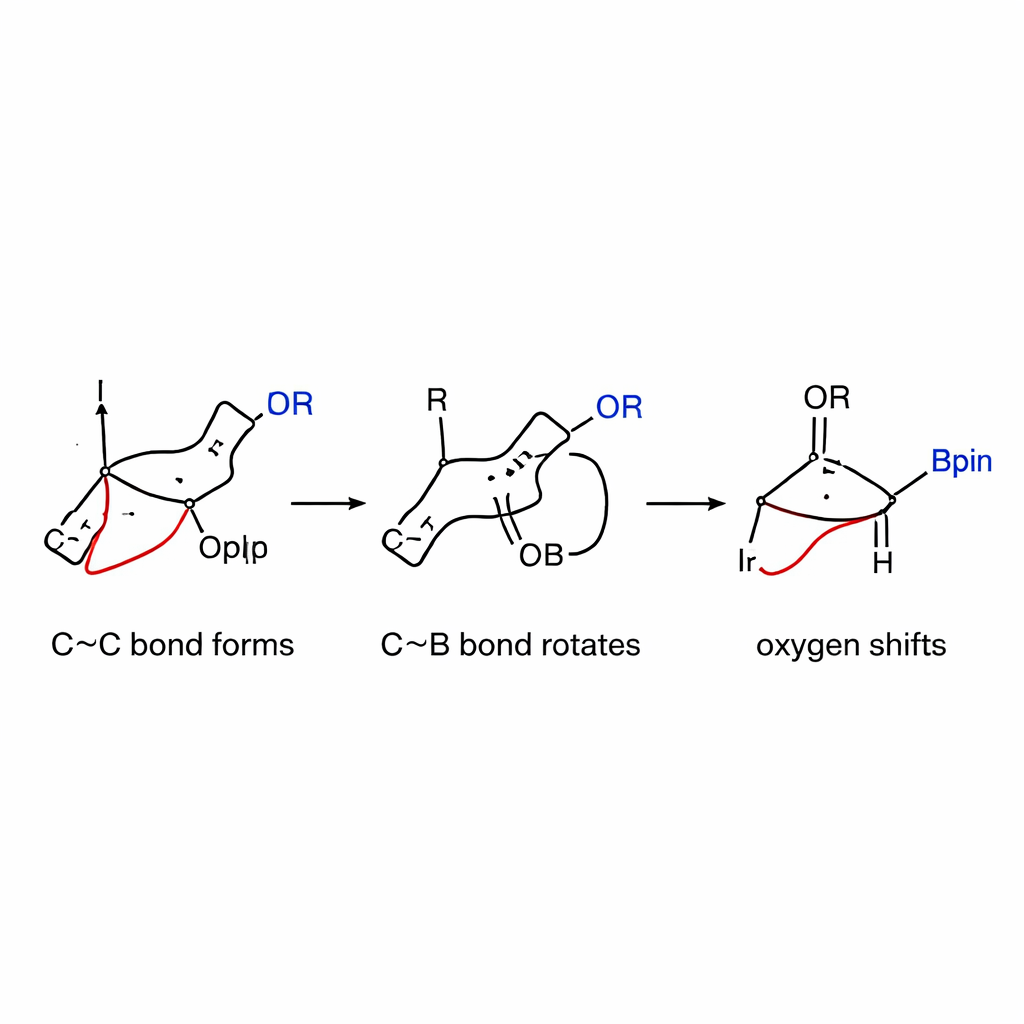
Onder de motorkap van het mechanisme kijken
Om te begrijpen waarom de reactie zo selectief is, combineerden de auteurs kinetische metingen met gedetailleerde computersimulaties. Ze vonden dat de trage, snelheidsbepalende stap de initiële koolstof–koolstofbindingsvorming is tussen de iridium–allylsoort en het gespannen boronaatcomplex, niet de eerdere activatie van het allylcarbonaat. Elektronische tests toonden aan dat allylpartners die positieve lading stabiliseren sneller reageren, wat een mechanisme ondersteunt waarin een gedeeltelijk geladen intermediair wordt gevormd. Berekeningen toonden verder aan dat rotatie rond de koolstof–boorbinding — eerder gedacht moeilijk te zijn — in dit systeem een verrassend lage energiedrempel heeft, dankzij de opgeslagen ringspanning. Zodra rotatie de zuurstofgroep uitlijnt, verloopt de 1,2-verschuiving soepel en geeft bij voorkeur het cis-product in plaats van de gebruikelijkere trans-vorm.
Nieuwe hulpmiddelen voor het vormgeven van toekomstige geneesmiddelen
Buiten het aantonen van een mechanistisch punt levert de reactie veelzijdige producten op. De cyclobutanolen behouden een boronzuurester-eenheid, die kan worden omgezet in veel andere functionele groepen met gevestigde chemie. De auteurs toonden tal van late-stage modificaties, zoals hydrogenatie, oxidatie, olefine-metathese en verdere koppelingen, terwijl de precieze driedimensionale vorm van de ring behouden bleef. Eenvoudig gezegd verandert dit werk een ooit problematisch nevenpad — zuurstofmigratie in boronaatcomplexen — in een krachtig synthetisch hulpmiddel. Door ringspanning en een fijn afgestemde iridiumkatalysator te benutten, bieden de onderzoekers scheikundigen een betrouwbare manier om complexe, chirale cyclobutanen te bouwen die sleutelrollen zouden kunnen spelen in de volgende generatie geneesmiddelen en geavanceerde moleculaire materialen.
Bronvermelding: Zhu, XY., Ji, CL., Dong, TG. et al. Catalytic asymmetric functionalization of bicyclo[1.1.0]butane boronic esters enabled by 1,2-oxygen migration. Nat Commun 17, 1941 (2026). https://doi.org/10.1038/s41467-026-69860-9
Trefwoorden: cyclobutaan, organoboorchemie, asymmetrische katalyse, bicyclobutaan, zuurstofmigratie