Clear Sky Science · nl
CD19+ tumorgeassocieerde macrofagen veroorzaken een immunosuppressieve micro-omgeving bij hepatocellulair carcinoom
Waarom het afweersysteem soms de leverkanker helpt
Leverkanker behoort tot de dodelijkste vormen van kanker wereldwijd, deels omdat tumoren het eigen immuunsysteem tegen het lichaam kunnen keren. Deze studie onthult een verrassende subgroep immuuncellen in levertumoren die, in plaats van kanker te bestrijden, actief helpt bij het verbergen en laten groeien van de tumor. Inzicht in wie deze ‘verraders’ zijn en hoe ze werken, opent nieuwe wegen om immunotherapie effectiever te maken voor mensen met hepatocellulair carcinoom, de meest voorkomende vorm van leverkanker.
Een bijzondere groep immuuncellen in tumoren
De auteurs richtten zich op tumorgeassocieerde macrofagen, immuuncellen die normaal gesproken ziekteverwekkers en celresten opruimen maar die binnen tumoren vaak gecorrumpeerd raken. Door levertumor-monsters van veel patiënten te analyseren, ontdekten ze een onderscheidende subgroep macrofagen die een oppervlaktemolecuul dragen dat CD19 heet—meestal aangetroffen op B-cellen en niet op macrofagen. Deze CD19-positieve macrofagen kwamen veel vaker voor in levertumoren dan in nabijgelegen gezond leverweefsel of bloed, en waren ook verrijkt in meerdere andere solide tumoren. Enkelcelanalyses bevestigden dat het echte macrofagen zijn met een uniek gen‑ en eiwitprofiel, en geen verkeerd geïdentificeerde B-cellen.
Hoe deze cellen een tumorvriendelijke omgeving vormen
Patiënten wier tumoren veel CD19-positieve macrofagen bevatten, hadden doorgaans grotere, agressievere tumoren en een kortere overleving. Tumormonsters met veel van deze cellen toonden minder kanker-dodende CD8-T-cellen en meer regulerende T‑cellen, een patroon dat kenmerkend is voor een sterk immunosuppressieve omgeving. In muismodellen leidde het toevoegen van CD19-positieve macrofagen aan leverkankercellen tot snellere tumorvorming en minder nuttige T-cellen, terwijl andere onderdrukkende myeloïde cellen toenamen. Belangrijk was dat, wanneer de onderzoekers geengineerde T‑cellen gebruikten die CD19 herkennen om deze macrofagen selectief te verwijderen, levertumoren krompen zelfs in muizen zonder normale B‑cellen, waarmee werd aangetoond dat de macrofagen zelf therapeutische doelen zijn.
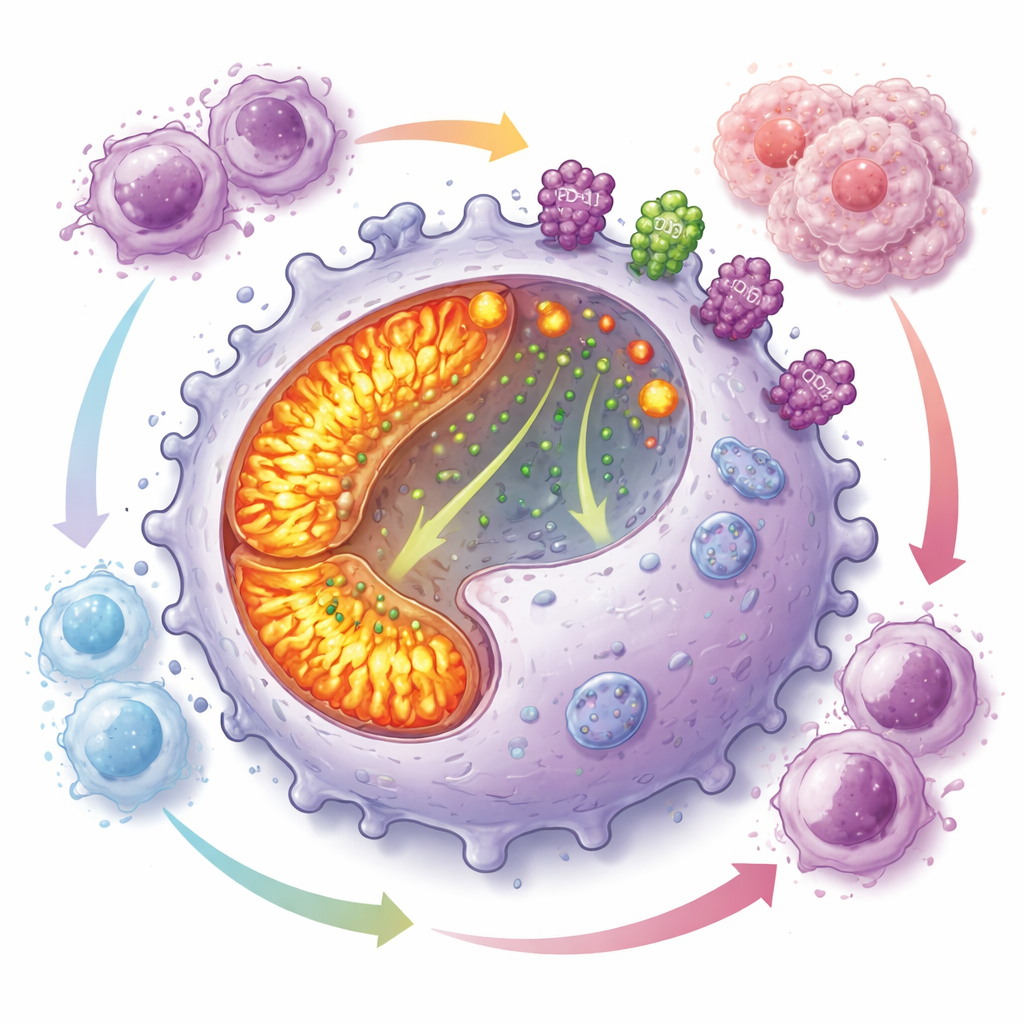
Een energiehongerig programma dat de immuunaanval dempt
Dieper onderzoek toonde aan dat CD19-positieve macrofagen hun interne ‘energiecentrales’ op volle toeren laten draaien. Hun mitochondriën—de organellen die energie produceren—waren talrijker en actiever dan in andere macrofagen, met toegenomen oxidatieve fosforylering en reactieve zuurstofsoorten. Ondanks deze energierijke staat hadden deze cellen een slechte capaciteit om doelen te fagocyteren maar deelden ze zich snel, wat hun ophoping in tumoren bevordert. Tegelijkertijd vertoonden ze hoge niveaus van PD-L1 en CD73 aan het celoppervlak—twee moleculen die bekendstaan om het uitschakelen van T‑celreacties en het genereren van adenosine, een klein molecuul dat de immuniteit sterk dempt. Co‑kweekexperimenten toonden dat deze macrofagen de groei van meerdere T‑celtypen sterk remmen.
De hoofdschakel achter de verraderlijke macrofagen
De onderzoekers identificeerden een transcriptiefactor genaamd PAX5 als de centrale motor van dit schadelijke macrofaagprogramma. PAX5 is vooral bekend als begeleider van B‑celontwikkeling, maar hier was het sterk actief in CD19-positieve macrofagen. Het forceren van macrophage-achtige cellen om PAX5 te expressen verhoogde mitochondriale biogenese, verhoogde energieproductie en deed de eiwit—maar niet mRNA—niveaus van PD-L1, CD73 en CD19 stijgen. Mechanistische experimenten toonden dat PAX5 calcium in mitochondriën trekt, waardoor calcium in het cytosol daalt en een sleutelregulator genaamd TFEB wordt verhinderd de kern binnen te gaan. Met TFEB tegengehouden daalt de productie en functie van lysosomen, waardoor eiwitten zoals PD-L1 en CD73 niet efficiënt worden afgebroken en juist ophopen aan het celoppervlak, wat de immuunsuppressie versterkt.
Van ontdekking naar betere behandelingsopties
Aangezien deze macrofagen sterk afhankelijk zijn van CD73‑activiteit en mitochondriale stofwisseling, onderzochten de auteurs of het blokkeren van deze routes immunotherapie effectiever kan maken. In muismodellen van leverkanker leidde het combineren van PD‑L1-blokkade met óf CD73‑antistoffen óf een CD73‑remmer tot kleinere tumoren, meer infiltrerende T‑cellen en minder celdeling van kankercellen. Evenzo verbeterde het koppelen van PD‑L1‑antistoffen aan een remmer van mitochondriale oxidatieve fosforylering tumorgroei controle en bevorderde de instroom van immuuncellen in tumoren. Opvallend was dat deze voordelen verdwenen in muizen waarvan de macrofagen PAX5 misten, wat bevestigt dat de geneesmiddeleffecten gekoppeld waren aan het uitschakelen van het CD19-positieve, PAX5‑gedreven macrofaagprogramma. Gezamenlijk suggereren de resultaten dat selectief richten op deze macrofaagsubset—via CD19‑gerichte celtherapieën, CD73‑inhibitie of metabole geneesmiddelen—kan helpen een immunologisch ‘koude’ levertumor om te zetten in een tumor die veel beter reageert op bestaande checkpoint‑blokkerende behandelingen.
Bronvermelding: Wang, J., Cao, W., Huang, J. et al. Tumor-associated CD19+ macrophages induce immunosuppressive microenvironment in hepatocellular carcinoma. Nat Commun 17, 3250 (2026). https://doi.org/10.1038/s41467-026-69638-z
Trefwoorden: hepatocellulair carcinoom, tumorgeassocieerde macrofagen, immunotherapie, PD-L1 en CD73, mitochondriale stofwisseling