Clear Sky Science · nl
Tumor-specifieke HORMAD1-expressie verstoort mitotische arrestatie en vergroot gevoeligheid voor mitotische kinaseremmers
Waarom dit belangrijk is voor kankerbehandeling
Wanneer onze cellen zich delen vertrouwen ze op verfijnde veiligheidscontroles om het juiste aantal chromosomen door te geven. Kanker kapert of verzwakt deze waarborgen vaak, wat leidt tot chaotische genomen die zowel de ziekte aandrijven als bepalen hoe tumoren op medicijnen reageren. Deze studie onthult hoe een ongebruikelijk eiwit, HORMAD1, dat normaal alleen actief is in voortplantingscellen, in veel agressieve borst- en andere tumoren wordt aangezet. Door subtiel een belangrijke controle tijdens de celdeling te saboteren, maakt HORMAD1 kankercellen instabieler — maar ook ongewone kwetsbaar voor een nieuwe klasse experimentele geneesmiddelen.
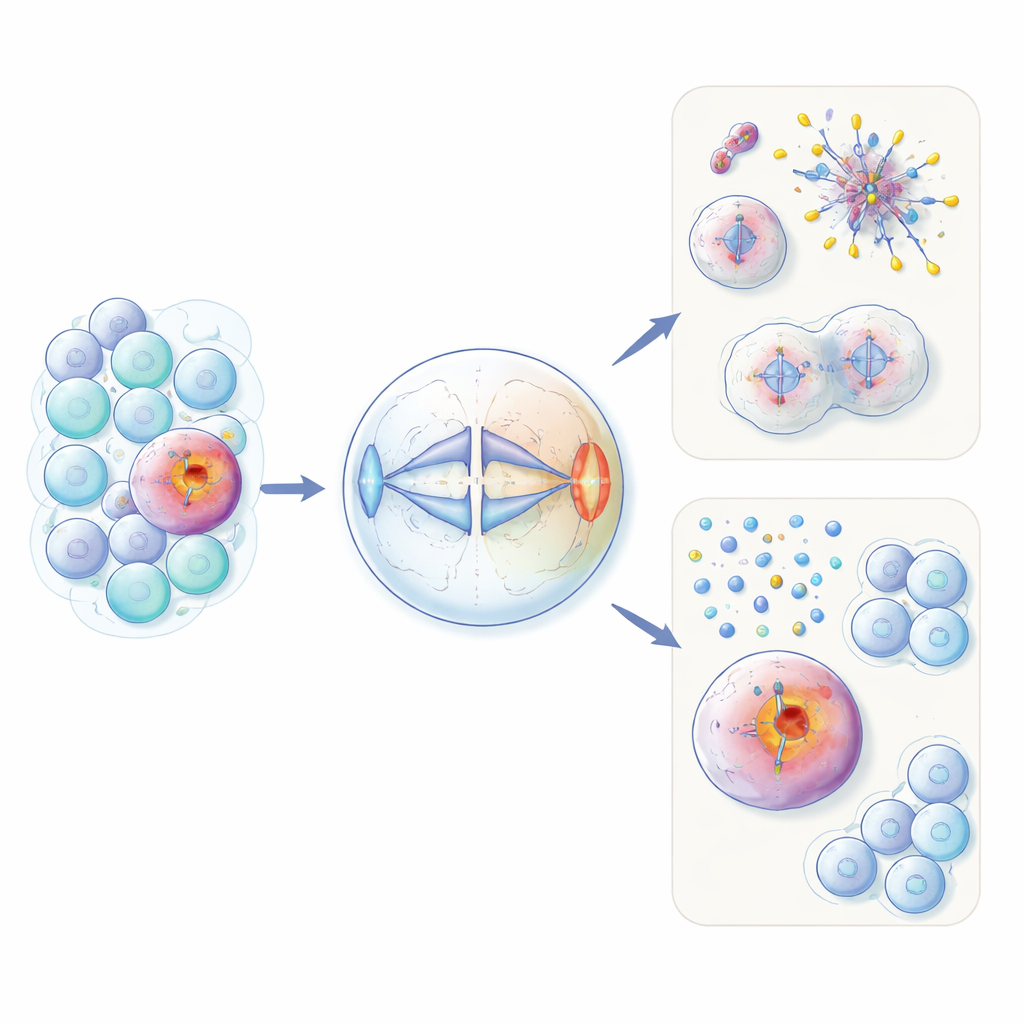
Een verkeerd geplaatste vruchtbaarheidseiwit in kankercellen
HORMAD1 komt gewoonlijk alleen voor in kiemcellen, waar eicellen en zaadcellen ontstaan. Daar helpt het bij het herordenen van DNA en kwaliteitscontrole tijdens de speciale celdeling die meiose heet. De auteurs tonen aan dat in ongeveer 60% van de triple-negatieve borstkankers — en in subsets van meerdere andere tumortypen — dit eiwit onterecht weer wordt aangezet. Met zowel gemodificeerde niet-kankercellen als kankercellijnen vonden ze dat extra HORMAD1 de gelijkmatige verdeling van chromosomen tijdens gewone celdeling verstoort. Cellen die HORMAD1 tot expressie brachten ontwikkelden meer achterblijvende chromosomen, extra of ontbrekende chromosomen (aneuploïdie) en kleine DNA-bevattende "micronuclei", allemaal kenmerken van genoomchaos die bij agressieve kankers worden gezien.
Hoe de veiligheidscontroles bij celdeling normaal werken
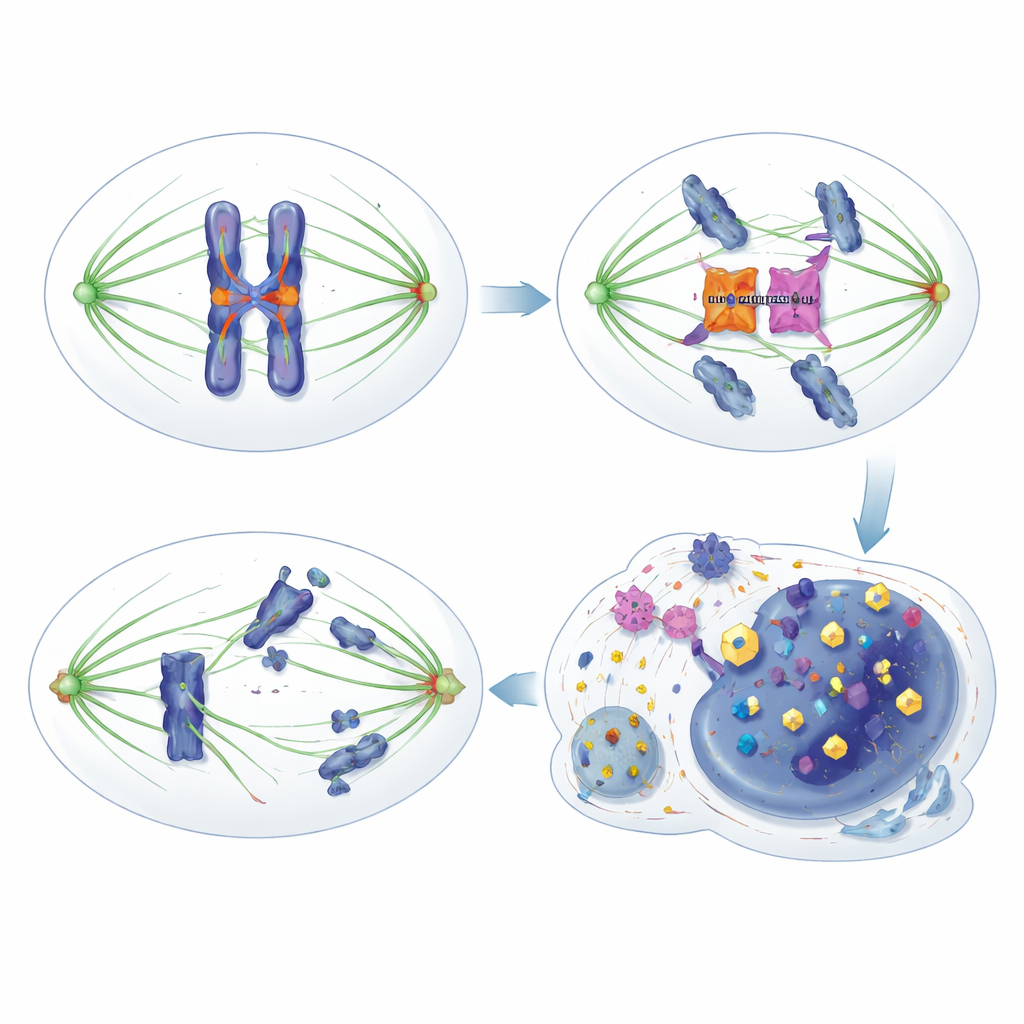
Om correct te delen bouwt een cel een spil van microtubulusvezels die aan elk chromosoom hechten. Een controlesysteem dat het spindle assembly checkpoint wordt genoemd fungeert als een op spanning gevoelig remsysteem: als een chromosoom niet goed is bevestigd, blokkeert de rem de voortgang en voorkomt scheiding totdat fouten zijn hersteld. Verschillende enzymen, mitotische kinases zoals MPS1, Aurora B en BUB1, helpen slechte bevestigingen te detecteren en bevorderen "foutcorrectie" zodat elke dochtercel de juiste set chromosomen ontvangt. Verstoring van dit systeem kan zowel kankerontwikkeling aanwakkeren als bijzondere zwaktes creëren die door bepaalde medicijnen benut kunnen worden.
HORMAD1 verzwakt stilletjes de rem
De onderzoekers ontdekten dat HORMAD1 deze veiligheidsrem op een subtiele maar belangrijke manier ondermijnt. In plaats van te interfereren met klassieke checkpointcomponenten zoals het HORMA-eiwit MAD2L1, bindt HORMAD1 direct aan de kinase Aurora B. Aurora B werkt normaal samen met een ander eiwit, INCENP, om volledig actief te worden en eiwitten bij centromeren en kinetochoren te fosforyleren — kritieke plaatsen op chromosomen waar spilvezels hechten. Wanneer HORMAD1 aanwezig is in delende tumorcellen, concurreert het met INCENP om toegang tot Aurora B, waardoor hun partnerschap afneemt en de activiteit van Aurora B wordt gedempt. Daardoor worden de gebruikelijke fosforyleringssignalen van Aurora B op verschillende doelwitten verzwakt, is foutcorrectie minder effectief en wordt het checkpoint ‘‘lekkend’’: cellen verlaten de mitose te vroeg, zelfs als de bevestigingen fout zijn, wat leidt tot fout verdeelde chromosomen en genoominstabiliteit.
Van zwakte naar therapeutische kans
Aangezien HORMAD1 alleen gedeeltelijk Aurora B en verwante waarborgen uitschakelt, blijven kankercellen net levensvatbaar genoeg om te groeien, maar ze zijn sterk afhankelijk van de resterende functie van mitotische kinases om herhaalde foutieve delingen te overleven. Het team testte dit door HORMAD1-positieve en HORMAD1-negatieve cellen bloot te stellen aan experimentele remmers van MPS1, Aurora B en BUB1. In meerdere modellen maakte HORMAD1-expressie cellen veel gevoeliger voor deze middelen, wat hun vermogen om te prolifereren of kolonies te vormen drastisch verminderde. Het genetisch uitputten van BUB1 was vooral dodelijk alleen in aanwezigheid van HORMAD1, wat een sterke, selectieve afhankelijkheid onthult. In muismodellen met patiënt-afgeleide triple-negatieve borstkankers krimpten tumoren met hoge HORMAD1-niveaus of groeiden ze langzamer wanneer behandeld met een nanopartikelformulering van een Aurora B-remmer, terwijl HORMAD1-negatieve tumoren grotendeels resistent waren tegen dezelfde behandeling.
Wat dit betekent voor patiënten
Voor een leek werkt HORMAD1 als een tweesnijdend zwaard in kanker: het duwt tumorcellen naar grotere chromosomale wanorde, wat de ziekte kan aanjagen, maar daardoor maakt het ze ook hachelijk afhankelijk van een paar overgebleven celdelingswaarborgen. De studie laat zien dat dit verkeerd geplaatste vruchtbaarheidseiwit een belangrijke checkpoint verzwakt door Aurora B te misleiden, waardoor HORMAD1-positieve tumoren bijzonder kwetsbaar worden voor middelen die Aurora B, MPS1 of BUB1 remmen. Omdat HORMAD1 grotendeels afwezig is in normale weefsels maar aanwezig in een duidelijke subset van kankers, zou het kunnen dienen als biomarker om patiënten te identificeren die het meest waarschijnlijk baat hebben bij deze opkomende mitotische kinaseremmers, wat mogelijk nieuwe gerichte behandelopties opent voor moeilijk behandelbare kankers zoals triple-negatieve borstkanker.
Bronvermelding: Walker, C., Kollarovic, G., Weekes, D. et al. Tumour specific HORMAD1 expression perturbs mitotic arrest and drives sensitivity to mitotic kinase inhibitors. Nat Commun 17, 2157 (2026). https://doi.org/10.1038/s41467-026-69561-3
Trefwoorden: HORMAD1, triple-negatieve borstkanker, chromosomale instabiliteit, Aurora B kinase, mitotische checkpoint-remmers