Clear Sky Science · nl
Heterobifunctionele proteomimetische polymeren voor gerichte afbraak van MYC en KRAS
Nieuwe instrumenten om de hardnekkigste kankereiwitten neer te halen
Veel van de gevaarlijkste, kankerveroorzakende eiwitten, zoals MYC en KRAS, zijn lange tijd als “ondrugbaar” bestempeld omdat geneesmiddelen zich er niet makkelijk aan kunnen hechten. Deze studie onthult een nieuw soort zacht, synthetisch materiaal — genaamd HYDRAC-polymeren — dat deze glibberige eiwitten kan grijpen en naar het cellulaire afvalverwerkingssysteem kan sturen. Voor lezers biedt dit werk een inkijkje in hoe scheikunde en nanotechnologie behandelopties kunnen openen voor kankers die traditionele middelen hebben weten te weerstaan.
Een flexibel geraamte in plaats van één pil
De meeste gerichte kankergeneesmiddelen zijn kleine moleculen die in holtes op het eiwitoppervlak passen, zoals een sleutel in een slot. Maar eiwitten zoals MYC zijn slapper en missen geschikte holtes, terwijl KRAS vaak muteert op manieren die klassieke geneesmiddelen omzeilen. De auteurs ontwierpen in plaats daarvan lange, ketenachtige polymeren opgebouwd uit repeterende eenheden. Langs deze ketens bevestigden ze twee soorten componenten: korte eiwitbindende segmenten die een doelwit als MYC of RAS herkennen, en ‘degron’-segmenten die het cellulaire afvalmachinerie aantrekken. Omdat veel kopieën van elk component aan dezelfde keten zitten, kan één HYDRAC-molecuul meerdere eiwitten en enzymen tegelijk bereiken — iets wat moeilijk te realiseren is met een enkel, star geneesmiddelmolecuul.
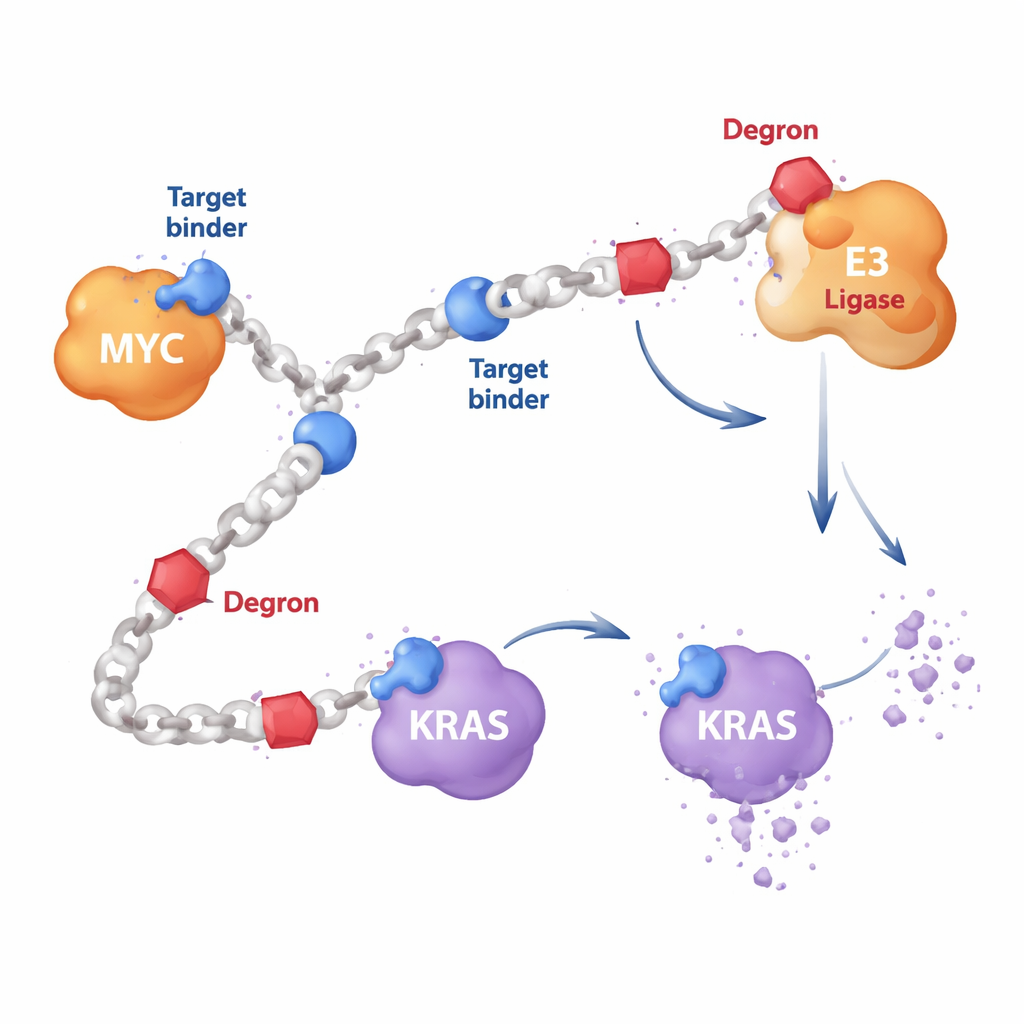
Cellen leren MYC af te breken
Als eerste test richtten de onderzoekers zich op MYC, een meesterregelaar die de groei in veel kankers aanstuurt maar decennialang directe aanvallen heeft weten te weerstaan. Ze bouwden HYDRAC-polymeren die een bekend MYC-bindend peptiden tonen naast een eenvoudig degronmotief dat eiwitten markeert voor vernietiging door het proteasoom, de belangrijkste eiwitversnipperaar van de cel. In buisjesexperimenten vouwden deze polymeren zich tot compacte, eiwitachtige vormen en bonden ze sterk aan MYC, maar niet aan niet-verwante eiwitten. In kankercellen drongen de HYDRACs gemakkelijk binnen, verstoorden door MYC gereguleerde genprogramma’s en leidden tot celdood — effecten die afhankelijk waren van het feit dat zowel het targetende als het degrondelend op dezelfde polymeerketen aanwezig waren.
Van kweekcellen naar krimpende tumoren
In cellen veroorzaakte behandeling met HYDRACs een scherpe daling van MYC-eiwitniveaus zonder dat MYC-RNA verminderd was, wat wijst op daadwerkelijke vernietiging in plaats van alleen stilzetting. Het blokkeren van het proteasoom of van sleutelenzymen die bepaalde afbraakroutes activeren, herstelde MYC-niveaus en toonde daarmee aan dat de polymeren werken door de cellulaire afvalsysteem om te leiden. Proteoom-brede analyses lieten zien dat heel weinig andere eiwitten werden beïnvloed, wat opmerkelijke selectiviteit suggereert. In muismodellen van MYC-gedreven tumoren stapelden fluorescent gelabelde HYDRACs zich na injectie preferentieel op in tumoren en bleven daar dagenlang aanwezig. Herhaalde toediening vertraagde tumorgroei zonder noemenswaardig gewichtsverlies of duidelijke weefselschade, en tumormonsters toonden minder delende cellen en meer tekenen van geprogrammeerde celdood.
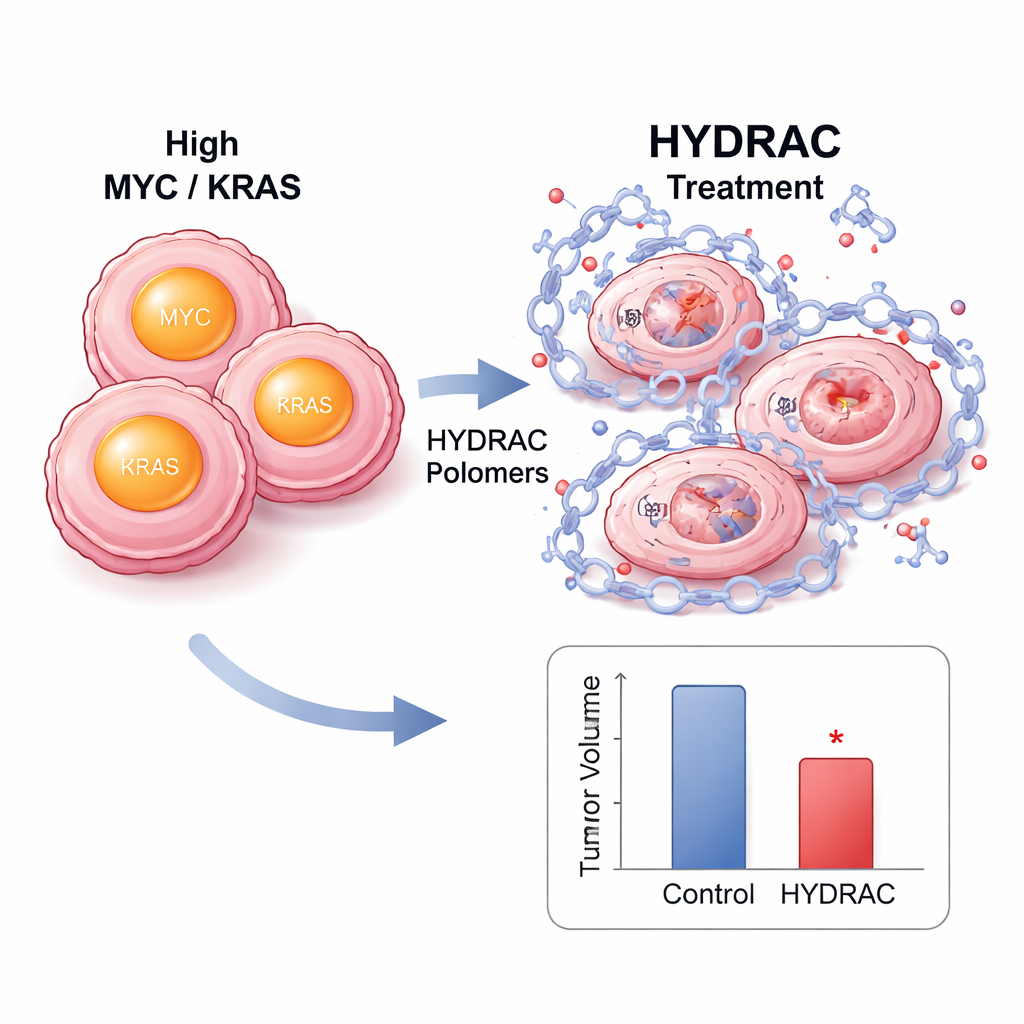
Een plug-and-playplatform voor veel ziektedoelen
Een kracht van de HYDRAC-benadering is dat de zijgroepen als verwisselbare onderdelen kunnen worden uitgewisseld. Het team verving het oorspronkelijke degron door andere rekruterende elementen die verschillende cellulaire enzymen aanspreken, waaronder diegenen die het geneesmiddel thalidomide herkennen. Elke versie degradeerde MYC alleen wanneer het beoogde enzym aanwezig en functioneel was, wat bevestigt dat de polymeren kunnen worden afgestemd op afzonderlijke cellulaire routes. Om de generaliteit te testen bouwden de onderzoekers vervolgens RAS-targetende HYDRACs met een peptide dat RAS-eiwitten herkent. Deze constructen degradeerden succesvol gemuteerd KRAS in twee verschillende kankercellijnen, wat wijst op een “pan-KRAS”-potentieel dat niet afhankelijk is van een specifieke mutatie — een belangrijke stap voor kankers waarin veel KRAS-varianten samen voorkomen.
Waarom dit er toe doet voor toekomstige kankerzorg
Dit werk introduceert HYDRACs als een nieuwe klasse programmeerbare materialen die niet alleen hinderlijke eiwitten blokkeren — ze helpen cellen die uit te wissen. Door veel doelgerichte en afbraak-eenheden op een flexibele polymeer te combineren, omzeilen HYDRACs de ontwerplimieten van traditionele kleine-molecuulgeneesmiddelen en PROTACs, die doorgaans maar één van elk kunnen dragen. Hoewel er nog veel werk nodig is voordat deze materialen de kliniek bereiken, suggereren de resultaten in MYC- en KRAS-gedreven modellen dat lang als “ondrugbaar” beschouwde kankereiwitten kwetsbaar kunnen blijken wanneer geneeskunde meer lijkt op een op maat gemaakte moleculaire borstel dan op één enkele kleine pil.
Bronvermelding: Wang, M.M., Truica, M.I., Gattis, B.S. et al. Heterobifunctional proteomimetic polymers for targeted degradation of MYC and KRAS. Nat Commun 17, 1706 (2026). https://doi.org/10.1038/s41467-026-68913-3
Trefwoorden: gerichte eiwitafbraak, MYC, KRAS, polymeertherapeutica, kanker-nanomedicijn