Clear Sky Science · nl
Integratief epigenomisch landschap van Alzheimer-patiëntenhersenen onthult oligodendrocytaire moleculaire verstoringen geassocieerd met tau
Waarom dit hersenonderzoek ertoe doet
De ziekte van Alzheimer staat het meest bekend om geheugenverlies en de ophoping van twee probleem-eiwitten in de hersenen: amyloïd en tau. Toch kunnen mensen met Alzheimer heel verschillende schadepatronen vertonen, zelfs met dezelfde diagnose. Deze studie stelt een kernvraag: welke schakelaars binnen hersencellen bepalen hoeveel van deze schadelijke eiwitten ophopen en hoe ze verschillende celtypen beïnvloeden? Door te kijken naar chemische labels op DNA in honderden hersenen, vinden de onderzoekers een verrassende koppeling tussen tau en de cellen die verantwoordelijk zijn voor de bedrading van de hersenen.
Chemische labels op DNA als verborgen schakelaars
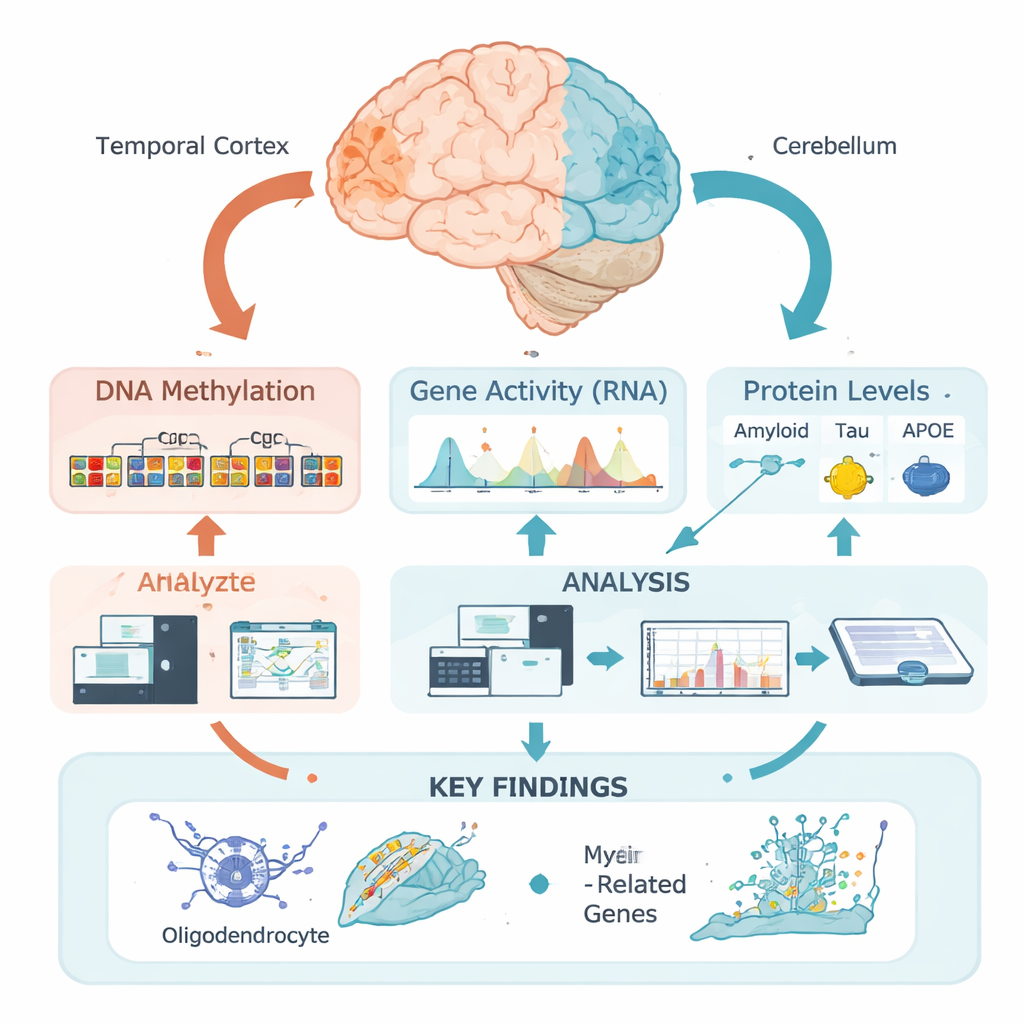
Ons DNA bevat de basisinstructies voor het bouwen en laten werken van hersencellen, maar die instructies worden geregeld door epigenetische markeringen—chemische labels die nabijgelegen genen hoger of lager kunnen zetten zonder de genetische code te veranderen. Een van de belangrijkste labels is DNA-methylering, waarbij kleine chemische groepen zich hechten aan specifieke DNA-locaties. In plaats van enkele sites afzonderlijk te bestuderen, gebruikte dit team een nieuwe „regionale” benadering: ze groeperen veel nabijgelegen sites in functionele zones op basis van hoe het DNA is ingepakt in de temporaalkwab, een regio die sterk door Alzheimer wordt getroffen, en het cerebellum, dat relatief gespaard blijft. Hierdoor konden ze biologisch gezien vragen waar methyleringspatronen veranderen in relatie tot ziektekenmerken.
Het verbinden van DNA-markeringen met Alzheimer-eiwitten
De onderzoekers analyseerden hersenweefsel van 472 mensen bij wie Alzheimer na overlijden was bevestigd. Voor elk staal uit de temporaalkwab maten ze gedetailleerde niveaus van amyloïd, tau en APOE-eiwitten in verschillende biochemische vormen, evenals klassieke microscopische scores voor amyloïde plaques en tau-kluwen. Vervolgens voerden ze epigenoom-brede associatiestudies uit om te testen of regionale DNA-methyleringsniveaus samenhingen met deze metingen. Opmerkelijk genoeg waren vrijwel alle sterke associaties die ze vonden niet gekoppeld aan amyloïd, maar aan tau—vooral aan totaal oplosbaar tau en een membraan-gebonden gefosforyleerde (chemisch gemodificeerde) vorm waarvan wordt gedacht dat die bijzonder toxisch is.
Een sterk signaal in de cellen van de hersenbedrading
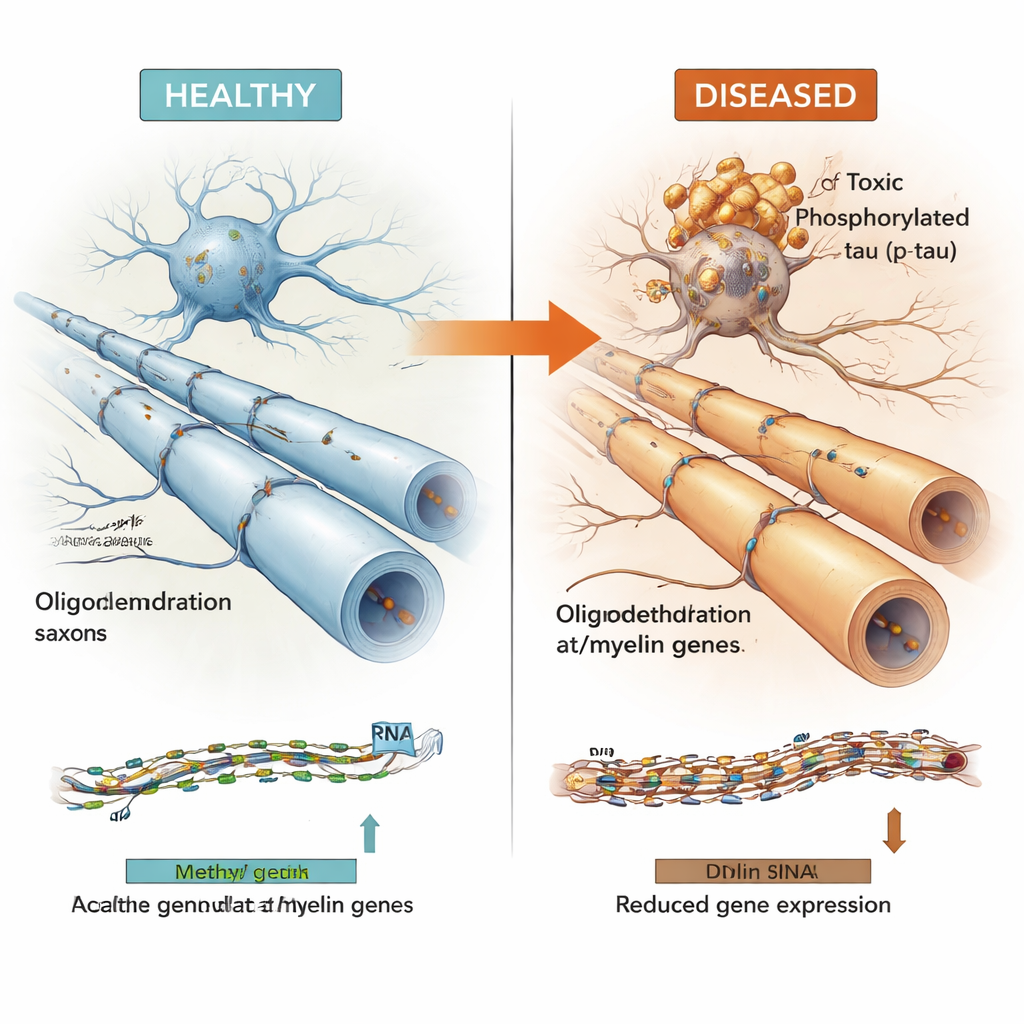
Veel van de DNA-regio’s die aan tau waren gekoppeld lagen in „actieve” delen van het genoom die invloed uitoefenen op nabijgelegen genen. Door methyleringsgegevens te combineren met genexpressiemetingen uit dezelfde hersenen, toonde het team aan dat deze regio’s vaak genen aansturen die door oligodendrocyten worden gebruikt—de cellen die zenuwvezels omhullen met isolerende myeline, waardoor elektrische signalen snel en betrouwbaar kunnen reizen. Belangrijke myeline-gerelateerde genen zoals MBP, MAG en MYRF, samen met het Alzheimer-risicogen BIN1 en een nieuwer kandidaatgen genaamd LDB3, verschenen in deze set. Hogere niveaus van toxisch gefosforyleerd tau gingen vaak gepaard met meer methylering in deze regio’s en lagere expressie van de bijbehorende oligodendrocytaire en myelinegenen, terwijl de meer onschadelijke hoeveelheid oplosbaar totaal tau het omgekeerde patroon liet zien.
Een patroon dat in meerdere hersenziektes terugkeert
Om te testen of deze bevindingen robuust en algemeen gelden, onderzochten de auteurs grote, onafhankelijke datasets uit andere Alzheimer-hersenverzamelingen en uit hersenen die werden getroffen door primaire „tauopathieën” zoals progressieve supranucleaire verlamming en Pick‑ziekte. Hoewel deze cohorten met verschillende technologieën en vaak in andere hersengebieden werden gemeten, vertoonden veel van dezelfde DNA-regio’s en oligodendrocytgenen consistent gedrag: hun methyleringsniveaus hielden verband met de hoeveelheid tau-kluwen, en hun expressie was verlaagd in zieke hersenen en in single-cell-studies die specifiek op oligodendrocyten waren gericht. Belangrijk is dat deze patronen niet eenvoudigweg leken te worden verklaard door genetica of door het algemene verlies van cellen, wat wijst op een daadwerkelijke epigenetische verschuiving in de functie van oligodendrocyten.
Wat dit betekent voor het begrijpen van Alzheimer
Samengevat ondersteunen de resultaten een model waarin stijgende niveaus van schadelijk tau sterk samenhangen met epigenetische veranderingen in oligodendrocyten die myeline-gerelateerde genen dempen, wat mogelijk de hersenbedrading verzwakt en bijdraagt aan cognitieve achteruitgang. Het is nog onduidelijk wat eerst komt—de ophoping van tau of de verstoring van deze myelinegenen—maar de sterke, herhaalde associaties over duizenden monsters en meerdere ziektes wijzen op een gedeeld mechanisme. Door deze DNA-schakelaars in kaart te brengen en te integreren in een openbare „Multiomic Atlas”, benadrukt dit werk oligodendrocyten en hun epigenetische regulatie als veelbelovende doelen voor toekomstige therapieën die gericht zijn op het stabiliseren van hersencircuits, in plaats van uitsluitend op neuronen of amyloïde plaques te focussen.
Bronvermelding: Oatman, S.R., Reddy, J.S., Atashgaran, A. et al. Integrative epigenomic landscape of Alzheimer’s Disease brains reveals oligodendrocyte molecular perturbations associated with tau. Nat Commun 17, 2116 (2026). https://doi.org/10.1038/s41467-026-68864-9
Trefwoorden: Ziekte van Alzheimer, tau-eiwit, DNA-methylering, oligodendrocyten, myeline