Clear Sky Science · nl
Structurele basis van menselijke zink-geactiveerde kanaal (ZAC) signalering en modulatie
Hoe een spoormetaal zenuwcellen helpt communiceren
Zink is vooral bekend als een voedingsstof in multivitaminepillen, maar binnen het lichaam fungeert dit metaal ook als een snelle chemische boodschapper in de hersenen. De hier beschreven studie onthult op atomaire resolutie hoe een weinig bekend eiwit, het zink‑geactiveerde kanaal (ZAC), zink buiten de cellen detecteert en dat signaal omzet in een elektrische reactie. Inzicht in deze bijzondere poort in het celmembraan kan verduidelijken hoe zink de hersenactiviteit vormt en nieuwe mogelijkheden aandragen om zenuwsignalen bij gezondheid en ziekte fijn af te stemmen.
Een speciale poort voor zinksignalen
Veel snelle boodschappen tussen zenuwcellen worden overgebracht door bekende chemicaliën zoals serotonine of acetylcholine, die ringvormige kanalen in het celmembraan openen. ZAC is een verre verwant van deze receptoren, maar in plaats van te reageren op een organische molecule, wordt het geactiveerd door metaalionen zoals zink, koper en protonen. ZAC komt voor in vele menselijke weefsels, waaronder de hersenen, maar ontbreekt bij standaard proefdieren zoals muizen en ratten, wat de voortgang heeft vertraagd. Dit werk gebruikt hoogresolutie cryo-elektronenmicroscopie om meerdere driedimensionale momentopnamen van menselijk ZAC vast te leggen: in de rusttoestand, met gebonden zink, en met twee verschillende geneesmiddelen die het kanaal uitschakelen. Samen laten deze structuren zien hoe zink zich vastzet aan de bovenkant van het kanaal, hoe ionen passeren, en hoe blokkeren de poort dichtklemmen of in een niet-geleidende toestand openwiggen.
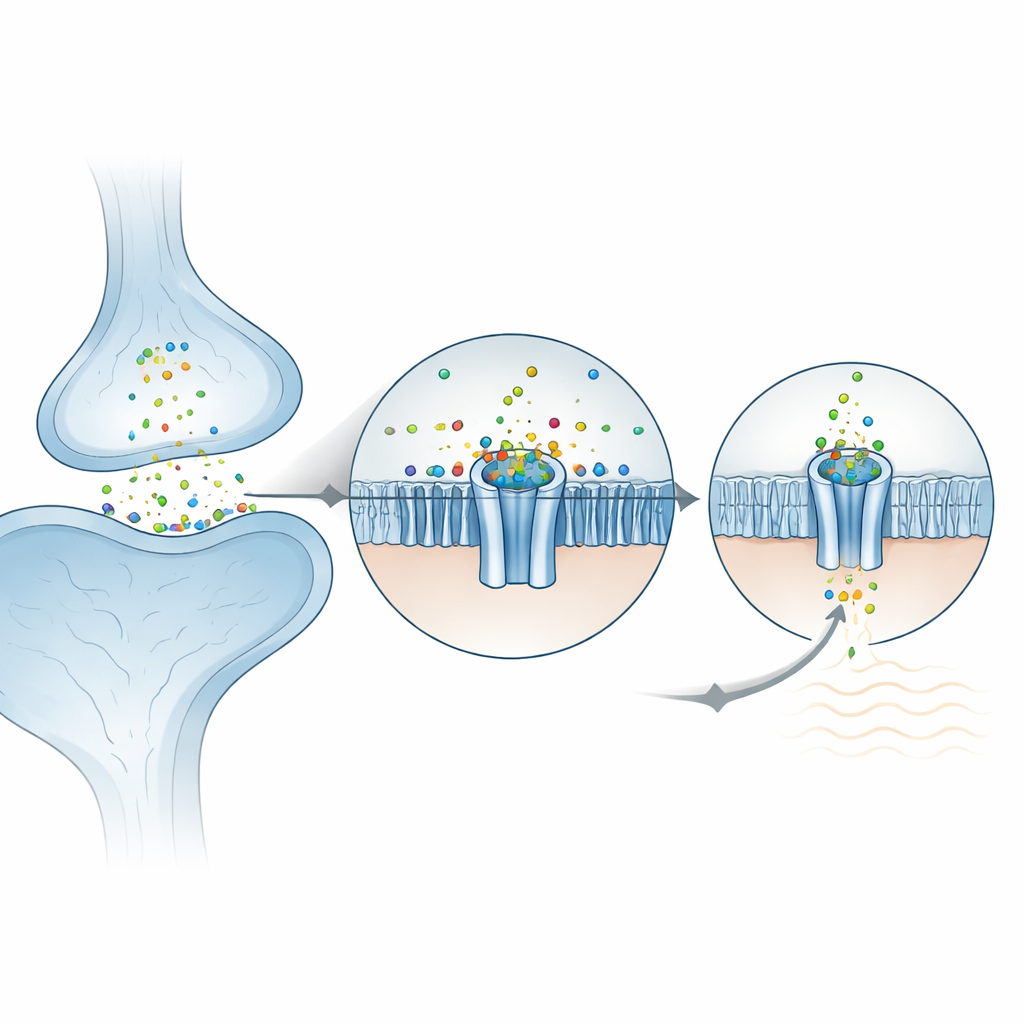
Hoe zink in het kanaal vergrendelt
Aan de buitenzijde van de cel is ZAC opgebouwd uit vijf identieke subunits die een rozet vormen. De onderzoekers vonden dat zinkionen zich nestelen in vijf equivalente zakjes, elk gelegen tussen twee aangrenzende subunits in het buitenste domein. Verrassend genoeg wordt zink niet vastgehouden door de gebruikelijke “grepen” van aminozuren die vaak metalen binden (zoals histidine of cysteïne). In plaats daarvan wordt het voornamelijk gekruld door twee ringvormige aromatische zijketens die het positief geladen ion stabiliseren via zogenoemde kation–π-interacties. Wanneer deze sleutelresiduen in kikkereicellen werden gemuteerd voor elektrische opnames, werd het kanaal ongevoelig voor zink, wat hun centrale rol bevestigt. De omliggende omgeving is al voorgeorganiseerd, wat helpt verklaren waarom ZAC opvallende spontane activiteit vertoont zelfs zonder zink: het eiwit zit dicht bij het kantelpunt tussen gesloten en open en zink duwt simpelweg de balans over.
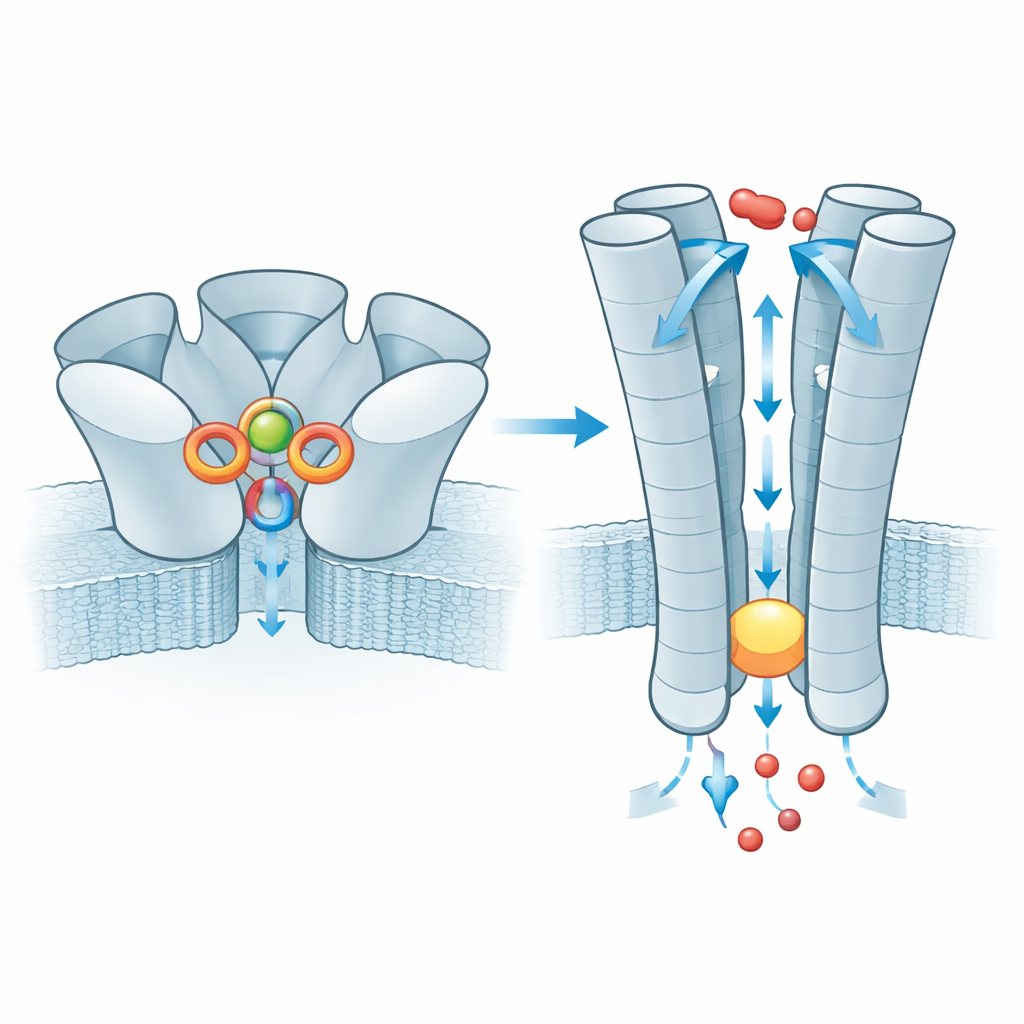
Het pad voor ionen en een veelvoorkomende genetische variant
Zodra zink is gebonden, wordt het effect doorgegeven aan het membraanoverspannende deel van ZAC, waar vijf binnenste helices de porie vormen. In de rusttoestand vernauwt deze buis bij een ring van leucineresiduen, waardoor een hydrofobe stop ontstaat die ionbeweging blokkeert. Met gebonden zink verwijdt de stop net genoeg zodat kleine positieve ionen zoals natrium en kalium erdoor kunnen glippen, terwijl de geladen voering van de porie helpt bij de selectie van deze ionen. Het team onderzocht ook een zeer veelvoorkomende menselijke variant van ZAC waarin één aminozuur (threonine) in een korte streng boven de stop is vervangen door alanine. Deze kleine verandering verzwakt een interactienetwerk tussen naburige subunits dat normaal helpt om zinkbinding naar de poort door te geven, en elektrische metingen laten zien dat kanalen opgebouwd uit deze variant veel kleinere stromen geleiden. De variant fungeert dus als een minder efficiënte signaalomzetter, hoewel de invloed op de menselijke fysiologie onbekend blijft.
Hoe twee geneesmiddelen het kanaal stilleggen
Naast zink onderzoekt de studie ook hoe twee antagonisten, TTFB en d‑tubocurarine (d‑TC), ZAC uitschakelen. TTFB is een op maat gemaakt kleine molecule die zich diep in het membraangebied nestelt, glijdend tussen twee van de pore‑vormende helices net boven de poort. Daar gaat het een wisselwerking aan met een nauw hydrofoob zakje en nabijgelegen polaire residuen, en verstevigt het als het ware de helices zodat ze niet in een volledig open geleidende staat kunnen bewegen. d‑TC, een ouder medicijn dat ooit als spierverslapper werd gebruikt, werkt breder. Eén d‑TC-molecule bindt in hetzelfde buitenste zakje dat normaal zink huisvest, waarbij het de positieve lading van zink nabootst maar voorkomt dat echt zink correct bindt. Een tweede d‑TC-molecule bevindt zich in de ingang van de porie zelf en plugt de tunnel fysiek af. Gezamenlijk vangen deze bindingen ZAC in een gedesensitiseerde, niet-geleidende conformatie terwijl de vorm van het eiwit relatief open blijft.
Wat de bevindingen betekenen voor zink en gezondheid
Dit structurele werk toont op heldere moleculaire wijze aan dat ZAC een ware zinksensor is, die een ongebruikelijke aromatische craddle gebruikt om het metaal te detecteren op hetzelfde type plaats waar andere familieleden neurotransmitters binden. Het identificeert ook specifieke interactienetwerken die bepalen hoe gemakkelijk het kanaal opent en sluit, en kaart twee verschillende geneesmiddelbindingsplaatsen die de poort kunnen dichthaken of de porie kunnen blokkeren. Voor niet‑specialisten is de kernboodschap dat zink niet slechts een statische voedingsstof is maar een actief signaal, en dat ZAC een van zijn toegewijde ontvangers is. Terwijl wetenschappers zoeken naar ZAC’s rollen in het menselijk lichaam en in neurologische aandoeningen die samenhangen met zinkonevenwicht, bieden deze blauwdrukken op atomaire schaal een routekaart voor het ontwerpen van meer precieze moleculen om dit kanaal te moduleren en mogelijk verstoorde zinksignaalgeving te corrigeren.
Bronvermelding: Zhou, Z., Long, Y., Chao, Y. et al. Structural basis of human zinc-activated channel (ZAC) signaling and modulation. Cell Discov 12, 23 (2026). https://doi.org/10.1038/s41421-026-00878-5
Trefwoorden: zinksignaalgeving, ligand-gereguleerde ionkanalen, neuroscience, cryo-EM-structuur, kanalmodulatie