Clear Sky Science · nl
ASCT2-palmitoylering gereguleerd door de JNK1-ZDHHC14-as orkestreert glutaminemetabolisme en NSCLC-progressie
Brandstof voor de vlam van longkanker
Veel snelgroeiende longkankers zijn verslaafd aan glutamine, een veelvoorkomend aminozuur dat dient als belangrijke brandstof en bouwsteen. Deze studie onthult hoe tumorcellen een belangrijke glutamine-"poort" in hun membraan fijnregelen en hoe het verstoren van dit controlesysteem de kankergroei kan vertragen. Inzicht in dit verborgen brandstofventiel verklaart waarom sommige tumoren zo moeilijk uit te hongeren zijn en wijst op nieuwe medicijncombinaties die hun energievoorziening effectiever kunnen afsluiten.
Een cellulair portaal voor glutamine
Glutamine komt cellen binnen voornamelijk via een transportereiwit genaamd ASCT2, dat in het buitenmembraan zit en glutamine naar binnen vervoert. Niet-kleincellige longkanker (NSCLC), de meest voorkomende vorm van longkanker, is vaak sterk afhankelijk van glutamine om snelle celdeling en overleving te ondersteunen. Hoge ASCT2-niveaus in tumoren worden geassocieerd met agressieve ziekte en slechtere patiëntuitkomsten. Toch wordt ASCT2 voortdurend aangemaakt, gemodificeerd en afgebroken, wat de vraag oproept: wat bepaalt hoeveel van deze poortwachter op een gegeven moment op het celoppervlak aanwezig blijft?
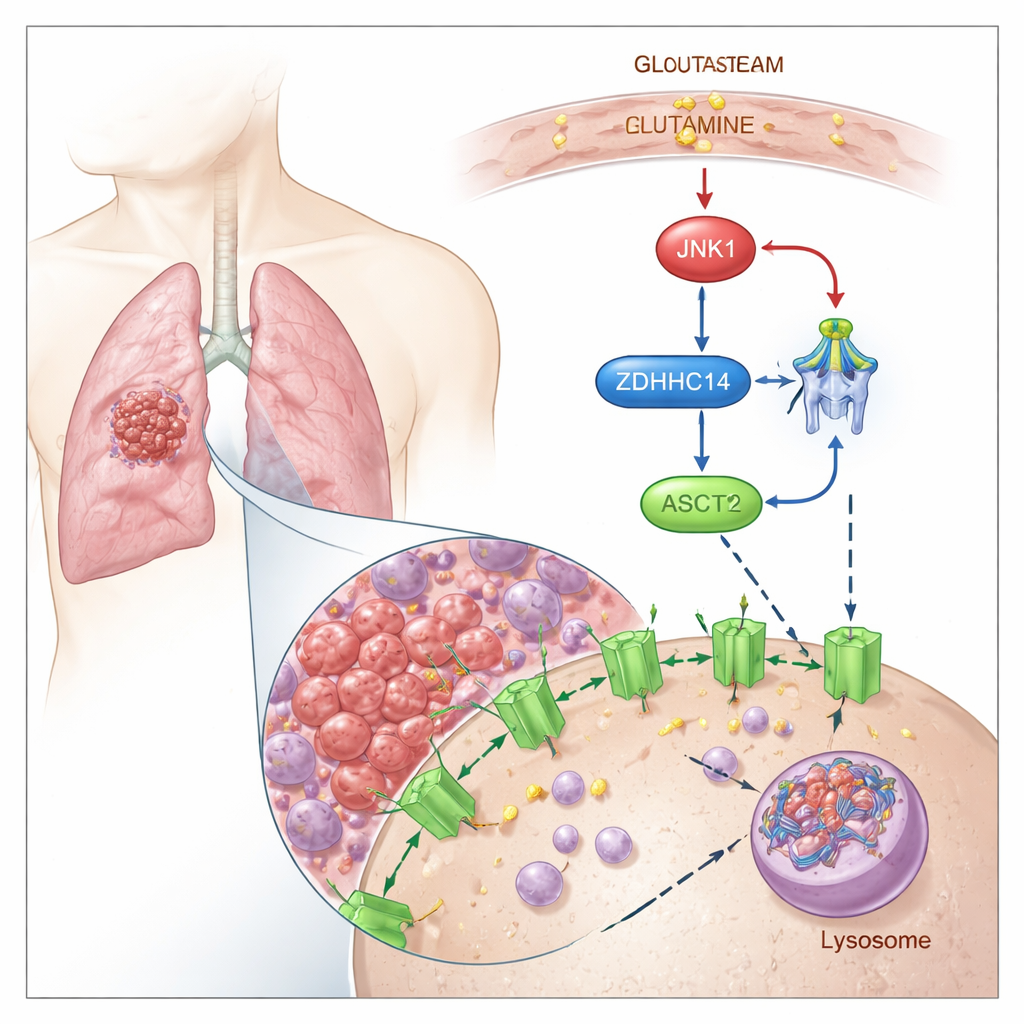
ASCT2 markeren voor afbraak
De onderzoekers tonen aan dat ASCT2 wordt gereguleerd door een chemische "tag" genaamd palmitoylering, waarbij een vetzuur aan specifieke cysteïnebouwstenen in het eiwit wordt gekoppeld. Ze vinden dat een enzym genaamd ZDHHC14 dit lipidetiket aan twee geconserveerde locaties op ASCT2 toevoegt (Cys39 en Cys48). Eenmaal gemarkeerd, wordt ASCT2 omgeleid van het celoppervlak naar cellulaire recyclingcentra, de lysosomen, waar het wordt afgebroken. Het blokkeren van palmitoylering voorkomt dat ASCT2 wordt gemarkeerd en afgebroken, wat leidt tot hogere ASCT2-eiwitniveaus en een verhoogde glutamineopname, zonder de onderliggende genactiviteit te veranderen.
Een tegengesteld enzym dat de poort beschermt
Tegenover ZDHHC14 staat een ander enzym, ABHD17B, dat het vetlabel van ASCT2 verwijdert. Wanneer ABHD17B actief is, is ASCT2 minder gepalmitoyleerd, stabieler en groter de kans dat het wordt gerecycled naar het celoppervlak in plaats van naar het lysosoom te worden gestuurd. Dit heen-en-weer van taggen en ont-taggen fungeert als een fijn afgestelde knop voor de glutaminestroom: ZDHHC14 duwt ASCT2 richting afbraak, terwijl ABHD17B het redt en het glutaminetransport in stand houdt. In longkankercellen verhoogt het verschuiven van dit evenwicht naar minder palmitoylering de glutamineopname en ondersteunt het tumorgroei in kweek en in muismodellen.
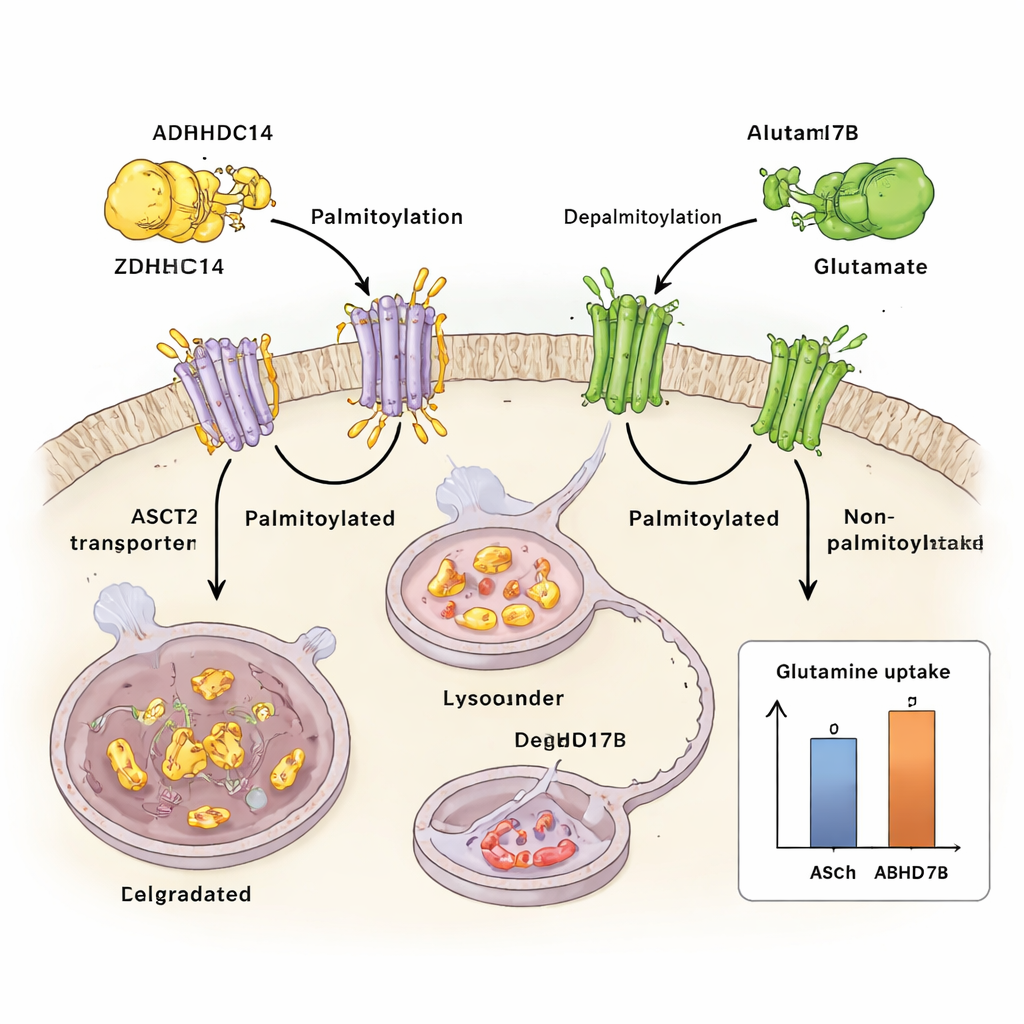
Hoe voedingsstress het systeem herbedraadt
Het team onderzocht vervolgens wat er gebeurt wanneer tumorcellen weinig glutamine hebben. Onder glutaminedeprivatie wordt een stressgevoelig signaalproteïne genaamd JNK1 geactiveerd. JNK1 bindt fysiek aan ZDHHC14 en voegt een fosfaatgroep toe op een specifiek motief (Thr440), waarmee ZDHHC14 wordt gemarkeerd voor zijn eigen lysosomale afbraak. Naarmate ZDHHC14-niveaus dalen, ontvangt ASCT2 minder palmitoyleringstags, ontsnapt het aan afbraak en bouwt het zich op aan het celoppervlak—juist wanneer de cel het meest gebaat is bij het opsporen van schaarse glutamine. Het muteren van deze enkele JNK1-gevoelige plaats stabiliseert ZDHHC14, herstelt ASCT2-tagging en vermindert glutamineopname, wat benadrukt hoe nauw voedingsstress in deze regelkring is ingebouwd.
Het mechanisme vertalen naar therapie
Aangezien ASCT2 zo belangrijk is voor tumormetabolisme, worden middelen die het blokkeren, zoals de experimentele verbinding V9302, onderzocht als kankerbehandelingen. Deze studie laat zien dat JNK1-signalisatie de afbraak van ASCT2 kan tegenwerken en zo effectief de glutaminepoort beschermt. In cel- en muismodellen van NSCLC verminderde een combinatie van een JNK-remmer met V9302 de glutamineopname, tumorcelgroei en tumorgrootte sterker dan elk middel afzonderlijk. Patiëntmonsters en openbare datasets tonen bovendien aan dat lage ZDHHC14- en hoge ASCT2-niveaus vaak voorkomen in NSCLC en geassocieerd zijn met slechtere overleving, wat suggereert dat dit moleculaire patroon kan helpen patiënten te identificeren die het meest baat hebben bij het richten op deze route.
Wat dit betekent voor patiënten
In eenvoudige bewoordingen toont dit werk aan dat bepaalde longkankers hun favoriete brandstof reguleren door een moleculaire klep op hun oppervlak aan te passen. Een trio spelers—JNK1, ZDHHC14 en ABHD17B—bepaalt of de glutaminepoort ASCT2 wordt gemarkeerd voor afbraak of open wordt gehouden. Wanneer glutamine schaars is, verschuift het systeem om ASCT2 te behouden en de brandstoftoevoer te handhaven, waardoor tumoren kunnen overleven onder moeilijke omstandigheden. Door zowel ASCT2 als de JNK-route die het beschermt gezamenlijk te blokkeren, konden onderzoekers kankercellen effectiever uithongeren in laboratorium- en diermodellen. Hoewel meer onderzoek nodig is, biedt deze fosforylering–palmitoylering-as een veelbelovende nieuwe invalshoek voor therapieën die proberen de voedingslifelines van glutaminehongerige longtumoren af te snijden.
Bronvermelding: Chen, X., Ke, Z., Wei, S. et al. ASCT2 palmitoylation regulated by JNK1-ZDHHC14 axis orchestrates glutamine metabolism and NSCLC progression. Cell Discov 12, 13 (2026). https://doi.org/10.1038/s41421-026-00870-z
Trefwoorden: glutaminemetabolisme, niet-kleincellige longkanker, ASCT2-transporter, eiwitpalmitoylering, JNK-signaleringsroute