Clear Sky Science · nl
De moleculaire mechanismen en potentiële therapeutische implicaties van de wisselwerking tussen DNA-methylering en metabole herprogrammering bij schildklierkanker
Waarom dit onderzoek ertoe doet buiten het lab
Schildklierkanker is een van de snelst toegenomen kankersoorten wereldwijd. Hoewel veel gevallen behandelbaar zijn, reageren de agressiefste vormen vaak niet meer op radioactief jodium, een hoeksteen van de behandeling, waardoor patiënten weinig goede opties overhouden. Dit overzichtsartikel legt uit hoe twee onzichtbare krachten in cellen—chemische labels op DNA en veranderingen in hoe tumorcellen hun brandstof gebruiken—samen werken om schildklierkanker te stimuleren en therapieresistentie te veroorzaken. Inzicht in deze verborgen samenwerking zou de deur kunnen openen naar meer precieze en duurzamere behandelingen.
Hoe kankercellen hun instructiehandleiding herschrijven
Elke cel draagt hetzelfde DNA, maar chemische labels genaamd methylgroepen kunnen genen aan- of uitzetten zonder de genetische code zelf te veranderen. Bij schildklierkanker is deze DNA-markering sterk verstoord. Grote delen van het genoom verliezen methylgroepen, wat chromosomen kan destabiliseren, terwijl belangrijke remmen op groei en schildklierfunctie overmatig gemethyleerd en uitgeschakeld raken. Dit betreft onder meer tumorsuppressorgenen en schildklier-specifieke genen die normaal helpen bij het opnemen van jodium. Het resultaat is een genetisch instructieboek waarin veel veiligheidshoofdstukken zijn doorgestreept, wat ongecontroleerde groei en verlies van normale schildklieridentiteit bevordert.
Hoe kankercellen hun brandstofleidingen herbedraden
Tegelijk veranderen schildkliertumorcellen hoe ze energie verkrijgen en gebruiken. In plaats van voornamelijk efficiënt brandstof te verbranden in mitochondriën, leunen ze sterk op snelle maar inefficiënte suikerafbraak, waarbij ze zure bijproducten produceren die hen helpen het immuunsysteem te ontwijken. Ze voeren ook de productie en verbranding van vetten op, en leiden aminozuren zoals serine en glutamine om ter ondersteuning van snelle celdeling. Deze verschuivingen zijn niet willekeurig: ze worden gestuurd door kankerveroorzakende signalen en creëren een flexibel metabolisch netwerk dat tumorcellen in staat stelt te overleven bij lage zuurstof, resistent te zijn tegen medicijnen en op nieuwe locaties te groeien.
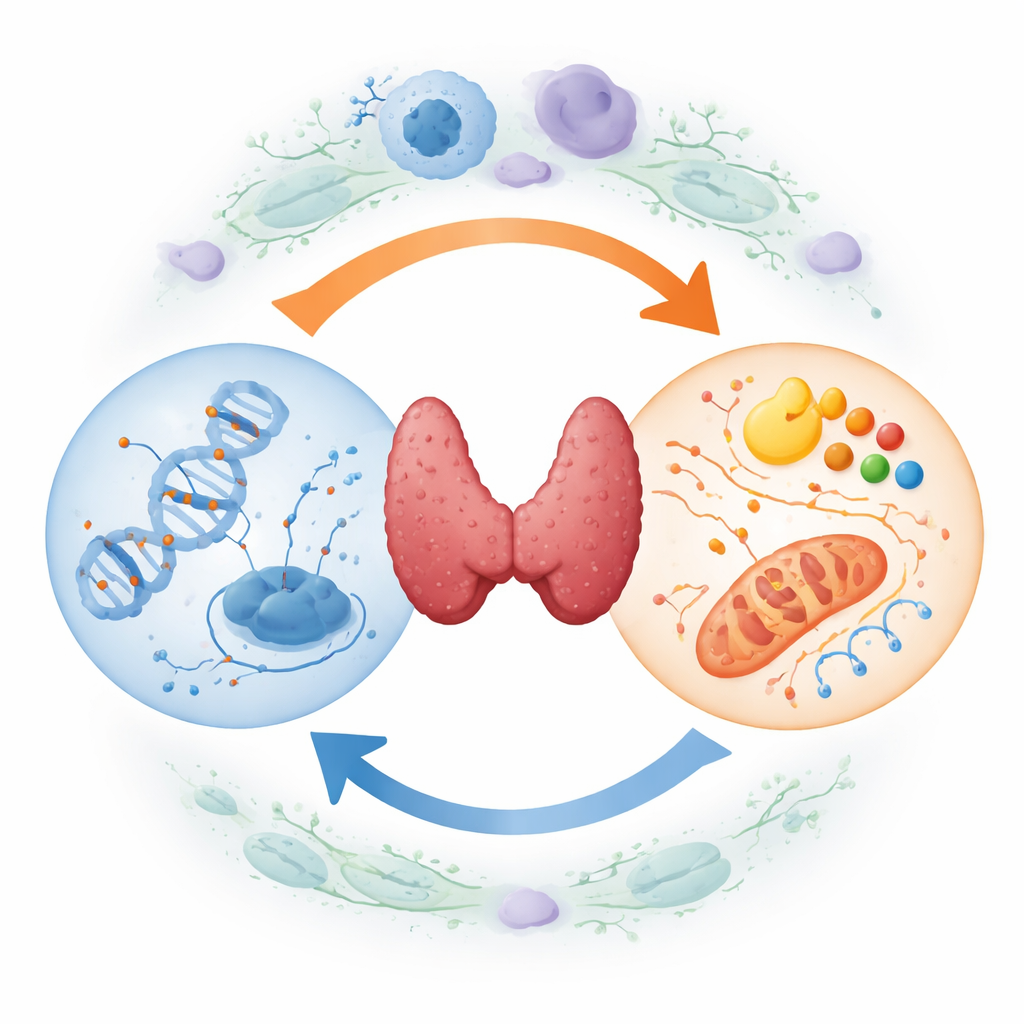
Twee-wegverkeer tussen DNA-labels en celmetabolisme
Een centrale boodschap van het artikel is dat DNA-markering en brandstofgebruik geen losse verhalen zijn—ze vormen een zichzelf versterkende lus. Enerzijds produceert het veranderde metabolisme van tumorcellen specifieke kleine moleculen die fungeren als schakelaars voor de enzymen die methylgroepen op DNA plaatsen of verwijderen. Wanneer de niveaus van deze moleculen veranderen, kunnen ze het genoom duwen naar meer of minder methylering op gevoelige locaties. Anderzijds kan DNA-methylering direct genen stilleggen of activeren die suikergebruik, vetverwerking en aminozuurtransport regelen. In de loop van de tijd vergrendelt dit tweerichtingsverkeer een kankervriendelijk stadium waarin abnormale DNA-markeringen en verstoord metabolisme elkaar voortdurend versterken.
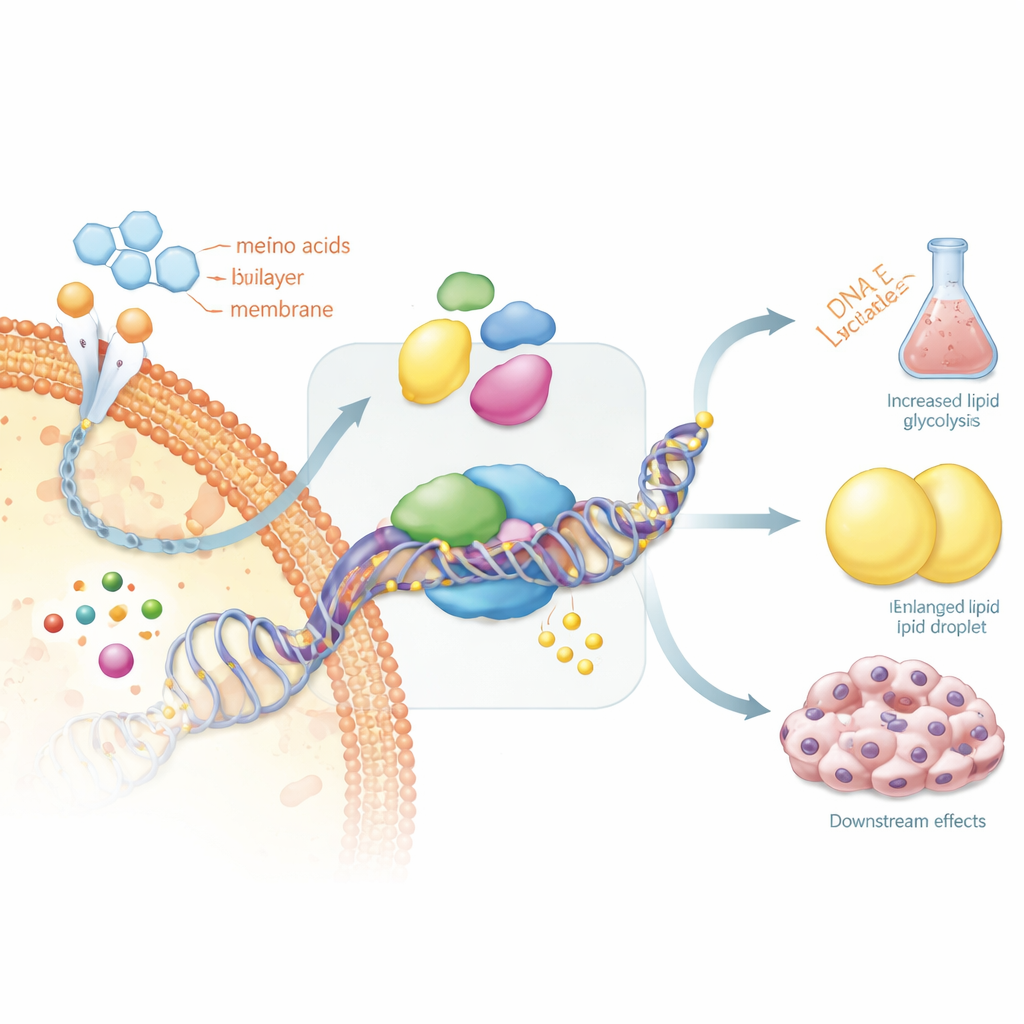
Waarom sommige schildklierkankers stoppen met jodium opnemen
Deze feedbacklus heeft zeer praktische gevolgen voor patiënten. Radioactieve jodiumtherapie werkt alleen als tumorcellen de moleculaire apparatuur behouden die nodig is om jodium binnen te halen. Het overzicht benadrukt dat sleutelgenen van de schildklier die hiervoor verantwoordelijk zijn, waaronder de receptor voor schildklierstimulerend hormoon en de natrium–jodide-transporter, vaak worden stilgelegd door zware methylering van hun regelregio’s. Zodra dit gebeurt, "vergeten" kankercellen dat ze schildkliercellen zijn en nemen ze geen jodium meer op, waardoor de standaardtherapie faalt. De auteurs stellen voor deze DNA-signalen zorgvuldig om te keren, of de metabole paden die ze ondersteunen te blokkeren, om zo de jodiumopname te herstellen en de gevoeligheid voor behandeling terug te winnen.
Nieuwe behandelideeën gebaseerd op een geïntegreerde visie
Het bekijken van schildklierkanker als een ziekte van een "DNA-methylering–metabolisme-as" leidt tot nieuwe therapeutische strategieën. In plaats van te vertrouwen op één enkel geneesmiddel pleiten de auteurs voor combinatiebenaderingen die meerdere onderdelen van de lus tegelijk treffen—epigenetische middelen die schadelijke DNA-tags versoepelen, metabolische middelen die belangrijke brandstofroutes afsluiten, en signaalremmende middelen die de belangrijkste kankerstimulerende paden afzwakken. Het toevoegen van moderne immunotherapieën en geavanceerde middelen voor geneesmiddellevering, zoals slimme nanodeeltjes, zou het evenwicht verder kunnen doen kantelen door de immuunomgeving van de tumor te hervormen terwijl bijwerkingen beperkt blijven. Vroege laboratorium- en klinische gegevens suggereren dat zulke gecoördineerde aanvallen de ziekte mogelijk kunnen vertragen, in sommige patiënten de opname van radioactief jodium kunnen herstellen en resistentie kunnen uitstellen.
Wat dit betekent voor toekomstige zorg
Voor een leek is de conclusie dat agressieve schildklierkankers mogelijk niet met één wondermiddel te genezen zijn, maar door de vicieuze cirkel tussen DNA-markeringen en celmetabolisme te begrijpen en te doorbreken. Door deze as in detail in kaart te brengen en deze veranderingen in bloed- en tumormonsters te volgen, kunnen artsen patiënten mogelijk op den duur koppelen aan op maat gemaakte combinaties van epigenetische, metabole, gerichte en immuuntherapieën. Als dat lukt, zou deze geïntegreerde aanpak de meest hardnekkige schildklierkankers van vandaag weer behandelbaar kunnen maken — en mogelijk voorkomen dat ze zo agressief worden in de eerste plaats.
Bronvermelding: Zhang, T., Han, H., Zhang, Y. et al. The molecular mechanisms and potential therapeutic implications of the crosstalk between DNA methylation and metabolic reprogramming in thyroid cancer. Cell Death Discov. 12, 110 (2026). https://doi.org/10.1038/s41420-026-02981-8
Trefwoorden: schildklierkanker, DNA-methylering, kankermetabolisme, radiojodiumresistentie, gerichte therapie