Clear Sky Science · nl
Het remmen van HSP27 activeert de XBP1s/CerS1-interactie, die DRP1-gedreven mitofagie op gang brengt, waardoor celsterfte wordt tegengegaan en de KSHV-lytische cyclus in primaire effusie-lymfoomcellen wordt bevorderd
Wanneer celstress een tweesnijdend zwaard wordt
Onze cellen overleven dagelijkse aanvallen door noodprogramma’s in te schakelen die schade herstellen en hen in leven houden. Kankercellen kunnen dezezelfde programma’s echter kapen om te groeien en om sluimerende virussen te beschermen. Dit artikel onderzoekt hoe het blokkeren van één stressbeschermend eiwit in een zeldzaam lymfoom niet alleen tumorcellen naar de dood duwt, maar ook een verborgen virus daarin een kans geeft wakker te worden en zich te vermenigvuldigen. Inzicht in dit precieze evenwicht kan helpen bij het ontwerpen van therapieën die kanker doden terwijl ze het virus de kans ontzeggen zich te verspreiden.
Een verborgen virus in agressief lymfoom
Primaire effusie-lymfoom is een zeer agressieve kanker van B-cellen, een type witte bloedcel. De meeste van deze tumorcellen dragen een sluimerende passagier: het aan Kaposi-sarcoom gerelateerde herpesvirus (KSHV). In zijn stille, of latente, staat produceert het virus slechts enkele eiwitten en verbergt het zich in het gastheer-genoom. Bepaalde stressfactoren kunnen het in een actieve, lytische fase duwen waarin het zichzelf kopieert en nieuwe virusdeeltjes produceert, wat meestal de gastheercel doodt. De tumorcellen zelf zijn afhankelijk van meerdere stressresponssystemen, waaronder zogenaamde heat shock-eiwitten en de unfolded protein response, die hen helpen omgaan met verkeerd gevouwen eiwitten, verstoorde vetstofwisseling en schade aan hun energieleverende mitochondriën. 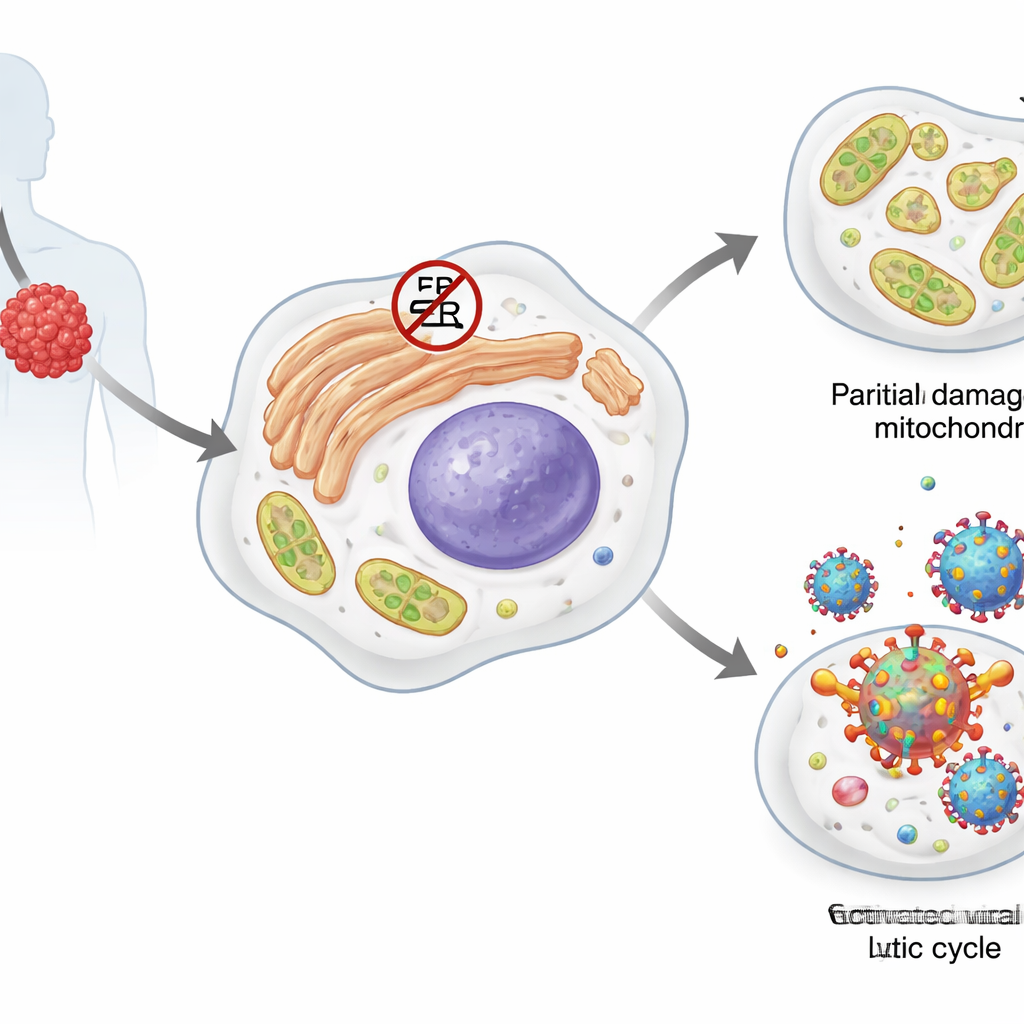
Een cellulair lijfwacht blokkeren
De onderzoekers richtten zich op HSP27, een klein heat shock-eiwit dat bekendstaat om cellen tegen stress te beschermen. Met een chemische remmer genaamd J2 of door het gen te stilte met kleine RNA’s verminderden ze HSP27-activiteit in in het lab gekweekte lymfoomcellen. Dit maakte de cellen minder levensvatbaar en activeerde een sterke stressreactie in een intern membraannetwerk, het endoplasmatisch reticulum. Merkers van deze respons, inclusief beschermende en pro‑dood factoren, namen toe en een belangrijke schakelaar genaamd XBP1s werd aangezet. Tegelijkertijd vertoonden de cellen meer tekenen van geprogrammeerde celdood, wat bevestigt dat het wegnemen van HSP27 hen naar een kantelpunt tussen overleving en ondergang duwt.
Een stresslus die communiceert met celvetten
Stress in het endoplasmatisch reticulum is nauw verweven met hoe cellen vetten verwerken. Het team ontdekte dat het blokkeren van HSP27 de niveaus van CerS1 verhoogde, een enzym dat een specifiek vetmolecuul maakt dat C18-ceramide heet. Toen ze XBP1s chemisch blokkeerden, verdween de stijging van CerS1, wat laat zien dat XBP1s in deze omstandigheden helpt het CerS1-gen aan te zetten. Opmerkelijk genoeg verlaagde het remmen van CerS1 op zijn beurt weer XBP1s, wat een positieve feedbacklus onthult: beide factoren ondersteunen elkaar. Deze moleculaire wisselwerking verandert niet alleen de vetstofwisseling, maar versterkt ook het vermogen van de cel om zich aan endoplasmatisch reticulumstress aan te passen, zelfs terwijl doodsignalen zich opbouwen.
Mitochondriën gerecycled in plaats van vernietigd
Stress in één deel van de cel slaat vaak over naar de mitochondriën, de kleine energiecentrales die energie produceren. Nadat HSP27 werd geremd, produceerden de lymfoomcellen meer reactieve zuurstofsoorten, een teken van mitochondriale problemen, en verhoogden ze de niveaus van DRP1, een eiwit dat mitochondriën in kleinere stukken knipt. De auteurs toonden aan dat de XBP1s–CerS1-lus verantwoordelijk was voor de verhoging van DRP1. Dit activeerde op zijn beurt mitofagie, een kwaliteitscontroletekst waarin beschadigde mitochondriën worden ingepakt in membranen en naar cellulaire ‘recyclingcentra’ genaamd lysosomen worden gebracht. Met behulp van fluorescerende kleurstoffen en eiwitmarkers bevestigden ze dat mitochondriën selectief werden verwijderd. Wanneer ze DRP1 chemisch of genetisch blokkeerden, nam deze mitofagie af en stierven de cellen gemakkelijker, wat betekent dat mitochondriale recycling de gestreste tumorcellen daadwerkelijk hielp vol te houden. 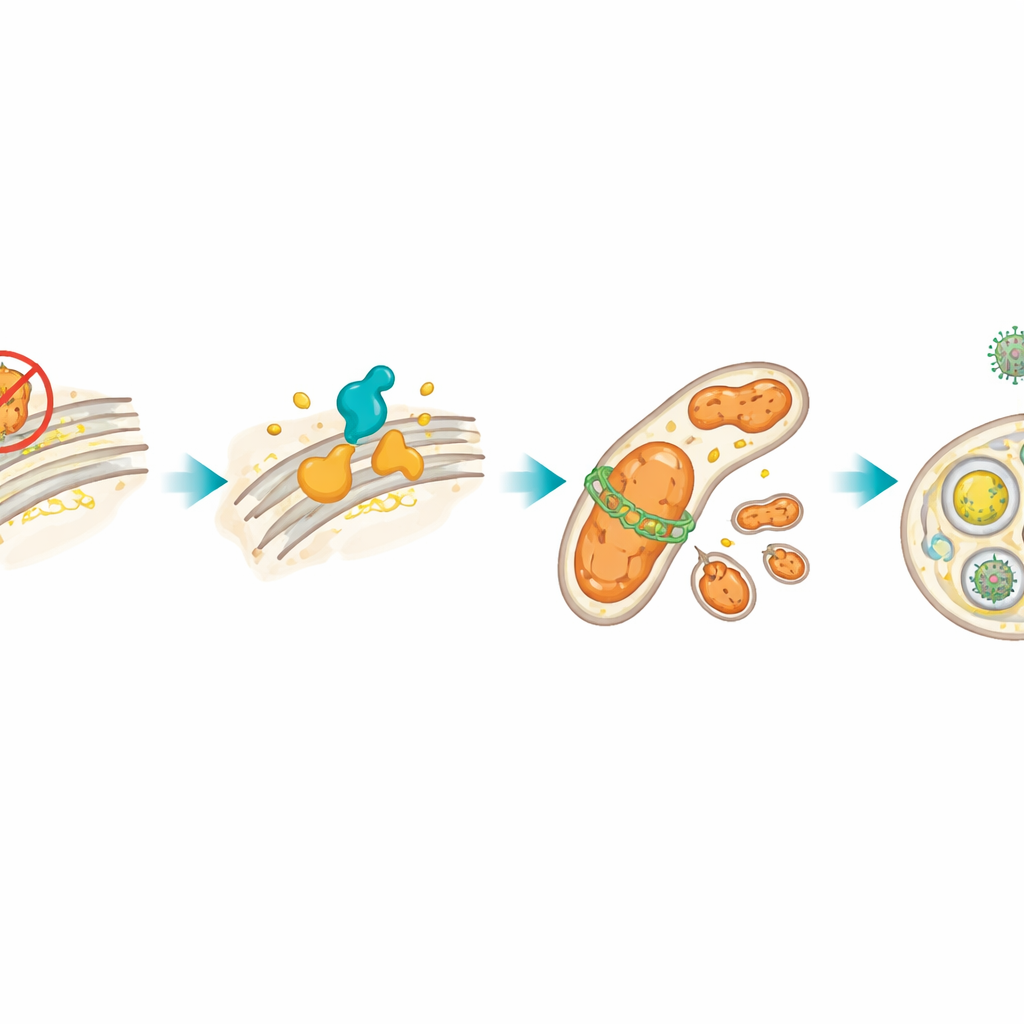
Het virus tijd geven om te ontsnappen
Dezelfde mitofagie die de tumorcellen beschermde, kwam ook KSHV ten goede. Activatie van XBP1s, de ophoping van C18-ceramide en toegenomen mitochondriale splijting zijn allemaal gekoppeld aan het hernieuwd ontwaken van dit virus. Hier, wanneer HSP27 werd geremd, brachten meer cellen vroege en late virale eiwitten tot expressie, duidelijke tekenen van lytische replicatie. Het blokkeren van DRP1, en dus mitofagie, verminderde deze virale reactivatie. De auteurs suggereren dat mitofagie door de overleving van cellen onder stress licht te verlengen KSHV de tijd geeft om zijn replicatiecyclus te voltooien en de stervende cel te verlaten, mogelijk nieuwe doelwitten te infecteren en bij te dragen aan kankervorming.
Wat dit betekent voor toekomstige behandelingen
Voor de niet‑specialist is de belangrijkste boodschap dat HSP27 fungeert als een centrale verkeersleider voor hoe lymfoomcellen met stress omgaan, hoe ze beschadigde mitochondriën recyclen en hoe een met kanker geassocieerd virus beslist wanneer het moet ontwaken. Het uitschakelen van HSP27 ontketent een keten van gebeurtenissen die zowel de celoverleving ondermijnt als, paradoxaal genoeg, cellen tijdelijk beschermt via mitofagie terwijl KSHV zich kan repliceren. Therapeutisch gezien zou het combineren van HSP27‑remming met middelen die DRP1‑gedreven mitofagie blokkeren tumorcellen sneller kunnen laten sterven en de kans van het virus om zich te verspreiden kunnen beperken, wat een tweesporenstrategie biedt tegen dit dodelijke lymfoom.
Bronvermelding: Gonnella, R., Corrado, V., Scaffidi, G.F. et al. Inhibiting HSP27 activates the XBP1s/CerS1 interplay, which triggers DRP1-driven mitophagy, thereby protecting against cell death and promoting the KSHV lytic cycle in primary effusion lymphoma cells. Cell Death Discov. 12, 118 (2026). https://doi.org/10.1038/s41420-026-02979-2
Trefwoorden: primaire effusie-lymfoom, Kaposi-sarcoomvirus, celstressrespons, mitofagie, hittechockeiwit HSP27