Clear Sky Science · nl
AdipoR1–AMPK-as neemt borstkanker onder de duim in verschillende moleculaire subtypes via multimodale celdoodroutes, waaronder ferroptose en apoptose
Waarom vetcellen ertoe doen bij borstkanker
De meesten van ons zien lichaamsvet als een passieve energiereserve, maar vetcellen zijn actieve fabrieken die hormonen en signaalmoleculen in de bloedbaan afgeven. Deze studie onderzoekt hoe een van die vet‑afgeleide signalen, werkend via een molecuul genaamd AdipoR1 op borstkankercellen, de tumorgroei kan vertragen. Het werk is belangrijk omdat het een nieuwe manier suggereert om veel vormen van borstkanker te behandelen door de communicatie tussen vetweefsel en tumoren te benutten, wat mogelijk de effecten van bestaande medicijnen kan versterken.
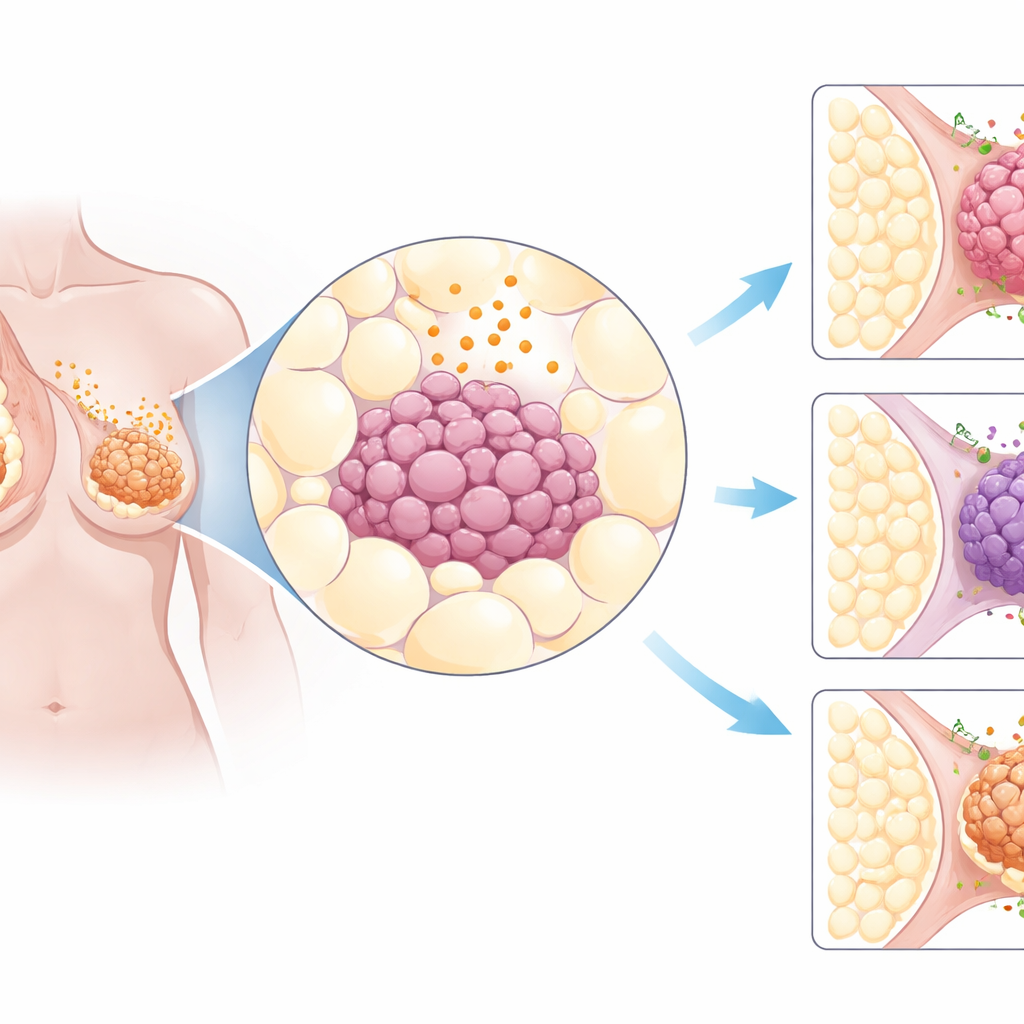
Kijkend over veel kankersoorten heen
De onderzoekers begonnen met het ontginnen van grote openbare kanker‑databases die genetische informatie van duizenden patiëntentumoren bevatten. Ze concentreerden zich op ongeveer drie dozijn genen die betrokken zijn bij signalen afkomstig van vetweefsel en de celstructuren die die signalen ontvangen. Toen ze tumoren uit 31 verschillende organen vergeleken met gezond weefsel, viel één patroon op: borstkankers toonden bijzonder sterke veranderingen in deze vetgerelateerde signalen. In het bijzonder kwam de receptor AdipoR1 vaak op hogere‑dan‑normale niveaus voor in borsttumoren, ongeacht of ze hormoongevoelig, HER2‑positief of het agressievere triple‑negatieve type waren. Weefselmonsters van meer dan 600 borstkankers bevestigden dat het AdipoR1‑eiwit veelvuldig aanwezig was in tumorcellen.
Een vet‑signaalmiddel testen op kankercellen
Om te zien wat AdipoR1 daadwerkelijk in tumoren doet, schakelde het team over op in het laboratorium gekweekte borstkankercellijnen die verschillende veelvoorkomende subtypes vertegenwoordigen. Ze behandelden deze cellen met AdipoRon, een klein molecuul dat AdipoR1 activeert. AdipoRon zette snel een bekende energie‑sensor in cellen in gang, genaamd AMPK, wat aantoonde dat het signaal doorkwam. Naarmate de dosis AdipoRon toenam, deelden kankercellen zich langzamer, bewogen ze minder in wond‑sluitingsproeven en ondergingen veel cellen geprogrammeerde zelfvernietiging. Wanneer de onderzoekers opzettelijk het AdipoR1‑niveau in de cellen verlaagden, verloor AdipoRon veel van zijn werkzaamheid, terwijl het verhogen van AdipoR1 het middel effectiever maakte, waarmee het effect rechtstreeks aan deze receptor werd gekoppeld.
Meerdere manieren om kankercellen naar de dood te duwen
Door genactiviteit na behandeling te analyseren, vonden de wetenschappers dat AdipoRon stressreacties binnen borstkankercellen activeerde. Het zette genen aan die gekoppeld zijn aan klassieke geprogrammeerde celdood evenals genen die betrokken zijn bij een recentelijk herkende vorm van ijzer‑afhankelijke celdestructie, ferroptose genoemd. Sleutelmarkers van dit proces stegen zowel op RNA‑ als eiwitniveau, vooral in hormoon‑gevoelige borstkankercellen, en chemische metingen van beschadigde celvetten ondersteunden deze bevinding. Tegelijkertijd verlaagde AdipoRon de niveaus van eiwitten die normaal gesproken kankercellen helpen te overleven, waaronder DNA‑herstelhelpers (BRCA1 en BRCA2), de oestrogeenreceptor die de groei in veel tumoren aandrijft, en TROP2, een membraaneiwit dat aan agressief gedrag wordt gekoppeld.
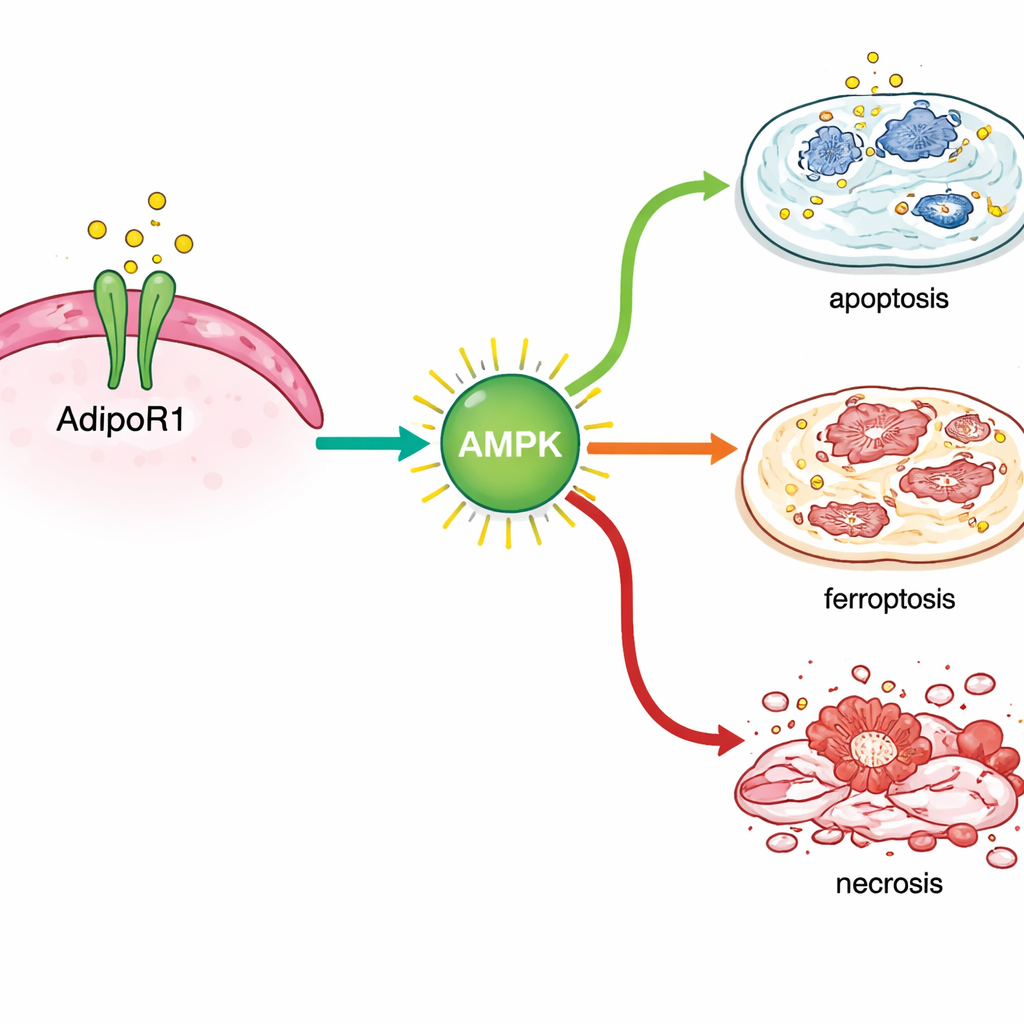
Samenwerkend met, niet tegen, huidige behandelingen
Het team vroeg zich vervolgens af of activatie van AdipoR1 complementair kon zijn aan standaardmedicijnen. In hormoon‑gevoelige borstkankercellen gaf de combinatie van AdipoRon en tamoxifen een sterkere groeiremming dan elk middel afzonderlijk. In triple‑negatieve lijnen versterkte AdipoRon de effecten van veelgebruikte chemotherapiemiddelen zoals paclitaxel en doxorubicine. In muizen met hormoon‑gevoelige borsttumoren kregen de onderzoekers AdipoRon via de mond toegediend. Tumoren in behandelde dieren groeiden langzamer en vertoonden onder de microscoop grotere dode zones. Belangrijk is dat de muizen tijdens de behandeling geen duidelijke bijwerkingen vertoonden in gedrag, gewicht of levergezondheid.
Wat dit voor patiënten kan betekenen
Samengevat suggereren de bevindingen dat het activeren van AdipoR1 in borstkankercellen meerdere overlappende routes naar celdood activeert terwijl het belangrijke overlevingssystemen verzwakt, en dat deze benadering werkt over verschillende genetische vormen van de ziekte. In plaats van bestaande therapieën te vervangen, zouden AdipoR1‑gerichte geneesmiddelen zoals AdipoRon als aanvullingen kunnen dienen die tumoren kwetsbaarder maken voor hormoontherapie, chemotherapie of toekomstige gerichte middelen. Voordat deze strategie de kliniek kan bereiken, moeten onderzoekers krachtigere en selectievere AdipoR1‑activatoren ontwikkelen, verduidelijken bij welke patiënten tumoren de receptor het sterkst tot expressie brengen en de veiligheid zorgvuldig evalueren. Toch wijst dit werk op een intrigerend idee: de signalen van ons eigen vetweefsel zouden kunnen worden omgeleid om te helpen borstkanker te bestrijden in plaats van deze te voeden.
Bronvermelding: Sato, S., Yamanaka, T., Komori, Y. et al. AdipoR1–AMPK axis suppresses breast cancer across molecular subtypes via multimodal cell death pathways, including ferroptosis and apoptosis. Cell Death Dis 17, 384 (2026). https://doi.org/10.1038/s41419-026-08583-7
Trefwoorden: borstkanker, adipokinen, AdipoR1, celdoodroutes, kankermetabolisme