Clear Sky Science · nl
Rol van lipidrafts bij FGFR2c-gemedieerde oncogene signalering door betrokkenheid van het TRPA1-kanaal in pancreatische ductale adenocarcinoomcellen
Waarom kleine eilandjes in celmembranen ertoe doen
Pancreaskanker behoort tot de dodelijkste vormen van kanker, deels omdat de kankercellen uitzonderlijk goed zijn in het losraken van de oorspronkelijke tumor en het binnendringen van omliggend weefsel. Deze studie onderzoekt piepkleine “eilandjes” in de buitenste laag van kankercellen, samengesteld uit cholesterol en lipiden, en stelt een eenvoudige vraag met grote implicaties: helpen deze eilandjes een groeisignaal te activeren dat pancreaskanker agressiever maakt, en kan het ontregelen ervan dat proces vertragen?
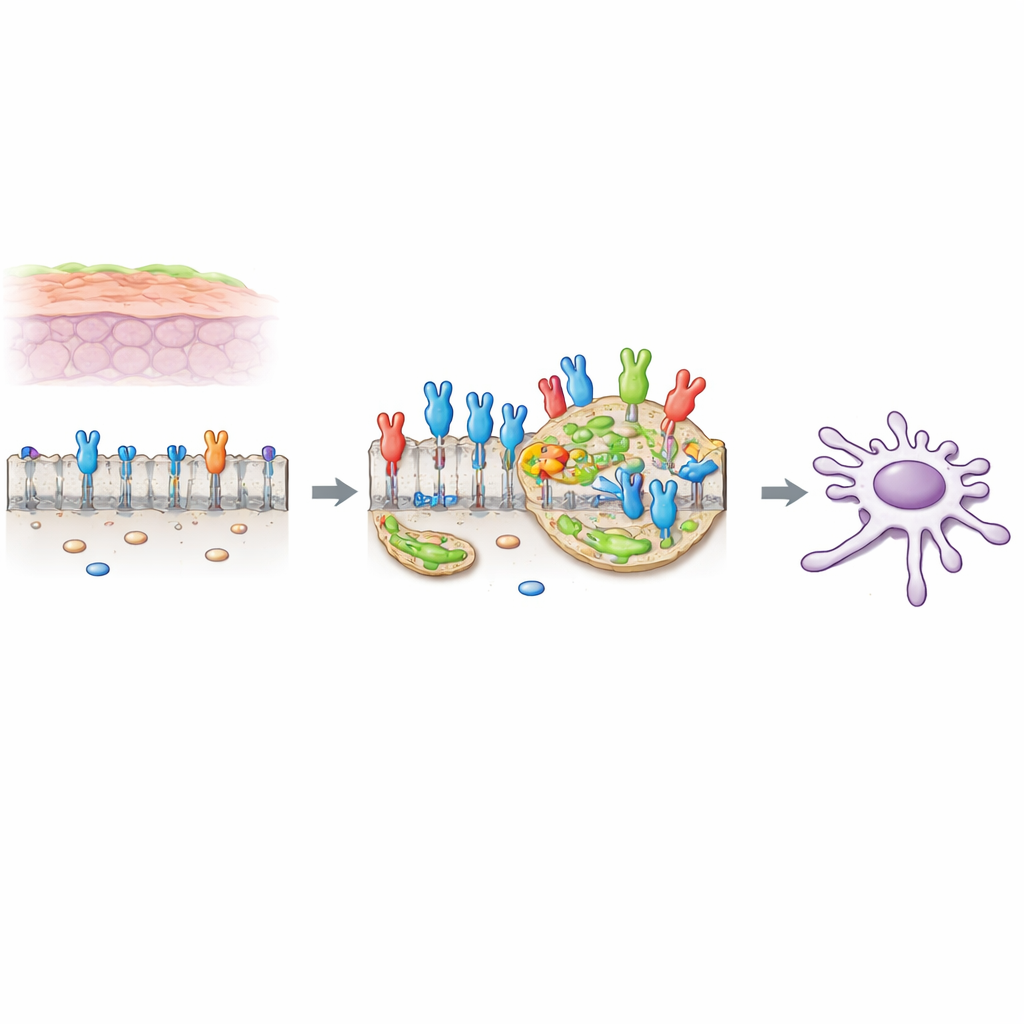
Een kankerversterkende schakelaar aan het celoppervlak
Veel cellen hebben schakelaars aan hun oppervlak die reageren op groeisignalen. Een van deze schakelaars, FGFR2c genoemd, is een variant die normaal gesproken voorkomt in flexibelere, mobielere cellen, maar die abnormaal overvloedig wordt aangetroffen in pancreatische ductale adenocarcinoom (PDAC) cellen. Wanneer deze schakelaar wordt ingeschakeld door zijn partnermolecuul in de omgeving, zet hij veranderingen in gang die bekendstaan als epitheel–mesenchymale overgang (EMT), waardoor cellen minder gehecht raken en beter kunnen bewegen en invaseren. Eerder werk van de auteurs toonde aan dat FGFR2c in PDAC-cellen een keten van interne boodschappers activeert, waarbij het eiwit PKCε en verschillende klassieke groeipaden betrokken zijn, wat de overleving, beweging en invasie van cellen bevordert.
Cholesterolrijke eilandjes als signaalversterkers
Het buitenste membraan van een cel is geen uniform vlak. Het bevat kleine, cholesterolrijke plekjes die lipidrafts worden genoemd en die fungeren als minischaalplatforms waar signalerende moleculen kunnen clusteren en efficiënter kunnen communiceren. De onderzoekers vonden dat wanneer FGFR2c door een extern signaal wordt geactiveerd, meer van de receptor naar deze lipidrafts verschuift. Met behulp van fluorescente markers en biochemische fractionering lieten ze zien dat geactiveerde FGFR2c zich concentreert in deze plekjes, terwijl de verdeling daarbuiten verandert van een glad patroon naar een gestippeld patroon, wat overeenkomt met clustering van receptoren op deze eilandjes.
Het verbreken van de eilandjes verzwakt kankereigenschappen
Om te testen of deze lipidereilandjes essentieel zijn voor de kankerversterkende effecten van FGFR2c, gebruikte het team een verbinding (methyl-β-cyclodextrine) die selectief cholesterol uit het membraan verwijdert en lipidrafts destabiliseert zonder de cellen te doden. In PDAC-cellen met veel FGFR2c verminderde het verstoren van de rafts sterk de activatie van belangrijke signaalmoleculen stroomafwaarts van de receptor en verzwakte het het EMT-programma: genen en eiwitten die samenhangen met een mobiel, invasief stadium namen af, terwijl epitheliale kenmerken gedeeltelijk werden hersteld. Dezelfde behandeling verlaagde ook de niveaus van invasiegerelateerde eiwitten zoals MCL-1, SRC en matrixafbrekende enzymen, en verminderde het vermogen van kankercellen om te bewegen en een gel die het omliggende weefsel nabootst te penetreren. Cellen met zeer weinig FGFR2c reageerden bijna niet, wat onderstreept hoe centraal deze receptor–raft-samenwerking is in deze tumoren.
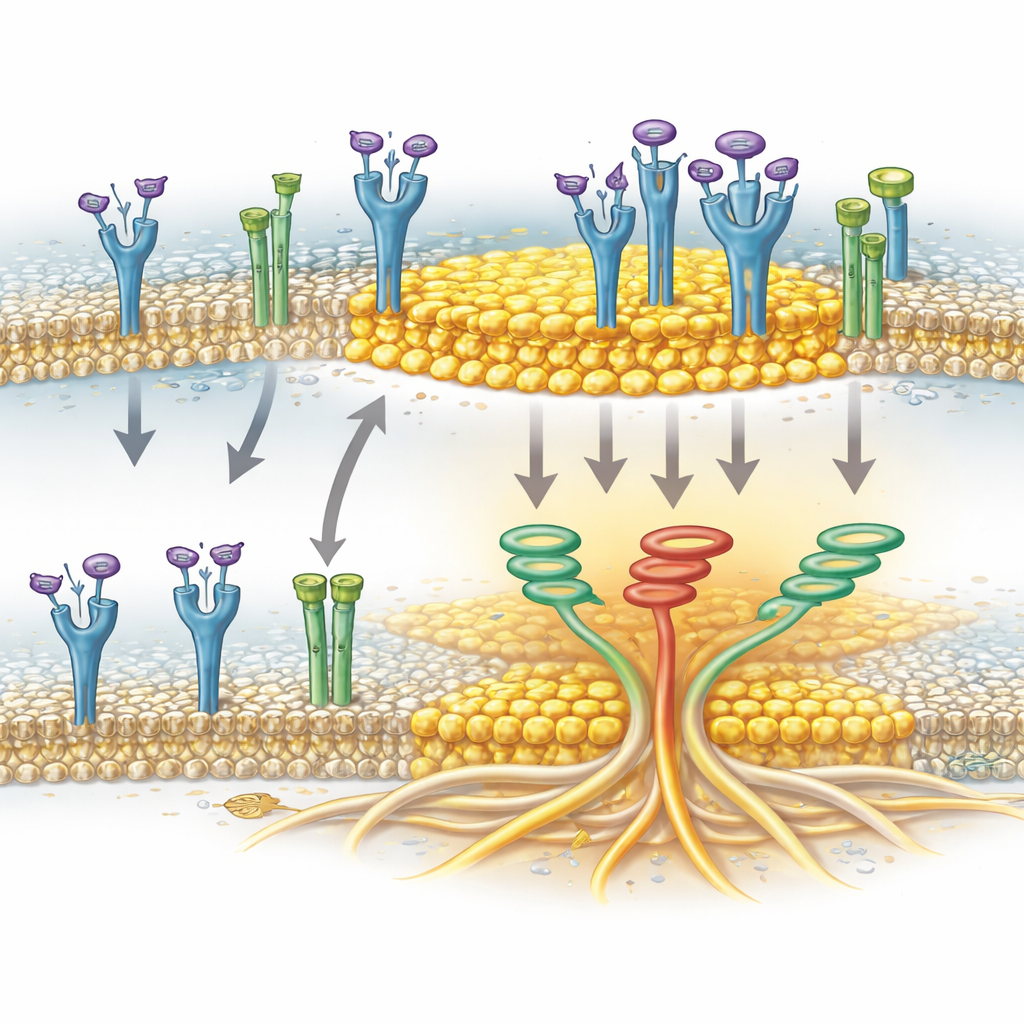
Een ionenkanaal als helper bij clustering
De studie identificeert ook een verrassende helper: TRPA1, een kanaaleiwit dat vooral bekendstaat om het waarnemen van irriterende stoffen en oxidatieve stress in zenuwen. In pancreaskankercellen is TRPA1 aanwezig in het membraan en kan het in lipidrafts worden aangetroffen. De auteurs toonden aan dat TRPA1 fysiek geassocieerd is met FGFR2c wanneer de receptor geactiveerd is en dat deze associatie samenvalt met de verrijking van FGFR2c in raftfracties. Toen de TRPA1-niveaus werden verlaagd, stapelde geactiveerde FGFR2c zich niet langer efficiënt op in de raftgebieden, hoewel de rafts zelf intact bleven. Dit wijst erop dat TRPA1 niet slechts een passagier is, maar actief helpt om FGFR2c naar of in deze cholesterolrijke platforms te begeleiden of te stabiliseren, waar de receptor effectiever het invasieve signaalknooppunt kan activeren.
Wat dit betekent voor toekomstige behandelingen
Samen schetst het werk het beeld dat FGFR2c, TRPA1 en lipidrafts een samenwerkende eenheid vormen die het invasieve gedrag van pancreaskankercellen versterkt. FGFR2c levert het groeisignaal, lipidrafts bieden het fysieke podium waar signaalcomplexen zich vormen, en TRPA1 helpt de receptor op dat podium te brengen. Voor een niet-specialistische lezer is de belangrijkste conclusie dat niet alleen de kankerveroorzakende moleculen zelf, maar ook de kleine membraanlandschappen die ze bezetten, kunnen bepalen hoe gevaarlijk een tumor wordt. Door FGFR2c, TRPA1 of de stabiliteit van deze cholesterolrijke eilandjes aan te pakken — afzonderlijk of in combinatie — zouden toekomstige therapieën in staat kunnen zijn het invasieve mechanisme van pancreaskankercellen op een meer precieze, tumorgemaakte manier te verzwakken.
Bronvermelding: Mancini, V., Manganelli, V., Garofalo, T. et al. Role of lipid rafts in the FGFR2c-mediated oncogenic signaling by involvement of TRPA1 channel in pancreatic ductal adenocarcinoma cells. Cell Death Dis 17, 259 (2026). https://doi.org/10.1038/s41419-026-08513-7
Trefwoorden: pancreaskanker, lipidrafts, FGFR2c, TRPA1-kanaal, celinvasie