Clear Sky Science · nl
Gericht op de p53-kankermutaties Y220C, Y220N en Y220S met de kleinmolecuulstabilisator rezatapopt
Waarom dit belangrijk is voor toekomstige kankerbehandelingen
Kanker schakelt p53, een eiwit dat wel de “bewaker” van de cel wordt genoemd, vaak uit door het te muteren zodat het gevaarlijke cellen niet langer in bedwang kan houden. Een specifieke verandering in p53, bekend als Y220C, komt veel voor in solide tumoren en is een proefcase geworden voor geneesmiddelen die kapot p53 willen herstellen in plaats van cellen rechtstreeks te doden. Deze studie stelt een praktisch, patiëntgericht vraagstuk: kan een veelbelovend experimenteel middel, rezatapopt, dat al in klinische onderzoeken staat voor Y220C, ook helpen bij mensen wier tumoren verwante maar zeldzamere mutaties op dezelfde positie in p53 dragen?
Een middel dat ontworpen is om een barst in p53 te dichten
Veel p53-mutaties zorgen ervoor dat het eiwit openklapt en zijn precieze vorm verliest. Bij de Y220C-mutatie ontstaat er een kleine holte op het eiwitoppervlak — een defect dat chemici zagen als iets wat je met op maat gemaakte kleinmoleculen kon “vullen” om p53 te stabiliseren. Rezatapopt is zo’n molecuul, ontwikkeld op basis van eerdere chemische series die in deze holte binden en als een moleculaire beugel werken. De auteurs richten zich op twee andere mutaties op dezelfde aminozuurpositie, Y220S en Y220N, die ook een vergelijkbare pocket uitsnijden maar p53 nog sterker destabiliseren dan Y220C. Als rezatapopt deze varianten ook zou kunnen dichten, zou dit precisiegeneeskunde voor jaarlijks duizenden extra patiënten kunnen betekenen. 
Meten hoe goed rezatapopt mutant p53 vastgrijpt en stabiliseert
Om dit te testen, zuiverde het team de DNA-bindende kern van p53 met de Y220C-, Y220S- of Y220N-veranderingen en bracht elk bloot aan rezatapopt (en nauw verwante chemische analogen). Met warmtegebaseerde assays toonden ze aan dat alle drie de gemuteerde eiwitten stabieler werden wanneer het middel bond, waarbij Y220C en Y220S effectief stevigheid terugkregen vergelijkbaar met wildtype. Y220N herstelde daarentegen slechts een deel van zijn verloren stabiliteit. Een tweede techniek die de warmte meet die bij binding vrijkomt, liet zien waarom: rezatapopt bindt zeer strak aan Y220C (ongeveer enkele tientallen nanomolair), iets minder sterk aan Y220S, en nog zwakker aan Y220N, hoewel alle affiniteiten binnen reeksen vallen die medicinale chemici veelbelovend achten.
De moleculaire pleister in atomaire detaillering zien
Hoogresolutie-röntgendiffractie-structuren gaven een visuele verklaring. In alle drie de mutanten nestelt rezatapopt zich in de door de mutatie gemaakte spleet met een behouden pose: het centrale skelet vult de holte, het ene uiteinde reikt diep de pocket in met een cluster van fluoratomen en het andere uiteinde interacteert met een nabijgelegen proteïneloop. Het middel vormt een netwerk van contacten, waaronder een strategisch geplaatste fluoratoom dat de eiwitbackbone aangrijpt. Bij Y220S blijven deze interacties bewaard met slechts kleine verschuivingen, waardoor sterke stabilisatie mogelijk is. Bij Y220N dwingt het binden van het middel echter de zijgroep van asparagine in de olierijke kern van het eiwit in een energetisch ongunstige positie, en enkele contacten met het gefluorideerde “anker” van het middel gaan verloren. Deze gespannen passing verklaart zowel de zwakkere binding als het onvolledige herstel van stabiliteit. 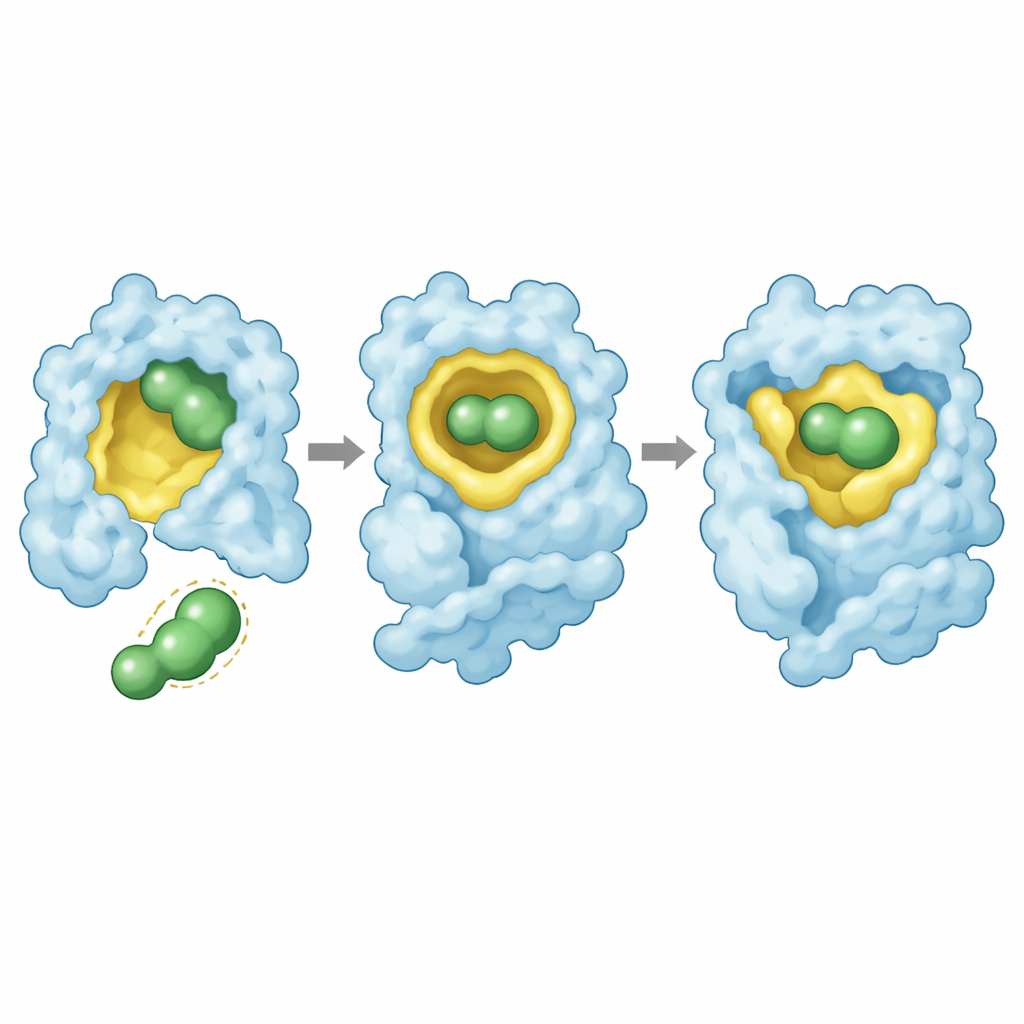
Van eiwitreparatie naar celgedrag
De cruciale proef is of dergelijke stabilisatie p53’s beschermende rol in levende cellen herstelt. De onderzoekers maakten longkankercellen zonder natuurlijk p53 zodat ze respectievelijk de Y220C-, Y220S-, Y220N- of Y220H-varianten konden tot expressie brengen. Bij behandeling met rezatapopt lieten cellen met Y220C een krachtige activatie zien van klassieke p53-doelgenen die betrokken zijn bij het stoppen van de celcyclus en het opwekken van celdood. Y220S-cellen toonden een zeer vergelijkbaar patroon — herstel van de gevouwen, actieve vorm van p53, sterke genactivatie, vertraagde proliferatie en meer celdood — maar alleen bij geneesmiddelconcentraties die meer dan tienmaal hoger lagen dan voor Y220C nodig waren. Y220N-cellen toonden daarentegen bij verdragen doses geen duidelijke activatie van doelgenen en bleven grotendeels in de misgevouwen staat, hoewel lichte, laat optredende groeieffecten wijzen op een slechts gedeeltelijke functionele redding.
Wat dit betekent voor patiënten en toekomstig geneesmiddeldesign
Voor mensen met tumoren die de Y220S-mutatie dragen, zijn deze bevindingen voorzichtig bemoedigend: rezatapopt kan in principe de beschermende functie van p53 herstellen, maar alleen bij aanzienlijk hogere doses, die mogelijk moeilijk veilig te bereiken zijn bij patiënten. Voor Y220N lijkt het huidige middel onvoldoende om p53 onder realistische omstandigheden volledig te repareren. Toch geven de structurele blauwdrukken in dit werk inzicht waarom het huidige ontwerp ondermaats presteert en hoe toekomstige moleculen kunnen worden aangepast om alle drie de gemuteerde zijgroepen te engageren zonder ze in ongunstige posities te dwingen. Met andere woorden, het creëren van een echte "pan-Y220" p53-reparatietherapie is uitdagend maar haalbaar, en zou het aantal patiënten dat baat kan hebben bij deze opkomende strategie van het herstellen in plaats van vervangen van ’s lichaams eigen tumoronderdrukker bescheiden kunnen uitbreiden.
Bronvermelding: Mavridi, D., Funk, J.S., Balourdas, DI. et al. Targeting the p53 cancer mutants Y220C, Y220N, and Y220S with the small-molecule stabilizer rezatapopt. Cell Death Dis 17, 268 (2026). https://doi.org/10.1038/s41419-026-08492-9
Trefwoorden: heractivering van p53, rezatapopt, Y220C-mutatie, precisiemedicijn tegen kanker, eiwitstabilisatie