Clear Sky Science · nl
OTUD4-deubiquitinering stabiliseert EGFR en activeert het PI3K/AKT-pad om de invasiviteit van triple-negatieve borstkanker te bevorderen
Waarom dit onderzoek van belang is voor borstkanker
Triple-negatieve borstkanker is een van de moeilijkst behandelbare vormen van borstkanker omdat ze de gebruikelijke hormoon- en groeimarkers mist waarop veel geneesmiddelen gericht zijn. Deze studie onthult een verborgen "beschermer"-molecuul dat kankercellen helpt een krachtig groeisignaal ingeschakeld te houden. Door dit onzichtbare ondersteuningssysteem te begrijpen, kunnen wetenschappers mogelijk nieuwe manieren vinden om de signalen af te snijden die tumorvorming en -verspreiding aansturen.
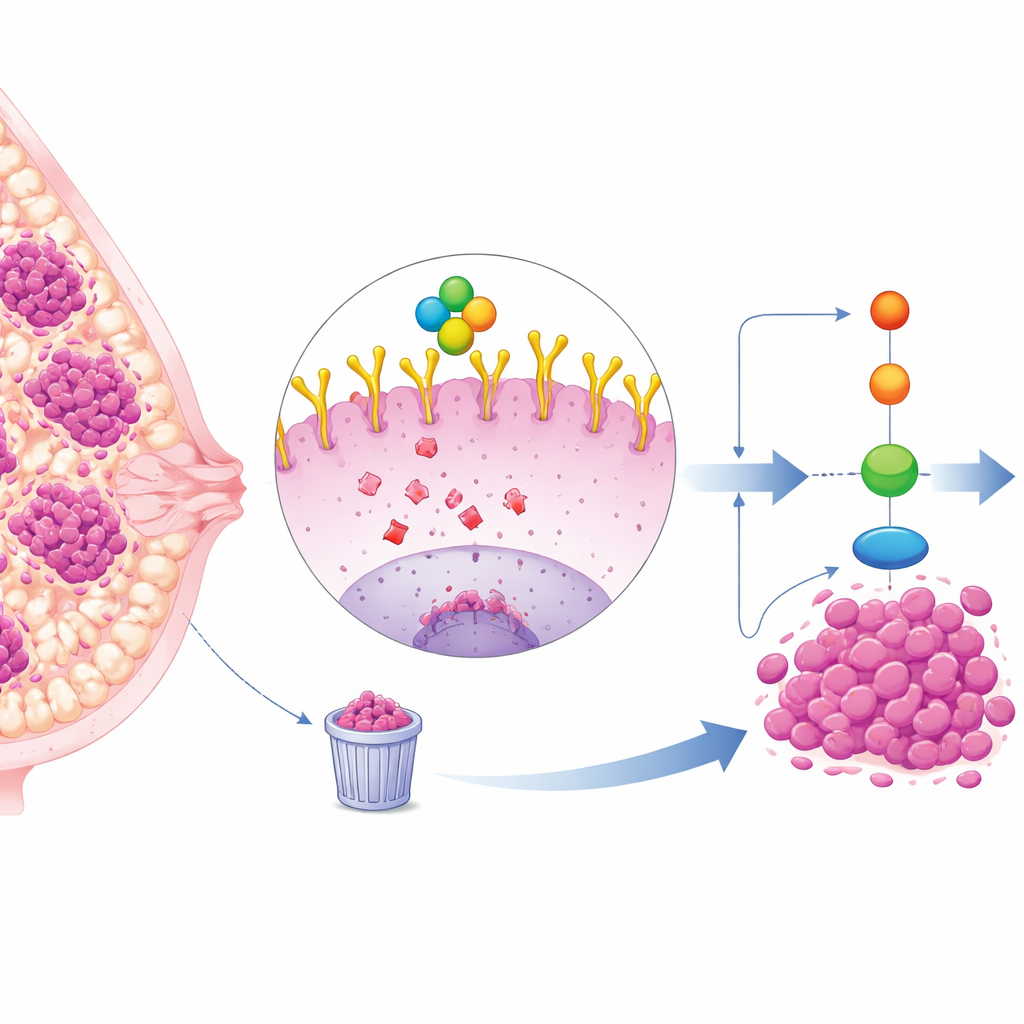
Een moeilijk te behandelen borstkankersubtype
Triple-negatieve borstkanker (TNBC) vormt ongeveer een kwart van de borstkankergevallen en neigt sneller te groeien en uit te zaaien dan andere subtypes. Omdat TNBC-cellen geen oestrogeen-, progesteron- of HER2-receptoren dragen, zijn standaard gerichte therapieën minder effectief, waardoor chemotherapie en chirurgie de belangrijkste opties blijven. Veel TNBC-tumoren vertonen echter hoge niveaus van een celoppervlakte-eiwit genaamd EGFR, dat fungeert als een antenne om groeisignalen en overlevingssignalen te ontvangen. Hoge EGFR-niveaus worden geassocieerd met slechtere uitkomsten, maar geneesmiddelen die EGFR rechtstreeks blokkeren hebben in de kliniek teleurstellende resultaten laten zien, wat suggereert dat er diepere lagen van regulatie aan het werk zijn.
Het vinden van een verborgen helper van tumorgroei
De onderzoekers concentreerden zich op OTUD4, een enzym dat kleine eiwitlabels genaamd ubiquitine van andere eiwitten verwijdert. Deze labels fungeren vaak als afvoer‑signalen en markeren eiwitten om afgebroken te worden; het verwijderen ervan kan het gemarkeerde eiwit stabiliseren en beschermen. Met behulp van grote kankerdatabases en weefselmonsters van patiënten liet het team zien dat OTUD4 in TNBC-tumoren en cellijnen hoger tot expressie komt dan in normaal borstweefsel. Patiënten van wie de tumoren meer OTUD4 bevatten, hadden doorgaans een slechtere overleving, wat erop wijst dat OTUD4 zich gedraagt als een oncogen, een gen dat de kankerprogressie bevordert.
Hoe OTUD4 kankercellen agressiever maakt
Om te onderzoeken wat OTUD4 daadwerkelijk doet in TNBC-cellen, verlaagden de wetenschappers de OTUD4-niveaus in twee veel bestudeerde TNBC-cellijnen. Wanneer OTUD4 werd gereduceerd, groeiden kankercellen langzamer, vormden ze minder kolonies en waren ze minder in staat te migreren in wondgenezings- en Transwell-assays — allemaal aanwijzingen voor verminderde agressiviteit. Toen OTUD4 juist werd verhoogd, gebeurde het omgekeerde: cellen deelden sneller en bewogen gemakkelijker, wat het idee versterkt dat OTUD4 een drijvende kracht is achter malign gedrag. In muizen groeiden tumoren gevormd uit cellen zonder OTUD4 langzamer en toonden ze verminderde markers van celdeling en groeisignalen, wat deze effecten ook in levende organismen bevestigt.
Een moleculair schild dat EGFR beschermt
Om de werkingsmechanismen te achterhalen, gebruikte het team eiwitinteractie‑screens en biochemische assays om EGFR als directe bindingspartner van OTUD4 te identificeren. Ze ontdekten dat OTUD4 zich bindt aan een specifiek deel van EGFR en K48‑gekoppelde ubiquitineketens verwijdert — het type label dat normaal eiwitten markeert voor afbraak door het cellulair recyclingsysteem. Wanneer OTUD4 werd verminderd, degradeerde EGFR sneller, terwijl de genactiviteit van EGFR gelijk bleef, wat aantoont dat OTUD4 na de productie van EGFR werkt en niet op DNA‑ of RNA‑niveau. Het blokkeren van het eiwitafvalsysteem herstelde de EGFR-niveaus, wat benadrukt dat de cruciale stap bescherming tegen afbraak is. Met stabielere EGFR aan het celoppervlak blijft een belangrijk intern signaalpad, het PI3K/AKT/mTOR‑pad, ingeschakeld, wat celgroei en overleving aandrijft.
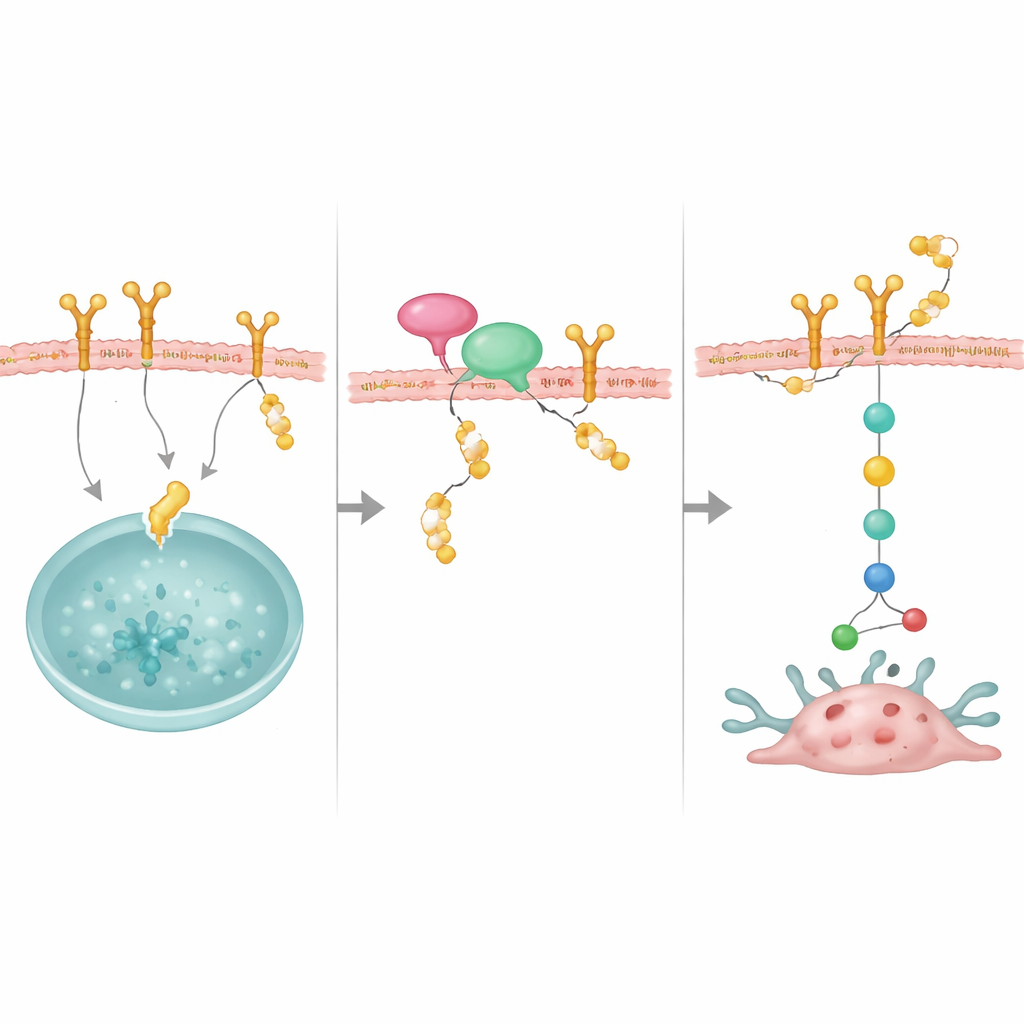
Een adaptor die de beschermer naar zijn doel brengt
De studie bracht ook een belangrijke partner aan het licht, NRP1, een membraaneiwit dat eerder in verband werd gebracht met agressieve borstkankers. NRP1 bindt zowel OTUD4 als EGFR en helpt OTUD4 in positie te brengen om EGFR te redden van vernietiging. Wanneer NRP1 werd verlaagd, werd EGFR minder stabiel en verzwakten zijn groeisignalen, ondanks onveranderde OTUD4-niveaus. Overexpressie van OTUD4 kon het verlies van NRP1 gedeeltelijk compenseren, wat suggereert dat NRP1 fungeert als een aanlegplaats die OTUD4 naar EGFR rekruteert. Samen vormen deze moleculen een stabiliserend complex dat EGFR in overvloed aan het celoppervlak houdt.
Wat dit betekent voor toekomstige behandeling
Door te onthullen hoe OTUD4 en NRP1 samenwerken om EGFR te beschermen tegen afbraak, identificeert deze studie een nieuw regelpunt voor een belangrijk groeisignaal bij triple-negatieve borstkanker. In plaats van te proberen de activiteit van EGFR op zijn actieve plaats te blokkeren, zouden toekomstige therapieën kunnen mikken op het verstoren van de beschermende werking van OTUD4 of diens rekrutering door NRP1, waardoor EGFR-niveaus dalen en het PI3K/AKT‑pad dat tumor groei voedt, wordt gedempt. Hoewel meer werk nodig is om veilige en effectieve OTUD4‑remmers te vinden en mogelijke ontsnappingsroutes die kankercellen gebruiken te begrijpen, openen de bevindingen veelbelovende wegen voor preciezere behandelingen tegen dit uitdagende borstkankersubtype.
Bronvermelding: Ren, Y., Zhou, F., Tan, Z. et al. OTUD4 deubiquitination stabilizes EGFR and activates the PI3K/AKT pathway to promote the invasiveness of triple-negative breast cancer. Cell Death Dis 17, 245 (2026). https://doi.org/10.1038/s41419-026-08482-x
Trefwoorden: triple-negatieve borstkanker, EGFR-signaalgeving, OTUD4, PI3K AKT-pad, proteïnedegeneratie