Clear Sky Science · nl
Korteketenvetzuur‑acyl‑CoA dehydrogenase initieert mtDNA‑demethylering en lek naar buiten om antitumorimmuniteit in colorectale kanker te voeden
Waarom onze eigen cellen kanker soms voor het immuunsysteem verbergen
Colorectale kanker behoort tot de dodelijkste tumoren wereldwijd, deels omdat de immuunverdediging van het lichaam vaak faalt in het herkennen en aanvallen ervan. Deze studie brengt een onverwachte schakel bloot tussen hoe kankercellen vetten verbranden, hoe hun kleine energiecentrales (mitochondriën) met hun DNA omgaan, en of het immuunsysteem op de hoogte wordt gesteld van de tumor. Door deze keten van gebeurtenissen te volgen, benadrukken de onderzoekers ook een oud natuurlijk verbinding, hypericine, als een potentiële manier om de immuunaanval bij colorectale kanker te heractiveren.
Een ontbrekende mitochondriale “bewaker” in darmtumoren
Het team begon met het doorzoeken van grote menselijke en muisdatareeksen om metabole genen te vinden die consistent veranderen bij colorectale kanker. Eén enzym sprong eruit: korteketenvetzuur‑acyl‑CoA dehydrogenase, of ACADS, dat normaal mitochondriën helpt bij het afbreken van korte vetzuren. In zowel patiëntmonsters als verschillende muismodellen waren de ACADS‑niveaus duidelijk lager in tumorweefsel dan in het omliggende gezonde colon. Wanneer de wetenschappers ACADS verminderden in muisdarmkankercellen, groeiden tumoren sneller en agressiever; het verhogen van ACADS vertraagde tumorontwikkeling. Muizen die specifiek in hun darmepitheel geen ACADS hadden ontwikkeld meer en grotere tumoren in een chemisch model van colitis‑geassocieerde kanker, wat ondersteunt dat ACADS als tumorrepressor in de darm fungeert.
Hoe tumoren alarmtekens voor het immuunsysteem dempen
Deze groeieffecten konden niet simpelweg worden verklaard door de snelheid waarmee kankercellen in kweek deelden, die weinig veranderde. In plaats daarvan dreef verlies van ACADS tumorgroei alleen in dieren met een intact immuunsysteem, wat wijst op veranderingen in het tumormicro‑milieu. Enkelcellig onderzoek van menselijke colorectale kankers toonde dat tumoren met lage ACADS omringd waren door meer tumorcellen en immuunsuppressieve cellen — zoals myeloïde suppressorcellen, bepaalde macrofagen en regulerende T‑cellen — en minder behulpzame T‑cellen en natural killer‑cellen. Dit patroon wijst op een “immunosuppressieve buurt” die de kanker beschermt tegen aanval. 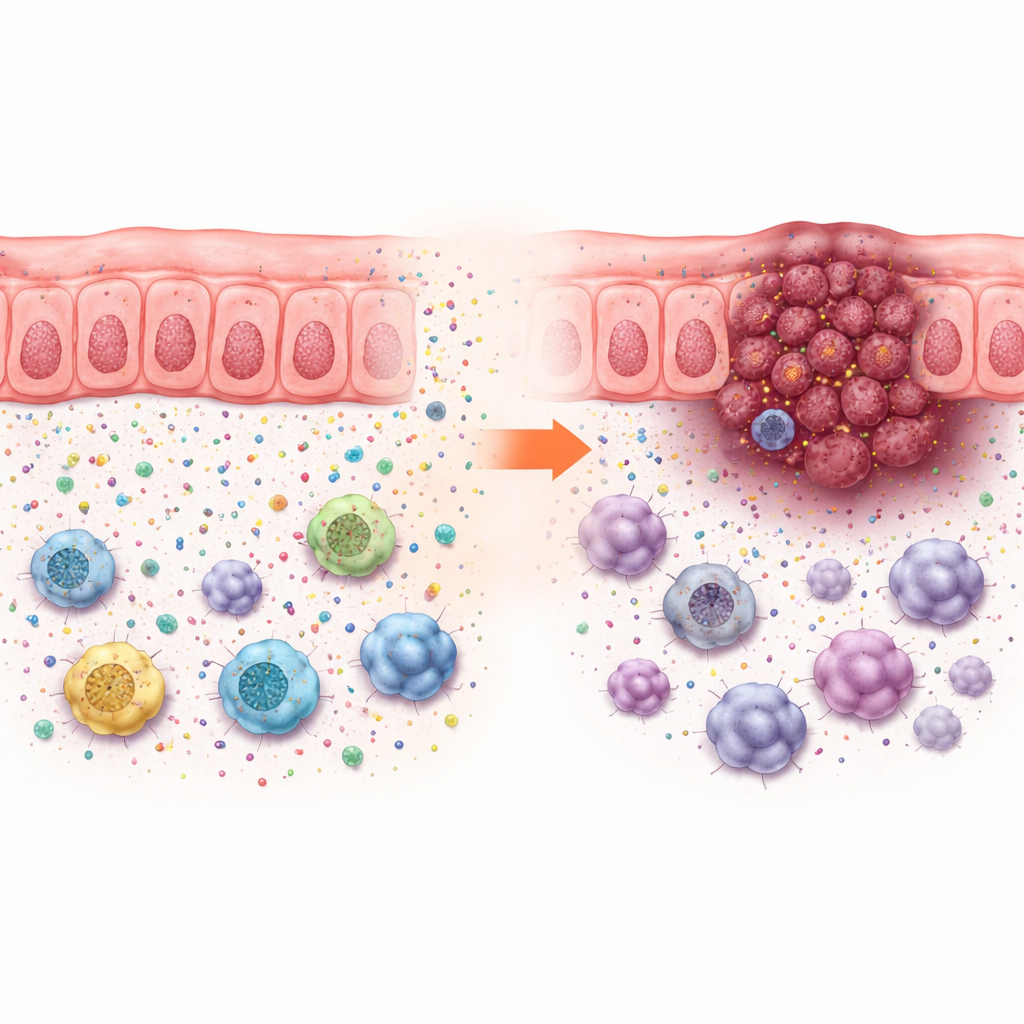
Leak van mitochondrieel DNA als de verborgen trigger
Wat verbindt een vetverbrandend enzym met een immuun‑DNA‑sensor? Het antwoord ligt bij mitochondrieel DNA (mtDNA). Onder stress kunnen fragmenten van mtDNA uit mitochondriën lekken in het omringende celinterstitium, waar cGAS ze als een gevaarsignaal detecteert. De onderzoekers toonden aan dat ACADS‑deficiënte kankercellen minder mtDNA in deze compartimenten hadden, hoewel de totale hoeveelheid mtDNA ongewijzigd bleef. Het blokkeren van mtDNA‑lekken in ACADS‑rijke cellen schakelde cGAS–STING uit, wat bevestigt dat deze ontsnapte DNA‑fragmenten het cruciale alarm vormen. Verrassend genoeg konden klassieke mitochondriale stressfactoren zoals reactieve zuurstofsoorten, calciumpieken en grote veranderingen in mitochondriale morfologie het verschil niet volledig verklaren. In plaats daarvan wijst de studie op de “poorten” in het mitochondriale membraan en, belangrijker nog, op de chemische markeringen op het mtDNA zelf. 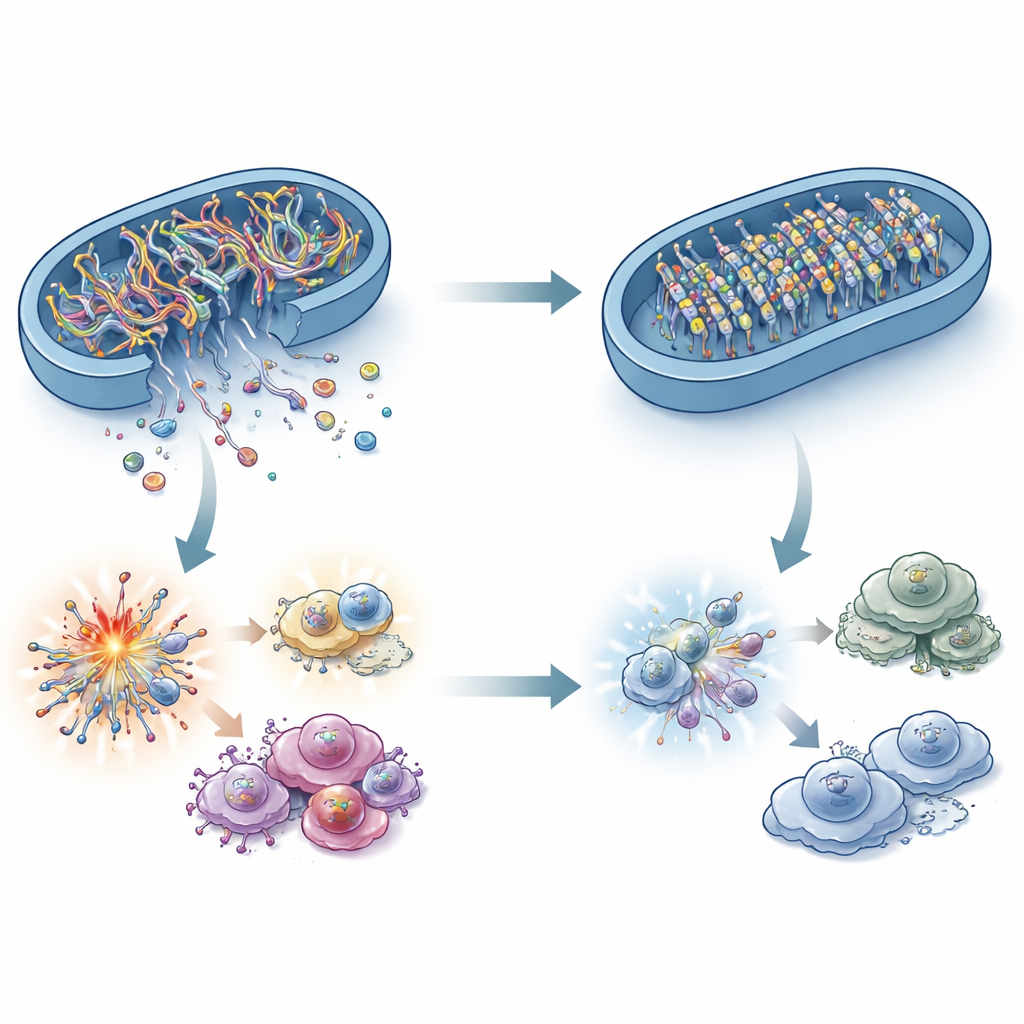
Een DNA‑methylaserende partner die het alarm binnen sluit
Via eiwitinteractiescreens bleek dat ACADS geassocieerd is met een mitochondriaal gelokaliseerde vorm van het DNA‑methylatie‑enzym DNMT1. Wanneer ACADS verloren ging, stapelde deze mitochondriale DNMT1 zich op en plaatste extra methylgroepen op mtDNA. Deze markeringen maken mtDNA stabieler en minder gevoelig voor breuk en lekken. Het overbelasten van cellen met mitochondriale DNMT1 verminderde mtDNA‑ontsnapping, dempte cGAS–STING‑signalering en versnelde tumorgroei, terwijl het blokkeren van DNMT1 met het geneesmiddel decitabine het mtDNA‑lek herstelde en ACADS‑deficiënte tumoren vertraagde. Patiëntmonsters spiegelden deze bevindingen: lage ACADS viel samen met hoge mitochondriale DNMT1, zwakkere STING‑signalen, minder effector‑T‑cellen, meer suppressieve immuuncellen en een slechtere voorspelde respons op checkpoint‑immunotherapie.
Immuunverdediging heractiveren met een oud middel
Om te onderzoeken of dit pad therapeutisch benut kon worden, gebruikten de onderzoekers computergestuurde screening om naar moleculen te zoeken die aan ACADS binden. Ze identificeerden hypericine, een natuurlijk pigment dat eerder is getest als lichtgeactiveerde behandeling voor bepaalde huidlymfomen. In colorectale kankercellen verhoogde hypericine ACADS‑niveaus, verlaagde mitochondriale DNMT1, vergrootte mtDNA‑lekken en heractiveerde cGAS–STING‑signalering — veranderingen die afhankelijk waren van de aanwezigheid van ACADS. In muismodellen van tumoren en in kortetermijnkweken van menselijke colorectale tumoren verkleinde hypericine de tumoren of verschuiven immuuncellen naar een actievere, T‑celrijke staat. Hoewel nader onderzoek nodig is vóór klinisch gebruik, suggereren deze resultaten dat farmacologisch het ‘aanzetten’ van ACADS kan helpen een koude, immunosuppressieve tumor om te zetten in een tumor die beter op immunotherapie reageert.
Wat dit betekent voor patiënten en toekomstige behandelingen
In gewone bewoordingen laat dit werk zien dat sommige colorectale kankers deels groeien omdat ze een mitochondriaal enzym uitschakelen dat normaal kleine DNA‑snippers in het celinterieur laat lekken, waar ze fungeren als fakkels om het immuunsysteem op te roepen. Door een DNA‑methylaserende partner toe te staan dat mitochondriale DNA vast te zetten, verbergen ACADS‑deficiënte tumoren die fakkels en vermijden zo immuundetectie. Het herstellen van ACADS‑activiteit, bijvoorbeeld met hypericine‑achtige middelen, zou dit mitochondriale alarmsysteem weer kunnen openen, de antitumorimmuniteit versterken en de respons op bestaande immunotherapieën verbeteren. ACADS, mitochondriale DNMT1 en STING‑padactiviteit kunnen daarom dienstdoen als nuttige biomarkers en doelwitten in de zoektocht naar effectievere behandelingen voor colorectale kanker.
Bronvermelding: Yang, F., Wang, M., Hu, S. et al. Short-chain acyl-CoA dehydrogenase initiates mtDNA demethylation and leakage to fuel antitumor immunity in colorectal cancer. Sig Transduct Target Ther 11, 113 (2026). https://doi.org/10.1038/s41392-026-02675-8
Trefwoorden: colorectale kanker, tumorimmuniteit, mitochondrieel DNA, lipidenmetabolisme, cGAS‑STING‑pad