Clear Sky Science · nl
FUS (fused in sarcoma) targeten: een nieuwe antisensestrategie voor de behandeling van idiopathische pulmonale fibrose
Waarom littekenvorming in de longen belangrijk is
Idiopathische pulmonale fibrose (IPF) is een meedogenloze longziekte waarbij de fijne luchtzakjes geleidelijk veranderen in stijve littekenweefsels, waardoor elke ademhaling zwaarder wordt. De huidige medicijnen kunnen deze littekenvorming vertragen maar niet stoppen of omkeren. Deze studie verkent een nieuw doelwit genaamd FUS, een eiwit dat cellen helpt hun genetische boodschappen te verwerken, en onderzoekt of het uitschakelen ervan met een ontworpen streng van DNA-achtige stof het littekenproces kan temperen en beschadigde longen kan helpen herstellen.
Een cellulaire verkeersleider die ontspoort
FUS is een eiwit dat normaal in de kern van de cel zit en helpt bij het beheren van hoe RNA — de werkende kopie van onze genen — wordt verwerkt en gebruikt. Bij hersenziekten zoals ALS kan FUS zich misdragen door de kern te verlaten, samen te klonteren in de buitenste delen van de cel en zo de normale celwerking te verstoren. De auteurs vroegen zich af of een soortgelijk mislopen van FUS bijdraagt aan littekenvorming bij IPF. Ze bestudeerden longfibroblasten — de bindweefselcellen die littekenmateriaal afzetten — van patiënten met IPF en van gezonde donoren. In IPF-cellen waren de FUS-niveaus over het geheel genomen hoger en, cruciaal, veel meer FUS werd in het cytoplasma aangetroffen dan in gezonde cellen. Met behulp van hoogresolutie-elektronenmicroscopie bevestigden ze dat dit eiwit abnormaal vaak buiten de kern aanwezig was, wat erop wijst dat de normale controle over RNA in gefibrotiseerde longen verstoord kan zijn. 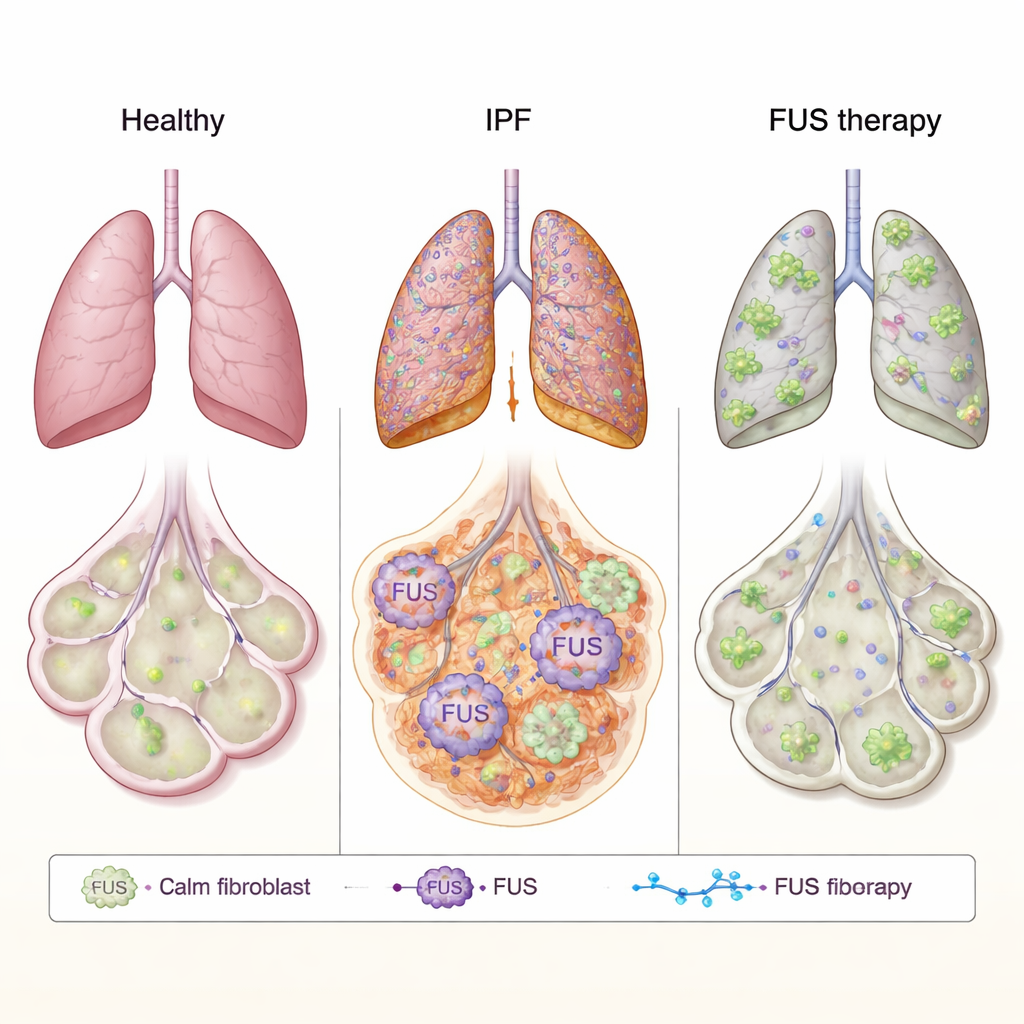
Hoe FUS littekencellen aanjaagt
Om te onderzoeken wat dit zich misdragende eiwit werkelijk doet, verhoogden de onderzoekers FUS in gezonde fibroblasten en verminderden het in IPF-fibroblasten. Extra FUS zette gezonde cellen aan tot sneller delen, terwijl het verlagen van FUS in IPF-cellen hun groei en beweging vertraagde — twee gedragingen die centraal staan bij littekenvorming. Het team gebruikte vervolgens een techniek die eiwit–RNA-partnerschappen ‘vriest’ en uitleest welke RNA’s aan FUS gebonden zijn. In IPF-fibroblasten bleek FUS vast te zitten aan veel genetische boodschappen die fibrose bevorderen, waaronder die voor collageen, groeifactoren zoals TGF‑β en ontstekingssignalen. Met andere woorden, FUS fungeerde als een knooppunt dat een heel netwerk van pro-litteken boodschappen verbond.
Het signaal dempen met een precisiegeneesmiddel
De studie onderzocht een antisense-oligonucleotide genaamd ION363 — een korte, chemisch aangepaste streng die is ontworpen om zich aan FUS-RNA te binden en dat RNA af te breken. Wanneer IPF-fibroblasten werden behandeld met ION363, daalden de FUS-niveaus, vertraagden de cellen in proliferatie en migratie, en kregen belangrijke genen voor littekenopbouw minder expressie. Belangrijk was dat dit effect niet afhing van het doden van cellen of het afdwingen van veroudering; het leek hun gedrag te resetten. Wanneer dezelfde behandeling werd toegepast op dunne plakjes IPF-longweefsel dat in het laboratorium in leven werd gehouden, werden grote groepen genen die gekoppeld zijn aan de extracellulaire matrix, ontsteking en abnormale epitheliale bekleding naar beneden bijgesteld, terwijl genen die geassocieerd zijn met gezonde surfactantproductie en alveolaire functie omhoog gingen. De behandeling verminderde ook collageenkleuring en verhoogde markers van functionele longoppervlaktecellen, wat wijst op een verschuiving van littekenvorming naar herstel.
Helpen van beschadigde luchtzakjes bij het opnieuw aangroeien
Aangezien de kleine cellen die de luchtzakjes bekleden, bekend als type II alveolaire cellen, cruciaal zijn voor longherstel, bouwden de onderzoekers driedimensionale ‘alveolosferen’ uit patiëntcellen om miniatuur longeenheden na te bootsen. In kweek van IPF-patiënten overleven deze structuren normaal slecht. Met ION363-behandeling vormden meer alveolosferen, groeiden ze groter en toonden ze een hogere lysosomale activiteit — een kenmerk van actieve vernieuwing. Gedetailleerde kleuring liet meer cellen zien die markers droegen van rijpe gasuitwisselende cellen, wat aangeeft dat het stilleggen van FUS niet alleen fibroblasten kalmeerde maar ook het beschadigde epitheel aanmoedigde om een gezondere oppervlakte te herbouwen. 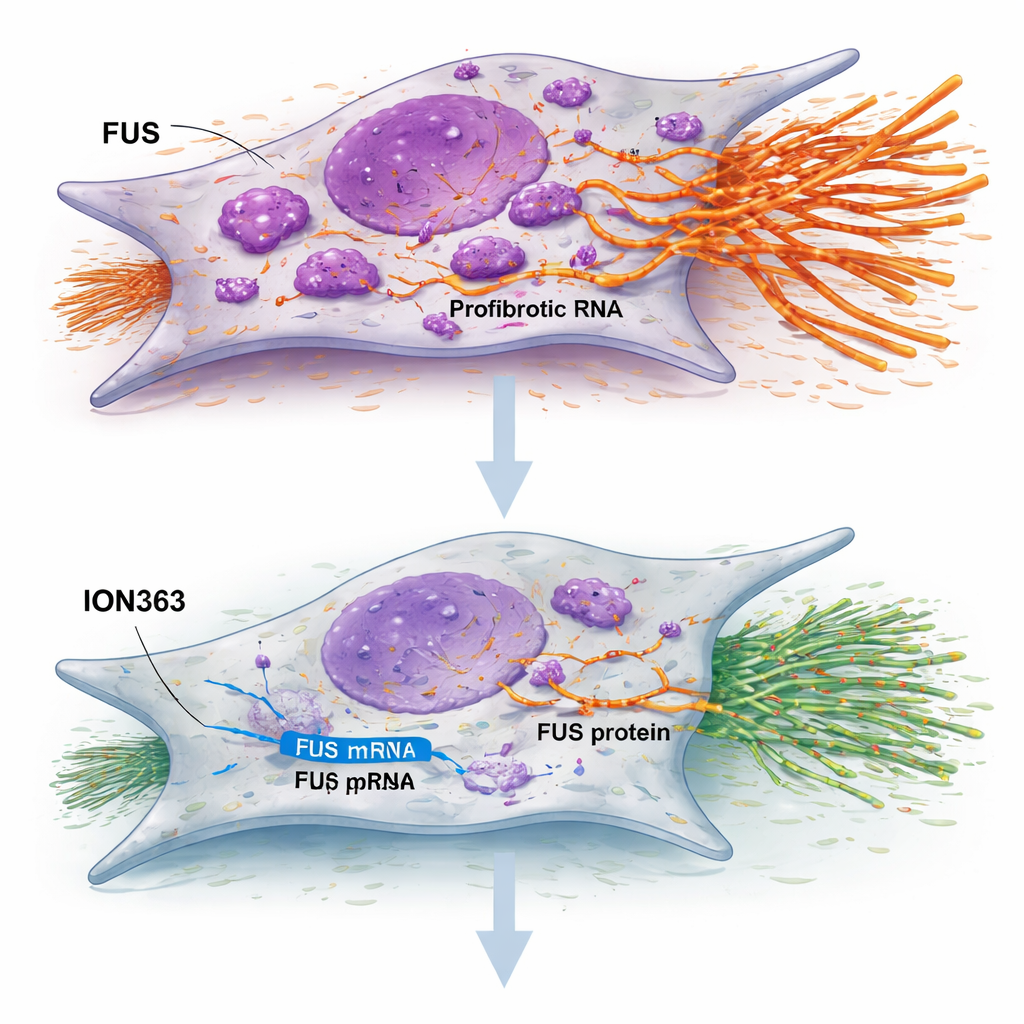
Wat dit voor patiënten zou kunnen betekenen
Alles bij elkaar schetst het werk FUS als een schakelpunt in IPF dat overactieve, littekenvormende fibroblasten verbindt met falend herstel van de fijne luchtzakjes. Door FUS met een gericht antisensemiddel te verlagen, konden de onderzoekers profibrotische genprogramma’s verminderen, collageenophoping verminderen en regeneratie bevorderen in patiëntafgeleide longmodellen. Hoewel deze benadering nog in het laboratoriumstadium verkeert en zorgvuldige testen in diermodellen en klinische proeven zal vereisen, suggereert het dat IPF ooit mogelijk niet alleen behandeld kan worden door littekenvorming te vertragen, maar door de cellulaire programma’s die longschade en herstel regelen direct te herevenwichten.
Bronvermelding: Katariya, B.B., Chillappagari, S., Arnold, L. et al. Targeting fused in sarcoma (FUS): a novel antisense strategy for treating idiopathic pulmonary fibrosis. Sig Transduct Target Ther 11, 70 (2026). https://doi.org/10.1038/s41392-026-02585-9
Trefwoorden: idiopathische pulmonale fibrose, antisense-oligonucleotide, FUS-eiwit, longfibrose, alveolaire reparatie