Clear Sky Science · nl
Gedeeltelijke truncatie van de C-terminus van PTCH1 in kanker bevordert tumorgenese via niet-canonische activatie van een GLI-PI3K lus
Waarom een kleine eiwitverandering belangrijk is bij dikkedarmkanker
Dikkedarmkanker ontstaat meestal door een geleidelijke ophoping van genetische fouten. Deze studie zoomt in op een verrassend kleine verandering in een celmembraaneiwit genaamd PTCH1 en laat zien hoe het afknippen van een deel van zijn staart kan helpen dat kankercellen sneller groeien, zich gemakkelijker verspreiden en mogelijk weerstand ontwikkelen tegen sommige bestaande geneesmiddelen. Het begrijpen van deze verborgen groeischakelaar kan de weg openen naar nieuwe, meer gerichte behandelingen voor een deel van de patiënten.
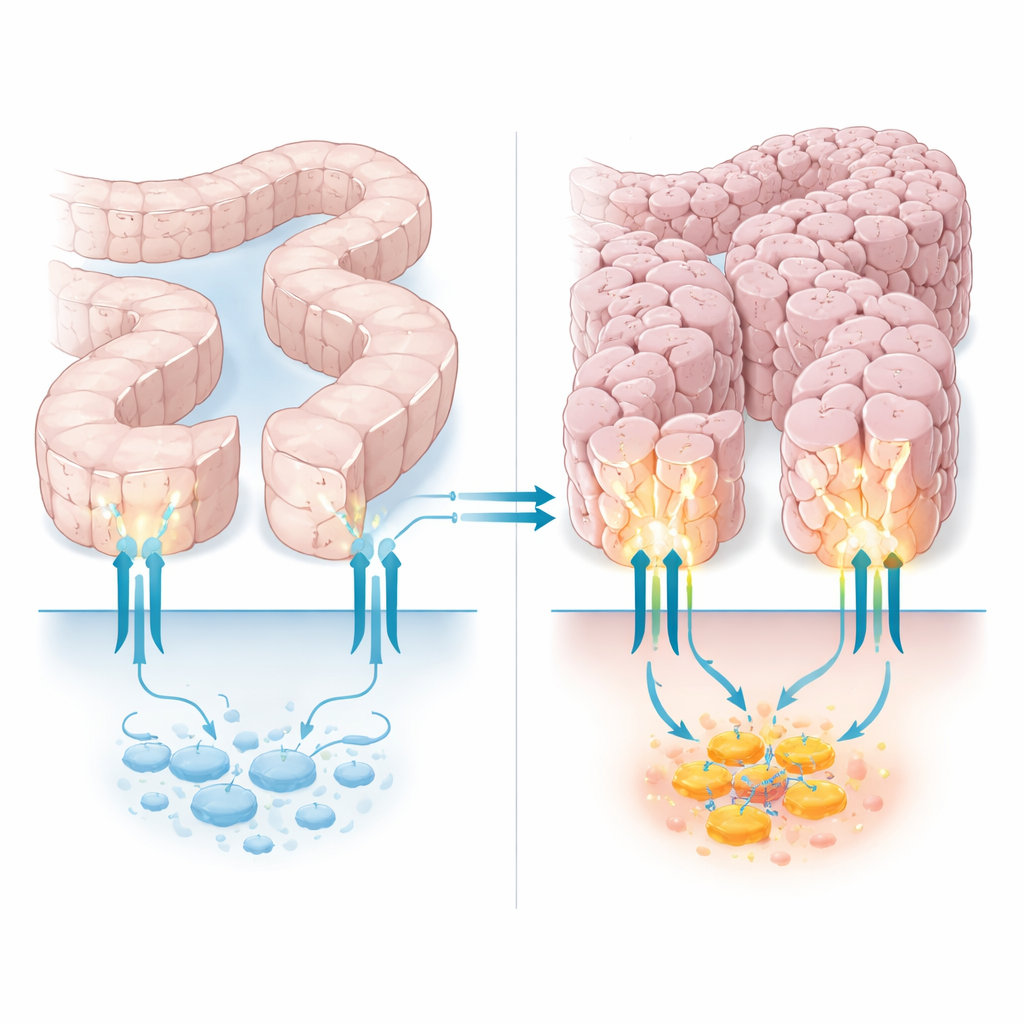
De poortwachter van de cel met een verborgen neventaak
PTCH1 is vooral bekend als de poortwachter van het Hedgehog-pad, een communicatielijn die cellen gebruiken tijdens ontwikkeling en weefselherstel. In zijn klassieke rol houdt PTCH1 een partner-eiwit, Smoothened, onder controle en reguleert daarmee een familie van DNA-regelaars genaamd GLI. Maar PTCH1 heeft ook een lange, slappe staart die binnenin de cel hangt en dienstdoet als aanmeerstrook voor andere eiwitten die invloed hebben op celdood, recycling van cellulaire componenten en meer. Eerder werk toonde aan dat sommige colon-, maag- en baarmoederkankers mutaties dragen die een deel van deze interne staart afknippen. Die mutaties leken de klassieke Hedgehog-schakelaar niet te verbreken, maar maakten kankercellen beter bestand tegen stress, wat suggereert dat dit staartsegment stilletjes bijdraagt aan PTCH1’s tumorrepressieve rol.
Het ontwerpen van kankercellen om het effect te testen
Om te zien wat deze staart-verkortende mutaties werkelijk doen, gebruikten de onderzoekers CRISPR/Cas9-genbewerking om ze na te bootsen in een dikkedarmkankercellijn. Ze vergeleken twee bewerkte klonen, elk met een andere truncatie in de PTCH1-staart, met anderszins identieke cellen met normaal PTCH1. De gemuteerde cellen deelden sneller, vormden veel meer kolonies en gedijden zelfs wanneer ze zonder hechting moesten groeien — een gedrag dat verband houdt met het vermogen zich in het lichaam te verspreiden. Wanneer ze in muizen werden geïmplanteerd, produceerden de staart-gemuteerde cellen in enkele weken veel grotere tumoren, met meer cellen die zich actief aan het delen waren. Belangrijk is dat de bewerkte cellen nog steeds PTCH1 produceerden en zijn hoofdpoortwachtersfunctie behielden, wat aangeeft dat de extra agressiviteit voortkomt uit het verlies van de gespecialiseerde interne taken van de staart, en niet uit het eenvoudigweg verwijderen van PTCH1.
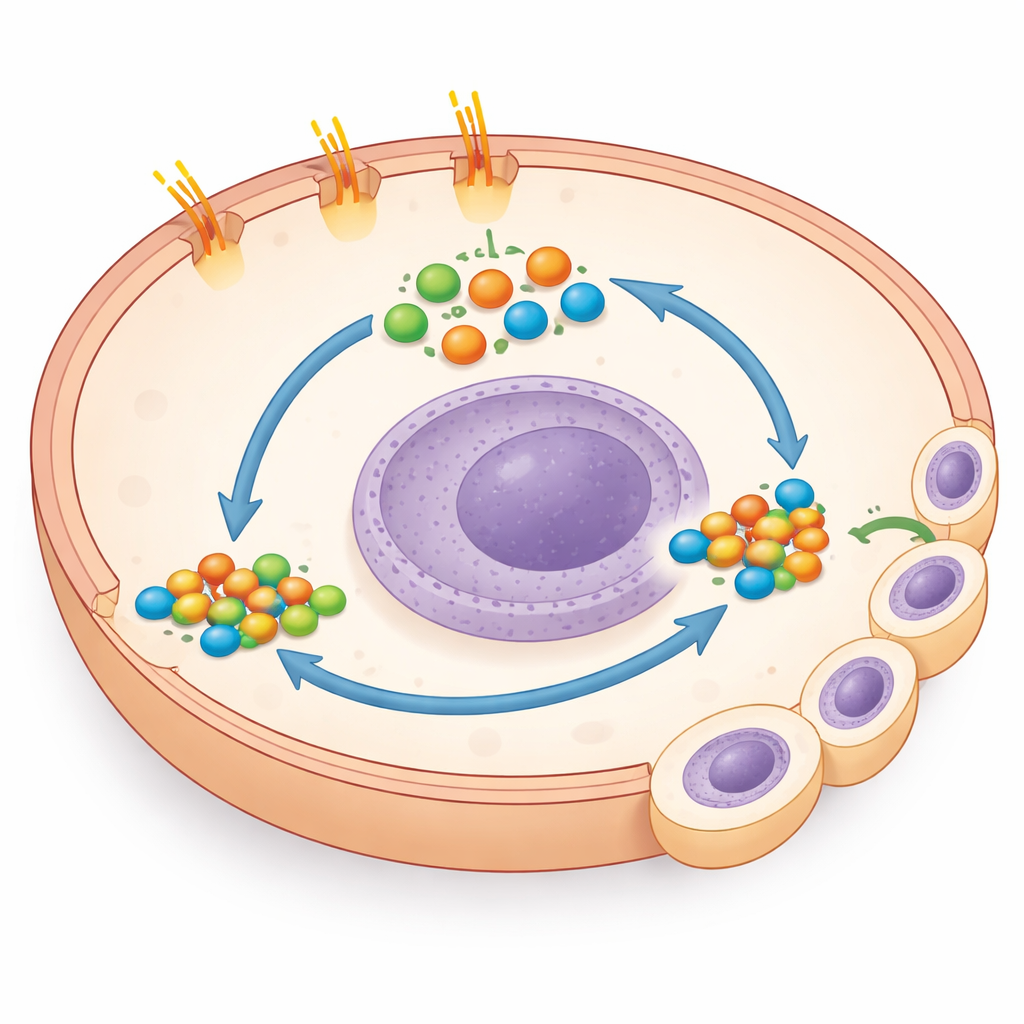
Een verrassende omweg naar een krachtige groeischakel
Bij nader onderzoek ontdekten de onderzoekers iets onverwachts: de staart-getrunceerde cellen hadden sterk verhoogde niveaus van GLI1 en GLI2, sleutelstuurders van genprogramma’s die groei en overleving bevorderen. Normaal gesproken stijgt GLI-activiteit wanneer Smoothened wordt vrijgegeven, maar het blokkeren van Smoothened had hier geen effect. In plaats daarvan verminderde directe blokkade van GLI met een klein molecuul, of het verlagen van GLI1 met genetische middelen, de groei van de gemuteerde cellen in kweekschalen sterk en in aanvullende dikkedarmkankercellijnen die van nature PTCH1-staartmutaties dragen. Dit toonde aan dat het verlies van de staart GLI activeert via een “niet-canonische” route die de gebruikelijke Hedgehog-schakelaar omzeilt, en dat de kankercellen sterk afhankelijk worden van deze omweg voor hun agressieve gedrag.
Meerdere groeicircuiten worden geactiveerd, maar één lus domineert
Door het RNA van de cellen te sequencen, vonden de onderzoekers duizenden genen waarvan de activiteit veranderde toen de PTCH1-staart werd getruncateerd. Veel behoorden tot bekende kankercircuits, waaronder die gecontroleerd door de epidermale groei-factorreceptor (EGFR), Ras, en signaalroutes die de celmetabolisme en initiatief-eigenschappen reguleren. De gemuteerde cellen vertoonden verhoogde activiteit van EGFR en zijn liganden en hogere activiteit in twee belangrijke downstreamroutes: de MAPK- en PI3K/Akt-paden. Toch vertraagden de gemuteerde cellen slechts gedeeltelijk wanneer de wetenschappers EGFR of zijn MAPK-tak blokkeerden. Daarentegen remden lage doses PI3K-remmers hun groei en kolonieformatie sterk en verlaagden ze GLI1-niveaus, wat PI3K/Akt benadrukt als een cruciale partner in dit nieuwe GLI-activerende mechanisme.
Een zelfversterkende lus die tumorgroei aandrijft
Verdere experimenten onthulden een terugkoppelingscyclus: het trunceren van de PTCH1-staart verhoogt GLI-activiteit; GLI helpt op zijn beurt PI3K/Akt-signaal hoog te houden; en PI3K/Akt helpt GLI te stabiliseren en te activeren. Het verstoren van ofwel GLI of PI3K verbrak deze lus en ontnam de gemuteerde cellen hun groeivoordeel, terwijl het simpelweg opdrijven van PI3K/Akt de directe GLI-blokkade niet kon overwinnen. De cellen toonden ook gereduceerde activiteit van PKA, een enzym dat normaal GLI-eiwitten markeert voor inactivatie, wat waarschijnlijk de balans verder in het voordeel van GLI-gedreven programma’s kantelt.
Wat dit kan betekenen voor toekomstige behandeling
Voor patiënten is de kernboodschap dat sommige dikkedarmkankers PTCH1-staartmutaties dragen die stilletjes een GLI–PI3K positieve feedbacklus bedraad, waardoor tumoren groeien en ontsnappen aan geneesmiddelen die de meer bekende Hedgehog-schakelaar of de EGFR–MAPK-route targeten. Deze tumoren kunnen in plaats daarvan bijzonder kwetsbaar zijn voor behandelingen die GLI direct uitschakelen of PI3K/Akt remmen. Het werk suggereert dat het sequentiëren van PTCH1 in colon tumoren — vooral die uit het rechterdeel van de dikke darm, waar dergelijke mutaties vaker voorkomen — kan helpen patiënten te identificeren die baat zouden kunnen hebben bij PI3K- of GLI-gerichte strategieën, en zo een subtiel eiwitknipje omzetten in een nuttige therapeutische aanwijzing.
Bronvermelding: Caballero-Ruiz, B., Bordone, R., Coni, S. et al. Partial truncation of the C-terminal domain of PTCH1 in cancer promotes tumourigenesis by non-canonical activation of a GLI-PI3K loop. Oncogene 45, 1013–1025 (2026). https://doi.org/10.1038/s41388-026-03698-9
Trefwoorden: dikkedarmkanker, Hedgehog-signaaltransductie, PTCH1-mutaties, GLI-transcriptiefactoren, PI3K-Akt-pad