Clear Sky Science · ja
MYCおよびKRASの標的分解のためのヘテロビファンクショナルなプロテオミメティックポリマー
がんの最も手ごわいタンパク質を倒す新しい道具
MYCやKRASのような多くの強力ながん駆動タンパク質は、薬剤が容易に結合できないため長く「ドラッガブルでない」と言われてきました。本研究はHYDRACポリマーと呼ばれる新しいタイプの柔らかい合成材料を紹介します。これらは滑らかな標的タンパク質を把持し、細胞のゴミ処理システムへと送り込むことができます。本稿は、化学とナノテクノロジーが従来の薬が効きにくかったがんに対する治療の選択肢を拓く可能性を示しています。
単一の薬ではなく柔軟な足場
ほとんどの標的化がん薬は、小分子としてタンパク質表面のくぼみに合う鍵のように働きます。しかしMYCのように柔軟で良い結合ポケットを欠くタンパク質や、古典的薬剤を回避する変異を生じるKRASにはこの戦略が効きにくい。著者らは代わりに、繰り返し単位からなる長い鎖状のポリマーを設計しました。この鎖の上に、MYCやRASなどの標的を認識する短いタンパク質結合セグメントと、細胞の廃棄機構を呼び寄せる「デグロン」セグメントという二種類の構成要素を付加します。同じ鎖に多数コピーが並ぶため、単一のHYDRAC分子が複数のタンパク質や酵素に同時にアクセスでき、剛直な単一分子薬では達成しにくい働きが可能になります。
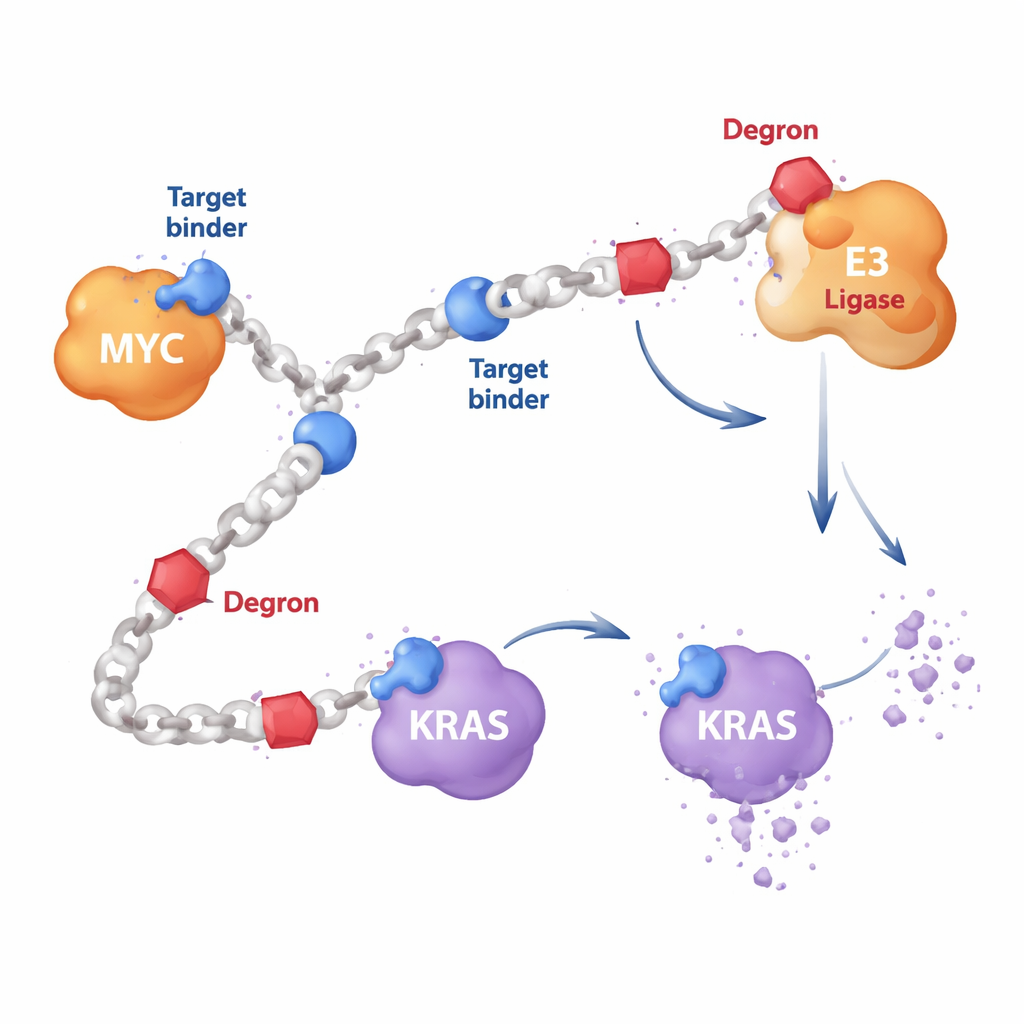
細胞にMYCを分解させる教え方
最初の試験として研究者たちは、長年直接攻撃が難しかった増殖のマスター因子MYCに着目しました。彼らは既知のMYC結合ペプチドと、細胞の主要なタンパク質粉砕装置であるプロテアソームによる分解の目印となる単純なデグロンモチーフを並べたHYDRACポリマーを構築しました。試験管内実験では、これらのポリマーはコンパクトでタンパク質様の形に折りたたまれ、非関連タンパク質には結合せずMYCに強く結合しました。がん細胞ではHYDRACが細胞内に入り込み、MYC制御の遺伝子プログラムを撹乱して細胞死を誘導しました。その効果は、標的化とデグロンの両方が同じポリマー鎖上に存在することに依存していました。
細胞培養から腫瘍縮小へ
細胞内でHYDRAC処理はMYCタンパク質量を鋭く低下させたが、MYCのRNA量は減らさず、単なる発現抑制ではなく実際の分解であることを示しました。プロテアソームや特定の分解経路を活性化する重要な酵素を阻害するとMYC量は回復し、これによりポリマーが細胞自身の廃棄機構を再配向して働くことが示されました。プロテオーム解析では非常に少数の他のタンパク質のみが影響を受けており、選択性の高さが示唆されます。MYC駆動腫瘍のマウスモデルでは、蛍光標識したHYDRACが注入後に腫瘍に優先的に蓄積し、数日間とどまりました。反復投与は体重減少や明らかな組織損傷を伴わずに腫瘍成長を遅らせ、腫瘍試料では分裂細胞の減少とプログラム細胞死の指標の増加が見られました。
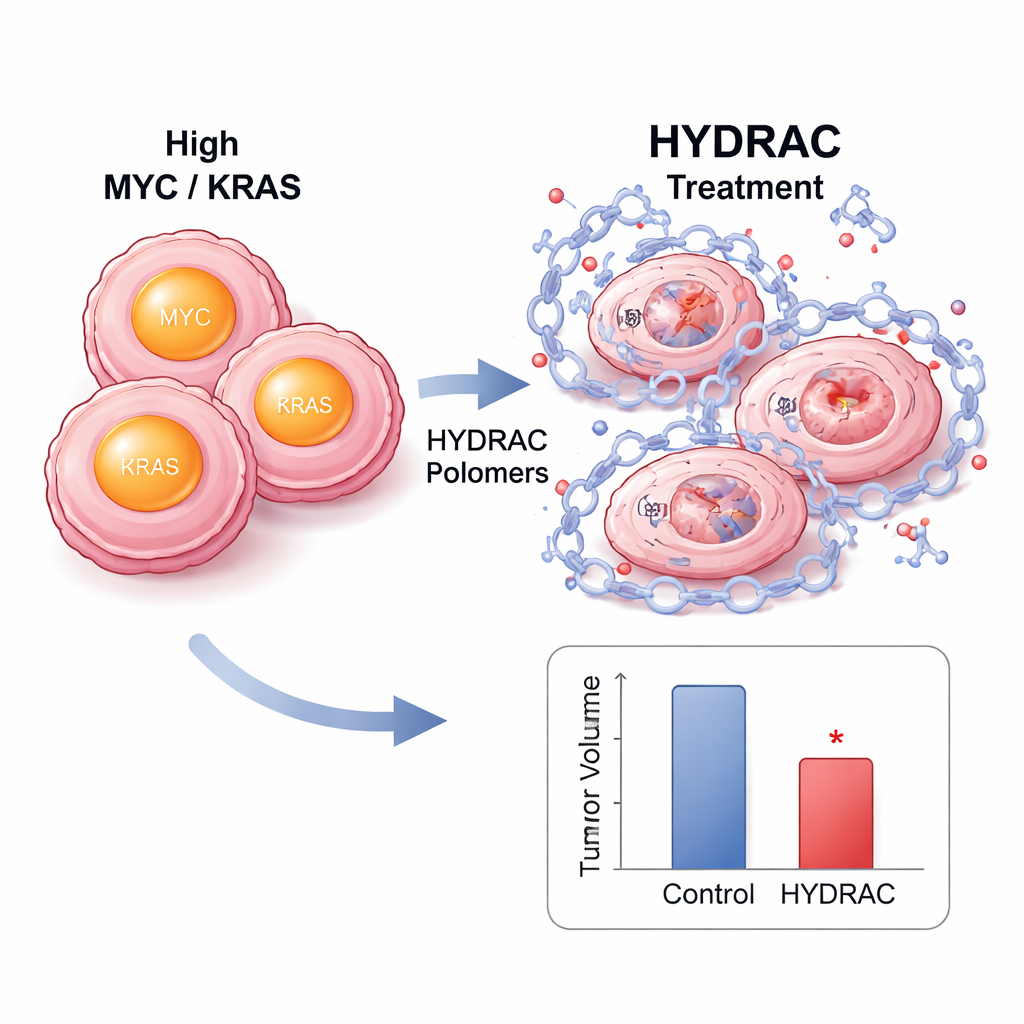
多くの疾患標的に使えるプラグ&プレイ式プラットフォーム
HYDRACアプローチの強みの一つは、側鎖を交換可能な部品のように差し替えられる点です。チームは当初のデグロンを、サリドマイドを認識するものを含むさまざまな細胞酵素を呼び寄せる他のリクルーターに置き換えました。各バージョンは、意図した酵素が存在し機能している場合にのみMYCを分解し、ポリマーが異なる細胞経路を使うように調整可能であることを確認しました。汎用性を試すために、研究者らはRASタンパク質を認識するペプチドを用いたRAS標的HYDRACも構築しました。これらは2つの異なるがん細胞株で変異型KRASを効果的に分解し、特定の変異に依存しない「汎KRAS」可能性を示唆しました。これは多くのKRAS変異が共存するがんにとって重要な一歩です。
将来のがん医療にとっての意義
本研究は、HYDRACをトラブルメーカーなタンパク質を単に阻害するのではなく、細胞がそれらを消去する手助けをするプログラム可能な材料の新しいクラスとして提示します。柔軟なポリマー上に多くの標的化ユニットと分解ユニットを組み合わせることで、HYDRACは従来の小分子薬やPROTACが抱える設計上の制約、すなわち通常それぞれを一つしか担えないという限界を回避します。臨床応用に至るまでには多くの課題が残りますが、MYCおよびKRAS駆動モデルでの結果は、長く“ドラッガブルでない”と考えられてきたがんタンパク質が、医療が単一の小さな錠剤ではなく、分子を織り上げたようなブラシ状の設計を目指すときに脆弱になり得ることを示唆しています。
引用: Wang, M.M., Truica, M.I., Gattis, B.S. et al. Heterobifunctional proteomimetic polymers for targeted degradation of MYC and KRAS. Nat Commun 17, 1706 (2026). https://doi.org/10.1038/s41467-026-68913-3
キーワード: 標的タンパク質分解, MYC, KRAS, ポリマーベースの治療薬, がんナノ医療