Clear Sky Science · ja
ヒト亜鉛活性化チャネル(ZAC)シグナリングと調節の構造基礎
微量金属が神経細胞の会話を助ける仕組み
亜鉛はマルチビタミン錠の栄養素としてよく知られていますが、体内ではこの金属が脳で速い化学的メッセージ伝達子としても働きます。本研究は、あまり知られていないタンパク質である亜鉛活性化チャネル(ZAC)が細胞外の亜鉛をどのように検出し、その信号を電気的応答に変換するかを原子分解能で明らかにしています。細胞膜上にあるこの特別なゲートを理解することは、亜鉛が脳活動に与える影響を解明し、健康や病気における神経信号の微調整につながる可能性があります。
亜鉛シグナルのための特別なゲート
神経細胞間の多くの迅速なメッセージは、セロトニンやアセチルコリンのような馴染みのある化学物質によって運ばれ、これらは細胞膜にリング状のチャネルを開きます。ZACはこれら受容体の遠い親戚にあたりますが、有機分子に応答する代わりに、亜鉛、銅、プロトンのような金属イオンによってスイッチが入ります。ZACは脳を含む多くのヒト組織に存在しますが、マウスやラットのような標準的な実験動物には存在しないため研究の進展が遅れてきました。本研究では高分解能のクライオ電子顕微鏡を用いて、ヒトZACの複数の三次元スナップショットを捕らえています:安定状態、亜鉛結合状態、およびチャネルを閉じる2種類の薬物と結合した状態です。これらの構造を合わせて調べることで、亜鉛がチャネルの上部にどのように結着するか、イオンがどのように通過するか、そして遮断剤がどのようにゲートを固く閉じるか、あるいは導通しない状態でこじ開けるかが明らかになりました。
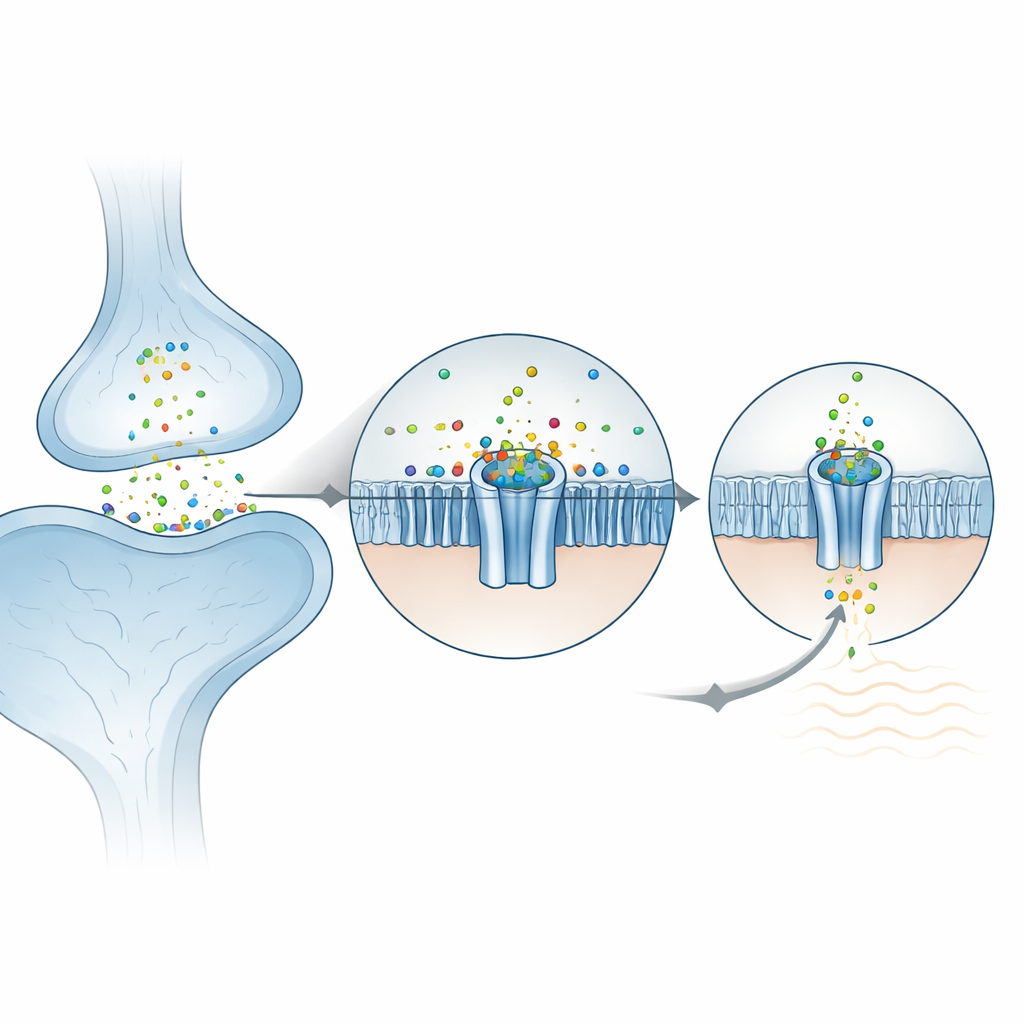
亜鉛がチャネルにロックインする仕組み
細胞外表面で、ZACは5つの同一サブユニットから成るロゼット状の構造をとります。研究者たちは、亜鉛イオンが5つの等価なポケットに落ち着くことを見出しました。これらのポケットは外部ドメインで隣接する二つのサブユニットの間に位置します。驚くべきことに、亜鉛は通常金属を結合する「掴み手」のようなアミノ酸(ヒスチジンやシステインなど)によって保持されているわけではありません。代わりに、主に二つの環状の芳香族側鎖によって受け止められ、いわゆるカチオン–π相互作用を通じて正に帯電したイオンを安定化しています。これらの重要残基をカエル卵母細胞での電気記録実験で変異させると、チャネルは亜鉛に反応しなくなり、これらの残基が中心的役割を果たしていることが確認されました。周囲の環境はすでに事前配列化されており、このことはZACが亜鉛なしでも顕著な自発活性を示す理由の一端を説明します:タンパク質は閉状態と開状態の境目に近い位置にあり、亜鉛は単にその均衡を後押しするのです。
イオンの通り道と一般的な遺伝子変異
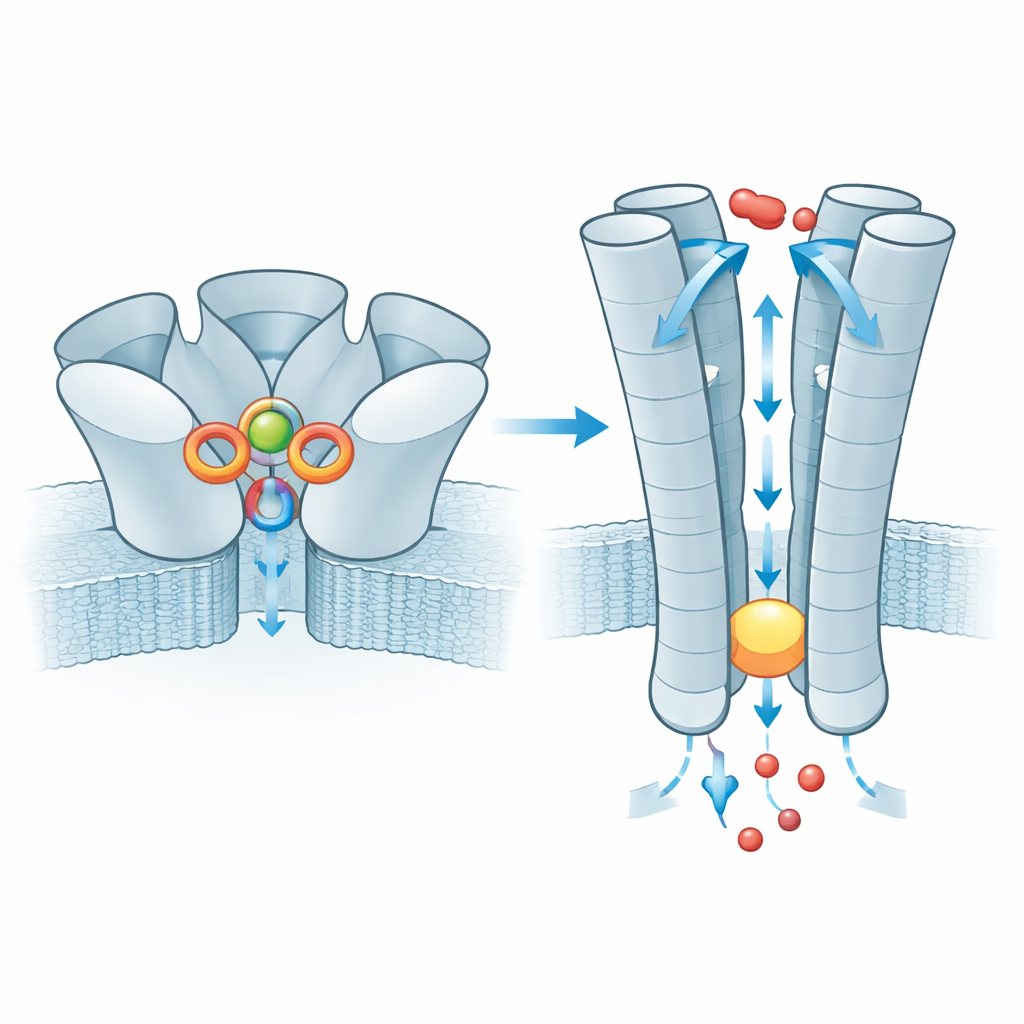
亜鉛が結合すると、その効果は膜貫通部に伝わり、そこでは5本の内側ヘリックスが孔を形成します。安定状態では、この管は一列のロイシン残基で狭窄し、疎水性のプラグを作ってイオンの移動を遮断します。亜鉛が結合すると、プラグはわずかに広がり、ナトリウムやカリウムのような小さな陽イオンが通り抜けられるようになります。一方で、孔の帯電した内面がこれらのイオンの選択性を助けます。チームはまた、プラグの上にある短い鎖で一つのアミノ酸(スレオニン)がアラニンに置換された非常に一般的なヒトの変異体も調べました。この小さな変化は隣接サブユニット間の相互作用ネットワークを弱め、通常は亜鉛結合の情報をゲートに伝える役割を担っています。電気的測定では、この変異体から構成されるチャネルははるかに小さな電流しか伝導しないことが示されました。したがってこの変異体は信号変換の効率が低い働きをしますが、そのヒトの生理学への影響はまだ不明です。
二つの薬物がチャネルを沈黙させる仕組み
亜鉛に加えて、本研究は二つの拮抗薬、TTFBとd-チュボクラリン(d‑TC)がどのようにZACを遮断するかも探っています。TTFBは設計された小分子で、膜領域の深部に入り込み、ゲートのすぐ上で二つの孔形成ヘリックスの間に滑り込みます。そこではぴったり合う疎水性ポケットや近くの極性残基と相互作用し、ヘリックスが完全に開いて導通状態になるための移動を抑える足場のように働きます。一方、かつて筋弛緩剤として用いられた古い薬剤であるd‑TCはより広範に作用します。1分子のd‑TCは通常亜鉛が宿る外部ポケットに結合し、亜鉛の正の電荷を模倣しつつ本物の亜鉛が正しく結合するのを妨げます。もう1分子のd‑TCは孔の入り口に位置し、物理的にトンネルを塞ぎます。これらの結合が共同で働くことで、ZACはタンパク質の形状が比較的開いたままの、脱感作された非導通の立体配座に閉じ込められます。
亜鉛と健康に関する発見の意義
この構造学的研究は、ZACが真の亜鉛センサーであり、他のファミリーメンバーが神経伝達物質を結合するのと同じ種類の部位で、異例の芳香族クレードル(受け皿)を用いて金属を検出していることを分子レベルで明確に示しています。また、チャネルの開閉のしやすさを調整する特定の相互作用ネットワークを同定し、ゲートを楔で閉じるか孔を詰めるかのいずれかの作用をする二つの異なる薬物結合部位を地図化しました。非専門家向けの要点は、亜鉛が単なる静的な栄養素ではなく能動的なシグナルであり、ZACがその専用の受容体のひとつであるということです。研究者たちがヒト体内や亜鉛不均衡に関連する神経疾患におけるZACの役割を探るにあたり、これらの原子レベルの設計図は、このチャネルをより精密に調節する分子を設計し、潜在的には障害された亜鉛シグナル伝達を修正するためのロードマップを提供します。
引用: Zhou, Z., Long, Y., Chao, Y. et al. Structural basis of human zinc-activated channel (ZAC) signaling and modulation. Cell Discov 12, 23 (2026). https://doi.org/10.1038/s41421-026-00878-5
キーワード: 亜鉛シグナル伝達, リガンド開口性イオンチャネル, 神経科学, クライオ電子顕微鏡構造, チャネル調節