Clear Sky Science · ja
補体受容体5a 2型はPSS–MFN2相互作用を介したミトコンドリア関連小胞体膜形成を促進して糖尿病性腎症を抑制する
この腎臓研究が重要な理由
糖尿病性腎症は、糖尿病患者が透析や移植を必要とする最も一般的な原因の一つであり、現在の治療は主に進行を遅らせるにとどまります。本研究は、糖や脂肪の有害な組合せに直面したときに腎細胞が備える予期せぬ自然の防御機構を明らかにします。あまり知られていない免疫受容体C5aR2が、腎細胞のエネルギー生産装置や脂質の取り扱いを守る仕組みを示すことで、免疫系を完全に遮断せずに腎臓を保護する新しいタイプの薬剤の可能性を示唆します。
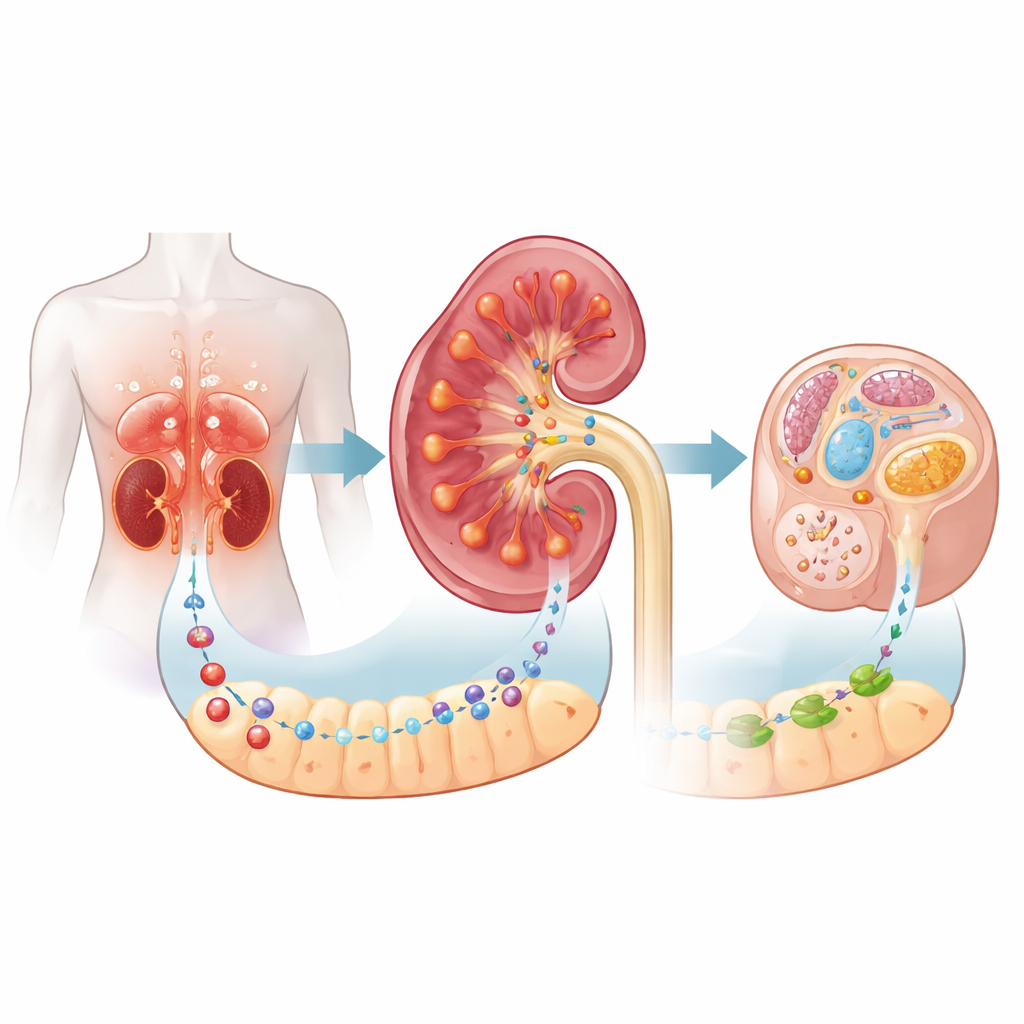
糖尿病腎に現れた意外な守護者
研究者らは、長期にわたる高血糖と代謝の乱れにさらされることで腎臓の微小構造が徐々に瘢痕化し機能不全に陥る糖尿病性腎症に着目しました。患者の腎生検を調べると、C5aR2と呼ばれる受容体が糸球体の間の間質組織で強く増加しており、特に栄養素を再吸収する近位尿細管細胞で顕著でした。C5aR2の増加は病状の悪化や腎不全への進行リスクと相関しており、損傷が蓄積するにつれてこの受容体の活動が高まることを示唆します。興味深いことに、これまでC5aR2は主に“デコイ”的な免疫受容体として扱われることが多かったが、本論文は細胞代謝においても重要な役割を果たすことを示しています。
守り手がいなくなると損傷が進む
C5aR2が味方か敵かを検証するために、研究チームはC5ar2遺伝子を欠損させた糖尿病マウスを用いました。受容体を持つ糖尿病マウスと比べると、ノックアウトマウスは尿中タンパクの喪失がより重く、腎組織の瘢痕化と炎症が増加し、顕微鏡で観察される構造的損傷も大きくなっていました。彼らの尿細管細胞は脂滴で詰まり、小胞体(タンパク質の折りたたみと梱包を担う器官)に強いストレス兆候を示し、膨張して機能不良になったミトコンドリアを有していました。C5aR2をサイレンシングした培養腎細胞でも同様の問題が現れ、ミトコンドリアの性能を直接示す酸素消費の低下が確認されました。これらの結果は、C5aR2が通常、尿細管細胞が糖尿病による代謝ストレスに耐えるのを助けていることを示しています。
小さな接触部位と重要な脂質が細胞を健康に保つ仕組み
さらに深入りすると、研究者らは腎臓の脂質プロファイルを解析し、C5aR2を欠くマウスで細胞膜の重要な構成要素であるホスファチジルセリンが著しく減少し、中性の貯蔵脂肪が増加していることを発見しました。ホスファチジルセリンは主に小胞体とミトコンドリアが接触する特殊な接合部、いわゆるミトコンドリア関連膜(MAM)で合成されます。これらの接触部位ではPSS1およびPSS2という酵素がホスファチジルセリンを合成し、MFN2というテンザタンパク質がそれをミトコンドリアへ渡すのを助けます。糖尿病マウスではこれらの接触ゾーンが既に短縮しており、C5aR2を除くとさらに縮み、接合部におけるPSS1、PSS2、MFN2の量が減少しました。細胞内では、C5aR2の活性化が転写因子c‑FOSを活性化し、それがPSS酵素の産生を増加させることが明らかになりました。さらにPSSタンパク質が物理的にMFN2に結合して機能的な橋を形成し、接触形成と脂質輸送の両方を支えていることを示しました。
欠けた連結を回復してストレス細胞を救う
この分子橋が実際に重要であることを証明するために、著者らは糖尿病マウスの腎尿細管細胞だけでPSS2の発現を人工的に増強しました。糖尿病は継続しているにもかかわらず、これらのマウスは尿中タンパク量の減少、瘢痕化の軽減、脂滴の減少、ミトコンドリアの形態と機能の改善、そしてミトコンドリアと小胞体間の接触ゾーンの延長を示しました。これら接合部でのホスファチジルセリン量も回復しました。培養細胞実験では、PSS2の増強がC5aR2が抑えられている場合でもエネルギー産生を回復し、脂肪蓄積を抑えたことから、PSS2がこの保護経路における重要な分岐点にあることが確認されました。
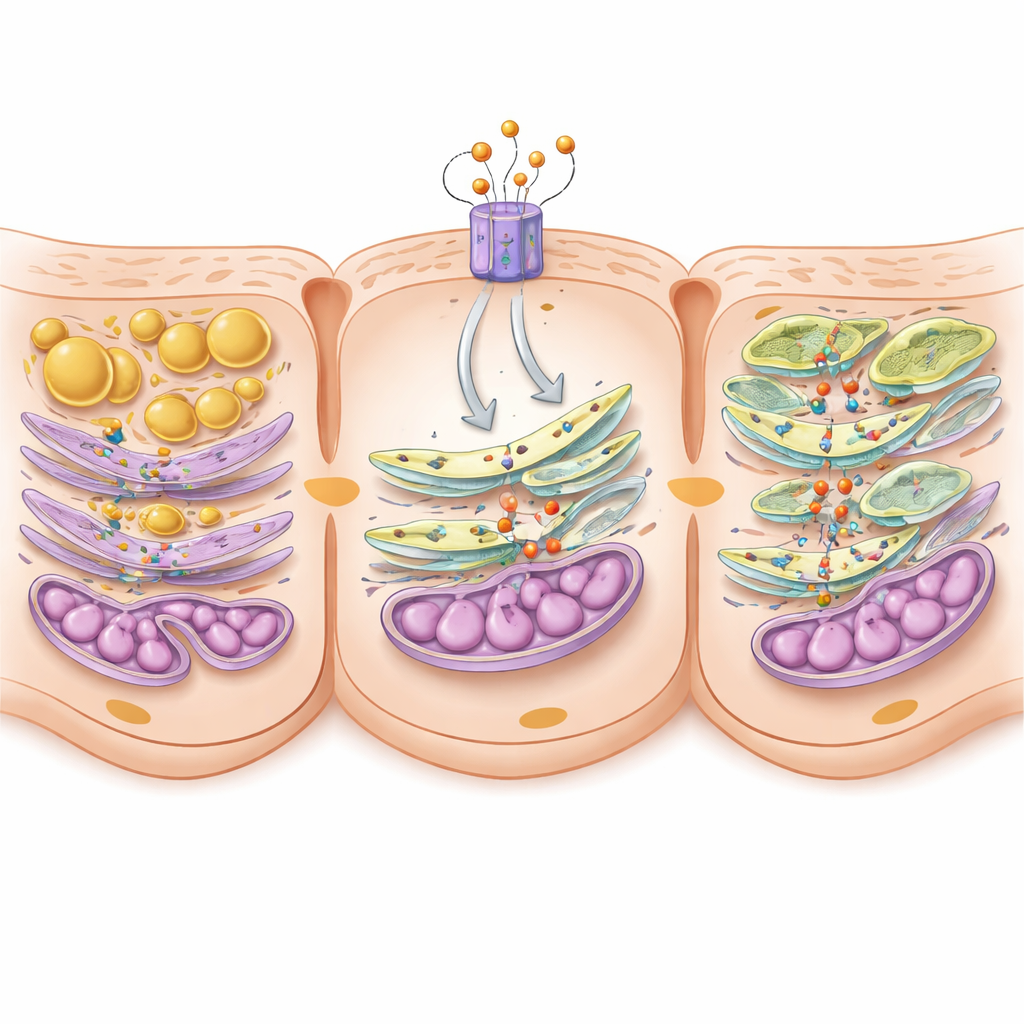
補体を遮断するのではなく調節する新しい薬理戦略
補体シグナルを完全に遮断すると宿主防御が損なわれる可能性があるため、研究者らはより選択的な戦術を検討しました:設計された小ペプチドP59でC5aR2を活性化することです。糖尿病性db/dbマウスに皮下投与で10週間与えたところ、体重と血中トリグリセリドが減少し、尿中タンパクの喪失が減り、間質の損傷が著しく改善しました。治療を受けたマウスの腎臓は脂質滴が少なく、小胞体ストレスが軽減され、ミトコンドリアは健全で、PSS1、PSS2、MFN2、ホスファチジルセリンに富むミトコンドリア関連膜が強化されていました。単一細胞RNAシーケンシングは、P59が障害を受けた近位尿細管細胞におけるPss2発現を特異的に回復させることを明らかにしました。培養腎細胞では、C5aR2またはPSS酵素をノックダウンするとP59の有益効果が消失し、その保護作用が新たに描かれたC5aR2–c‑FOS–PSS–MFN2軸を通ることを示しました。
糖尿病と共に暮らす人々にとっての意味
日常的な視点から見ると、本研究は糖尿病性ストレス下の腎臓がC5aR2をスイッチオンしてエネルギー系と脂質管理を維持しようとすることを示唆します。この受容体が欠如するか過負荷になると、細胞区画間の小さな接触部位が崩れ、重要な膜成分が不足し、脂質やストレスシグナルが蓄積して瘢痕化を促進します。標的を絞った薬剤でC5aR2を穏やかに刺激することで、これらの接触ブリッジを再構築し、より健全な脂質バランスを回復し、免疫系を広く抑制することなく腎機能を保護できる可能性があります。こうした治療が臨床に到達するまでには多くの作業が残されていますが、本研究は糖尿病患者の腎不全を遅らせる、あるいは予防するための有望な新たな道を開きます。
引用: Zhao, Yy., Wang, Yh., Li, Zh. et al. Complement 5a receptor 2 attenuates diabetic kidney disease by promoting mitochondria-associated endoplasmic reticulum membrane formation mediated by PSS-MFN2 interaction. Cell Discov 12, 24 (2026). https://doi.org/10.1038/s41421-026-00873-w
キーワード: 糖尿病性腎症, ミトコンドリア関連膜, 脂質代謝, 補体受容体 C5aR2, 近位尿細管細胞