Clear Sky Science · ja
JNK1–ZDHHC14軸が制御するASCT2のパルミトイル化はグルタミン代謝と非小細胞肺がんの進行を調整する
肺がんの炎を燃料補給する
増殖の速い多くの肺がんは、主要な燃料かつ構成要素である一般的なアミノ酸グルタミンに依存しています。本研究は、腫瘍細胞が表面の主要なグルタミン“ゲート”をどのように精密に調節しているか、そしてこの制御系を乱すことでがんの増殖を遅らせる可能性があることを明らかにします。この隠れた燃料弁を理解することで、なぜ一部の腫瘍が飢餓状態にしにくいのかが説明され、エネルギー供給をより効果的に断つ新しい薬剤併用の可能性が示されます。
グルタミンの細胞内への入り口
グルタミンは主にASCT2と呼ばれるトランスポータータンパク質を介して細胞内に取り込まれます。ASCT2は細胞外膜に位置し、グルタミンを細胞内に輸送します。非小細胞肺がん(NSCLC)は増殖や生存を支えるためにグルタミンに強く依存することが多く、腫瘍における高いASCT2発現は攻撃性の強い病状や患者予後不良と関連します。しかしASCT2自体は常に合成・翻訳後修飾・分解されており、どの時点でどれだけのゲートキーパーが細胞表面に残るかを決めるのは何かという疑問が残ります。
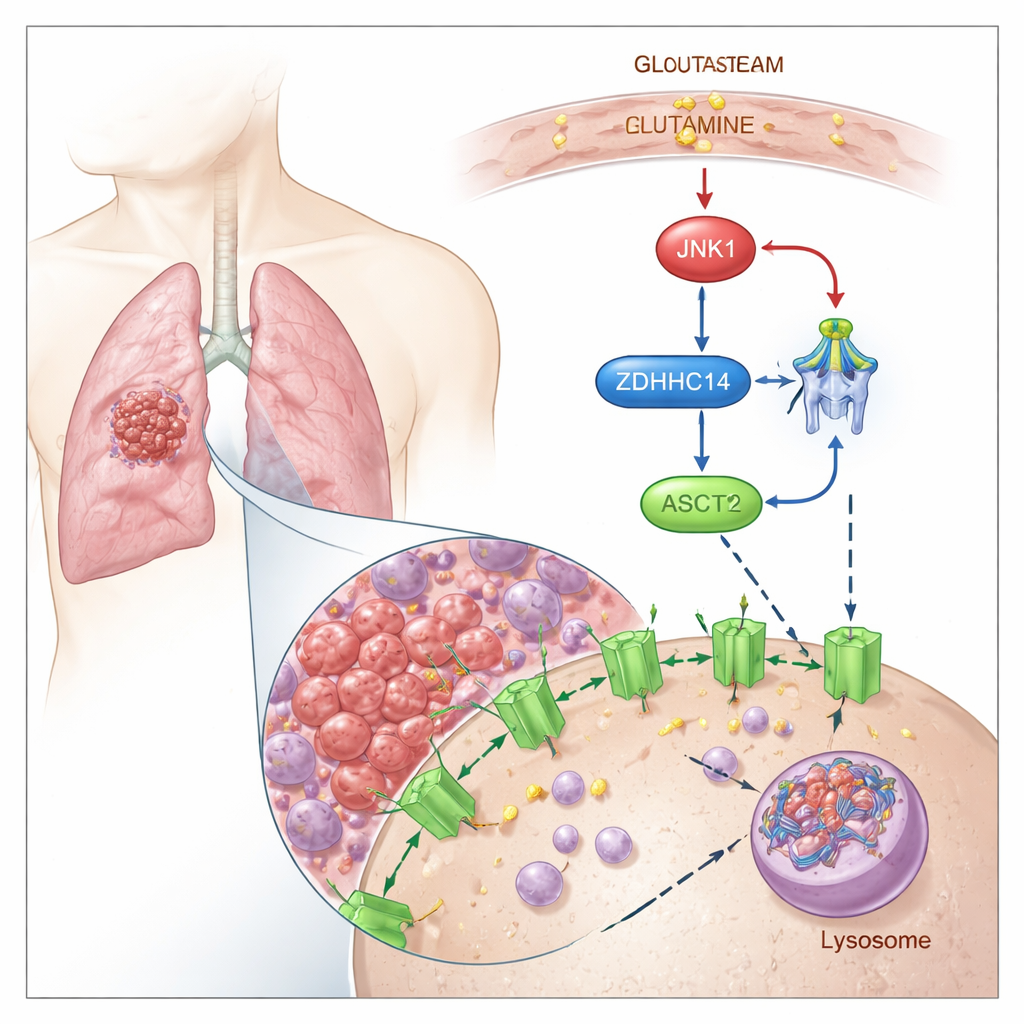
ASCT2を分解にタグ付けする仕組み
研究者らは、ASCT2がパルミトイル化と呼ばれる化学的“タグ”によって制御されることを示します。パルミトイル化では脂肪酸がタンパク質の特定のシステイン残基に付加されます。酵素ZDHHC14がASCT2の保存された二つの部位(Cys39およびCys48)にこの脂質タグを付けることを発見しました。タグが付くとASCT2は細胞表面からリソソームと呼ばれるリサイクル・分解装置へと経路が変えられ、分解されます。パルミトイル化を阻害するとASCT2はタグ付けと分解を受けず、基礎となる遺伝子発現は変わらないままASCT2タンパク質量が増え、グルタミン取り込みが増強されます。
ゲートを守る反対の酵素
ZDHHC14に対抗するのはABHD17Bという別の酵素で、ASCT2から脂質タグを除去します。ABHD17Bが活性化されるとASCT2のパルミトイル化は減り、安定化し、リソソームに送られるのではなく細胞表面に再巡回する可能性が高まります。この付加と除去の拮抗はグルタミン流入を微調整するダイヤルのように働きます。ZDHHC14はASCT2を分解へと押しやり、ABHD17Bはそれを救出してグルタミン輸送を維持します。肺がん細胞では、パルミトイル化を減らす方向にバランスが傾くとグルタミン取り込みが増え、培養やマウスでの腫瘍成長を支えます。
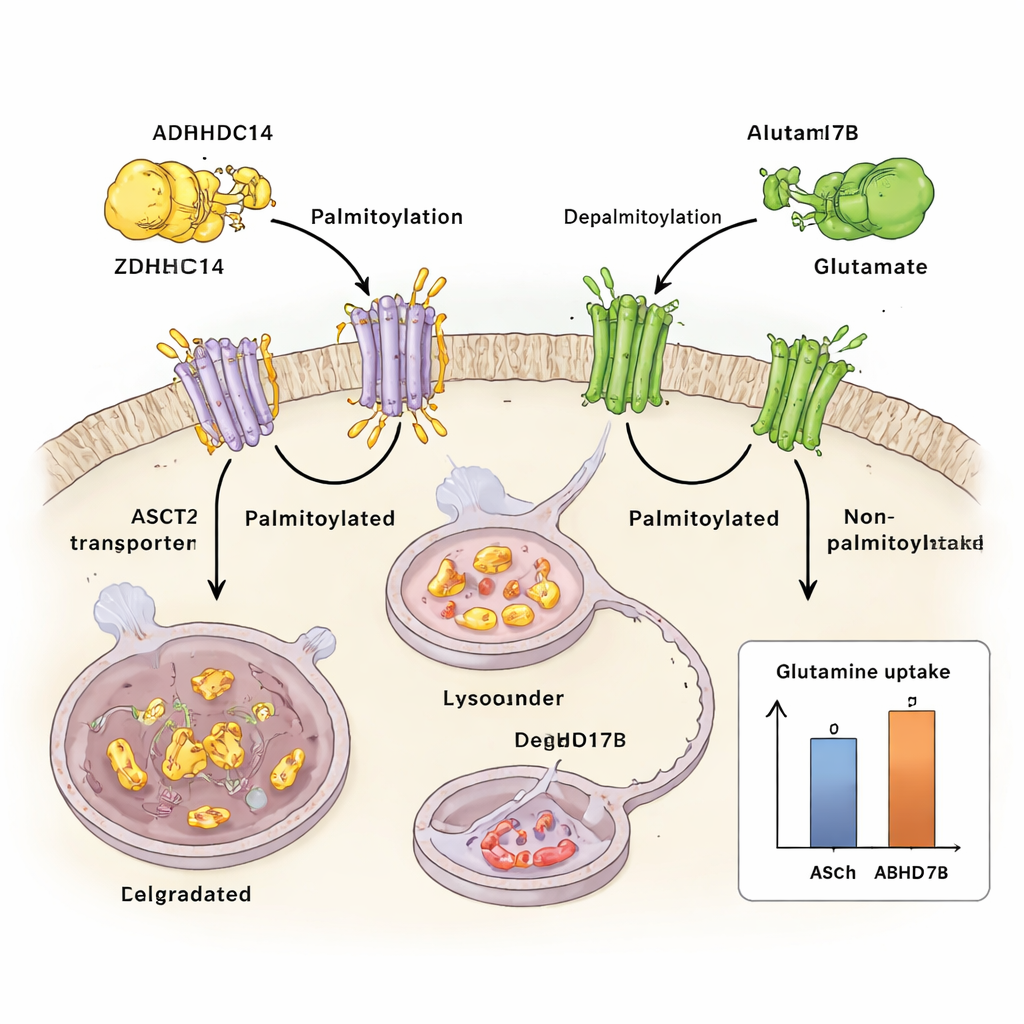
栄養ストレスが系をどのように書き換えるか
次に研究チームは腫瘍細胞がグルタミン不足になると何が起きるかを調べました。グルタミン欠乏下ではストレス感受性のシグナル伝達タンパク質JNK1が活性化します。JNK1はZDHHC14と物理的に結合し、特定の部位(Thr440)にリン酸基を付加してZDHHC14をリソソームによる分解の標的にします。ZDHHC14の量が減るとASCT2へのパルミトイル化タグは減り、分解を逃れて細胞表面に蓄積します。これは細胞が希少なグルタミンを効率的に取り込む必要があるときにちょうど起こります。JNK1感受性のこの単一部位を変異させるとZDHHC14が安定化してASCT2のタグ付けが回復し、グルタミン取り込みが減少することから、栄養ストレスがこの制御ループに密接に結び付いていることが示されます。
メカニズムを治療に結びつける
ASCT2は腫瘍代謝にとって重要であるため、実験的化合物V9302のようなASCT2を阻害する薬剤ががん治療として検討されています。本研究は、JNK1シグナルがASCT2の分解を阻むことでグルタミンゲートを保護し得ることを明らかにしました。NSCLCの細胞およびマウスモデルでは、JNK阻害剤とV9302を併用すると、いずれか単独よりもグルタミン取り込み、腫瘍細胞増殖、腫瘍体積がより強く抑制されました。患者検体と公開データベースの解析も、低ZDHHC14と高ASCT2の組み合わせがNSCLCに一般的であり、予後不良と関連することを示しており、この分子プロファイルがこの経路を標的とする患者の同定に役立つ可能性があります。
患者にとっての意味
日常語で言えば、本研究は一部の肺がんが表面の分子弁を調節して好む燃料をコントロールしていることを示しています。JNK1、ZDHHC14、ABHD17Bという三者が、グルタミンゲートであるASCT2を分解のためにタグ付けするか、それとも開いたまま維持するかを決めます。グルタミンが不足するとシステムはASCT2を保存して燃料供給を維持し、過酷な条件下で腫瘍が生き延びるのを助けます。ASCT2とそれを保護するJNK経路を同時に阻害することで、研究者らは培養および動物モデルでがん細胞をより効果的に飢えさせることができました。さらなる検証が必要ですが、このリン酸化–パルミトイル化軸は、グルタミンを多く消費する肺腫瘍の栄養供給を断つことを目指す治療の有望な新たな視点を提供します。
引用: Chen, X., Ke, Z., Wei, S. et al. ASCT2 palmitoylation regulated by JNK1-ZDHHC14 axis orchestrates glutamine metabolism and NSCLC progression. Cell Discov 12, 13 (2026). https://doi.org/10.1038/s41421-026-00870-z
キーワード: グルタミン代謝, 非小細胞肺がん, ASCT2トランスポーター, タンパク質のパルミトイル化, JNKシグナル伝達