Clear Sky Science · ja
HSP27の抑制はXBP1s/CerS1の相互作用を活性化し、DRP1駆動のミトファジーを誘導して細胞死を防ぎ、原発性滲出性リンパ腫細胞におけるKSHVの溶解期サイクルを促進する
細胞ストレスが二面性を帯びるとき
私たちの細胞は日々の損傷に対して、修復と生存を維持するための緊急プログラムを起動してやり過ごしています。しかしがん細胞は、これら同じ仕組みを乗っ取り、増殖や内部に潜むウイルスの保護に利用することがあります。本稿は、希少なリンパ腫において一つのストレス保護タンパク質を阻害することが、腫瘍細胞を死へと傾けるだけでなく、細胞内に潜むウイルスに覚醒と増殖の機会を与える仕組みを探ります。この微妙な均衡の理解は、ウイルスの拡散の余地を与えずにがんを葬る治療戦略の設計に役立ち得ます。
攻撃的なリンパ腫に潜む隠れたウイルス
原発性滲出性リンパ腫は、B細胞(白血球の一種)に起因する非常に攻撃的ながんです。これらの腫瘍細胞の多くは、休眠状態の同居者であるカポジ肉腫関連ヘルペスウイルス(KSHV)を抱えています。潜伏期にはウイルスはごく少数のタンパク質しか産生せず、宿主ゲノム内に隠れていますが、特定のストレスが加わると溶解期に移行し、自己複製と新しいウイルス粒子の生成を行い、通常は宿主細胞を死に至らしめます。腫瘍細胞自身は、誤った折り畳みタンパク質、脂質代謝の乱れ、エネルギー産生ミトコンドリアへの損傷に対処するために、熱ショックタンパク質や小胞体ストレス応答(UPR)など複数のストレス応答システムに依存しています。 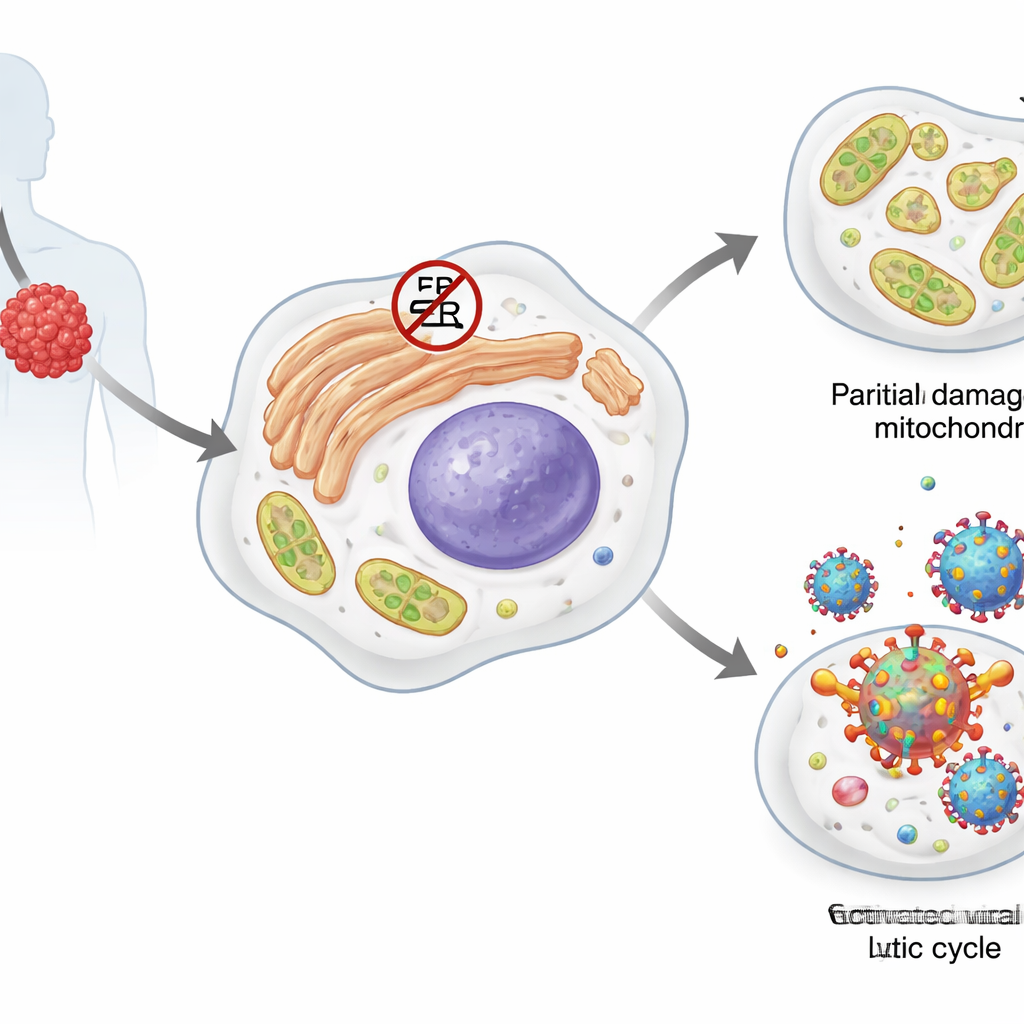
細胞の護衛を遮断する
研究者らは、ストレスから細胞を守ることで知られる小さな熱ショックタンパク質HSP27に着目しました。化学的阻害剤J2を用いるか、small RNAで遺伝子をサイレンシングすることで、培養リンパ腫細胞におけるHSP27活性を低下させました。その結果、細胞の生存率は下がり、小胞体と呼ばれる内部膜ネットワークで強いストレスシグナルが誘導されました。この応答のマーカー(保護因子や細胞死促進因子を含む)が上昇し、重要なスイッチであるXBP1sが活性化されました。同時に、プログラムされた細胞死の兆候も増え、HSP27を失うことが細胞を生存と死の瀬戸際へと押しやることが確認されました。
細胞脂質と対話するストレスループ
小胞体ストレスは細胞の脂質処理と密接に絡み合っています。研究チームは、HSP27を阻害すると特定の脂質分子であるC18セラミドを合成する酵素CerS1のレベルが上昇することを見出しました。XBP1sを化学的に阻害するとCerS1の増加が消えたため、これらの条件下でXBP1sがCerS1遺伝子の活性化を助けていることが示されました。興味深いことに、CerS1を阻害すると逆にXBP1sのレベルが下がり、両者が互いに支え合う正のフィードバックループが存在することが明らかになりました。この分子間のやり取りは脂質代謝を再構築するだけでなく、小胞体ストレスへの適応能力を強化しつつも、同時に細胞死のシグナルが蓄積する状況を生み出します。
破壊されるのではなく再生されるミトコンドリア
細胞のある部分でのストレスはしばしばミトコンドリアへ波及します。HSP27を阻害した後、リンパ腫細胞ではミトコンドリア障害の指標である活性酸素種が増加し、ミトコンドリアを小さく切断するタンパク質DRP1のレベルが上がりました。著者らはXBP1s–CerS1ループがDRP1を上昇させる原因であることを示しました。これが引き金となり、損傷したミトコンドリアが膜で包まれてリソソームという細胞の「リサイクルセンター」に運ばれる品質管理プロセス、ミトファジーが誘導されました。蛍光色素やタンパク質マーカーを用いてミトコンドリアが選択的に除去されていることを確認しました。化学的または遺伝学的にDRP1を阻害するとこのミトファジーは減少し、細胞はより容易に死んだため、ミトコンドリアの再循環がストレス下の腫瘍細胞の生存を実際に助けていることが示されました。 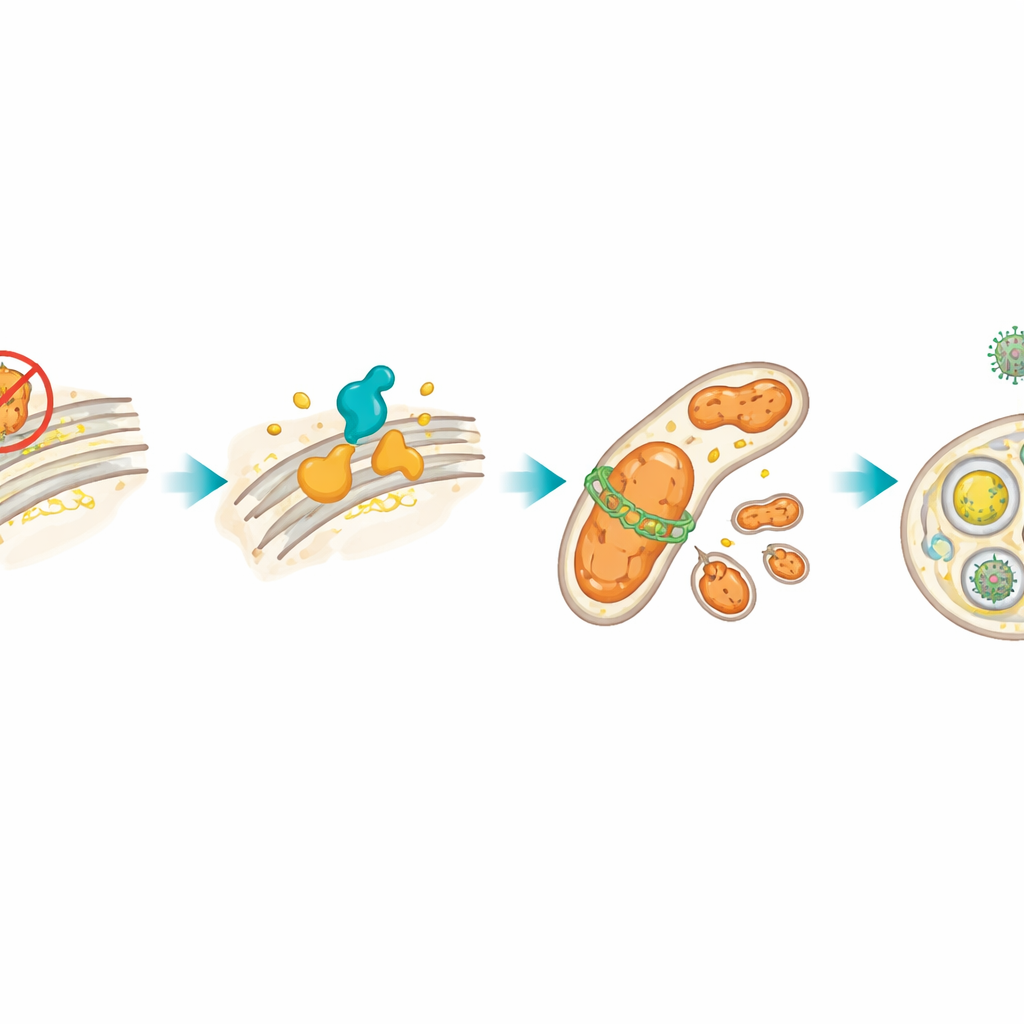
ウイルスに逃げる時間を与える
腫瘍細胞を保護する同じミトファジーはKSHVにも利益をもたらしました。XBP1sの活性化、C18セラミドの蓄積、増加したミトコンドリア分裂はいずれもこのウイルスの再活性化と関連しています。本研究ではHSP27を阻害すると、より多くの細胞が初期および晩期のウイルスタンパク質を発現し、溶解期複製の明確な兆候を示しました。DRP1、すなわちミトファジーを阻害するとこのウイルス再活性化は減少しました。著者らは、ミトファジーがストレス下で細胞生存をやや延長することで、KSHVに複製サイクルを完了して死にゆく細胞から脱出する時間を与え、新たな標的を感染させたり、がんの進展に寄与したりする可能性があると示唆しています。
今後の治療への示唆
非専門家に向けた要点は、HSP27がリンパ腫細胞のストレス対処、損傷ミトコンドリアの再循環、そしてがんに関連するウイルスがいつ覚醒するかを決める中心的な交通整理役として働く、ということです。HSP27の機能を止めると、一連の出来事が引き起こされ、細胞生存を損なう一方で、矛盾することにミトファジーによって一時的に細胞を保護しつつKSHVの複製を許してしまいます。治療的には、HSP27阻害をDRP1駆動のミトファジーを阻む薬と組み合わせることで、腫瘍細胞をより速やかに死に導き、ウイルスの拡散の機会を制限する──この致命的なリンパ腫に対する二方面作戦が期待されます。
引用: Gonnella, R., Corrado, V., Scaffidi, G.F. et al. Inhibiting HSP27 activates the XBP1s/CerS1 interplay, which triggers DRP1-driven mitophagy, thereby protecting against cell death and promoting the KSHV lytic cycle in primary effusion lymphoma cells. Cell Death Discov. 12, 118 (2026). https://doi.org/10.1038/s41420-026-02979-2
キーワード: 原発性滲出性リンパ腫, カポジ肉腫関連ヘルペスウイルス, 細胞ストレス応答, ミトファジー, 熱ショックタンパク質 HSP27