Clear Sky Science · ja
AdipoR1–AMPK 軸は、フェロトーシスやアポトーシスを含む多様な細胞死経路を介して分子サブタイプを横断して乳がんを抑制する
乳がんにおいて脂肪細胞が重要な理由
多くの人は体脂肪を受動的なエネルギー貯蔵と考えがちですが、脂肪細胞はホルモンやシグナル分子を血流へ送り出す能動的な工場です。本研究は、脂肪由来のシグナルの一つが乳がん細胞上の分子AdipoR1を介して作用し、腫瘍の成長を遅らせうる仕組みを探ります。本研究は、脂肪組織と腫瘍の間の情報伝達を利用することで、多くのタイプの乳がんに対する新たな治療法を示唆し、既存薬の効果を高める可能性がある点で重要です。
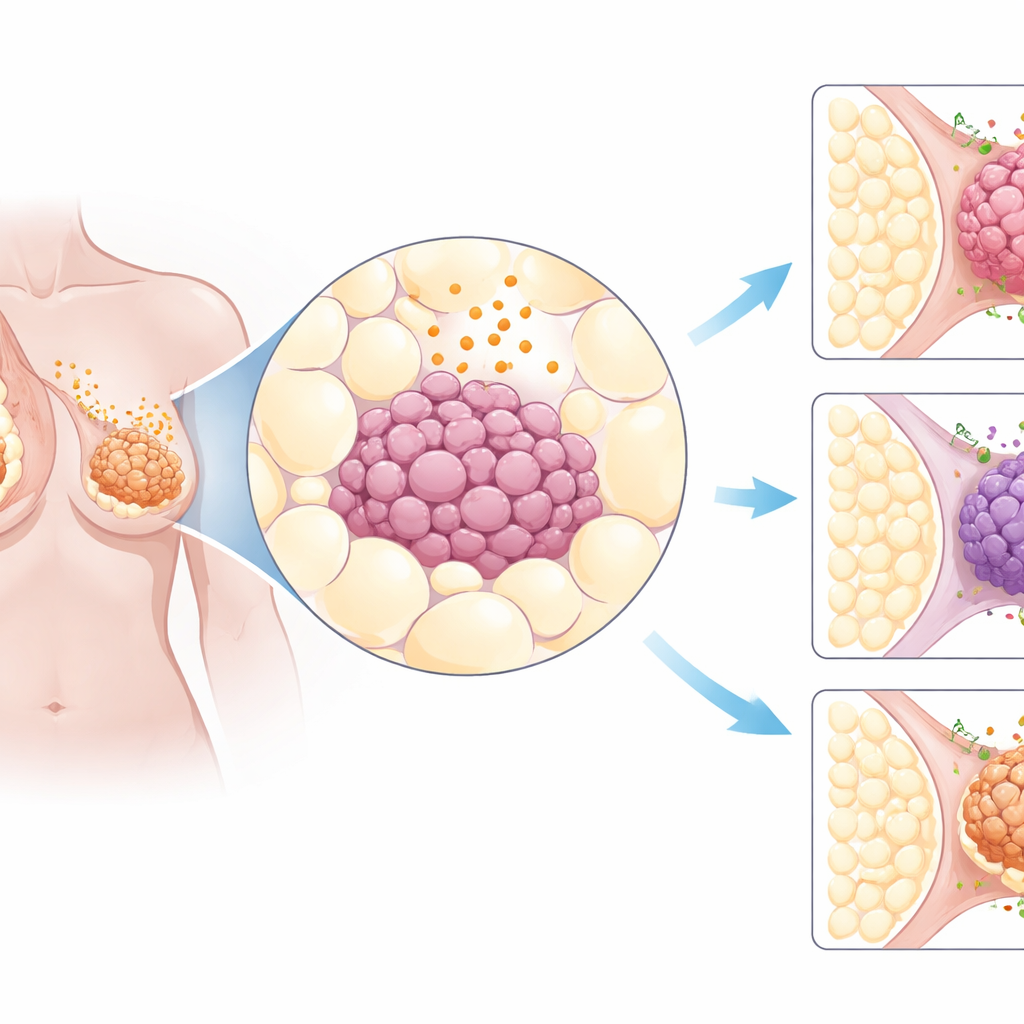
多くのがんを横断してみる
研究者たちはまず、何千件もの患者腫瘍の遺伝情報を含む大規模な公開がんデータベースを解析しました。彼らは脂肪組織からのシグナルやそれを受け取る細胞構造に関わる約30数個の遺伝子に注目しました。31の異なる臓器由来の腫瘍と正常組織を比較したところ、あるパターンが際立ちました:乳がんはこれら脂肪関連シグナルにおいて特に顕著な変化を示していました。とくに受容体AdipoR1は、ホルモン駆動型、HER2陽性、あるいはより攻撃的なトリプルネガティブ型であっても、乳がんでしばしば通常より高レベルで存在していました。600例以上の乳がん組織標本でも、腫瘍細胞にAdipoR1タンパク質が広く存在することが確認されました。
脂肪シグナル薬をがん細胞で試す
AdipoR1が腫瘍内で実際にどのように作用するかを調べるため、研究チームは複数の一般的なサブタイプを代表する乳がん細胞株を実験室で培養しました。彼らはAdipoR1を活性化する小分子であるAdipoRonでこれらの細胞を処理しました。AdipoRonは速やかに細胞内のエネルギー感知スイッチであるAMPKを作動させ、シグナルが細胞に伝わっていることを示しました。AdipoRonの用量が増すにつれ、がん細胞の増殖は遅くなり、創傷治癒試験での移動も減り、多くの細胞がプログラムされた自己破壊を起こしました。研究者が意図的に細胞内のAdipoR1レベルを低下させるとAdipoRonの効果は大部分失われ、一方でAdipoR1を増強すると薬剤の効果が高まり、この作用が直接この受容体に結び付くことが示されました。
がん細胞を死へと追いやる複数の経路
処理後の遺伝子発現を解析した結果、AdipoRonは乳がん細胞内のストレス応答を誘導していることが分かりました。標準的なプログラム細胞死に結びつく遺伝子だけでなく、鉄依存性の新しく認識された細胞死様式であるフェロトーシスに関係する遺伝子も活性化しました。この過程の主要なマーカーは、特にホルモン感受性の乳がん細胞でRNAとタンパク質レベルの両方で上昇し、細胞脂質の損傷を示す化学的指標もこの所見を支持しました。同時に、AdipoRonは通常がん細胞の生存を助けるタンパク質のレベルを低下させました。そこにはDNA修復を助けるBRCA1やBRCA2、多くの腫瘍で増殖を促すエストロゲン受容体、攻撃的な振る舞いに関係する表面分子TROP2などが含まれていました。
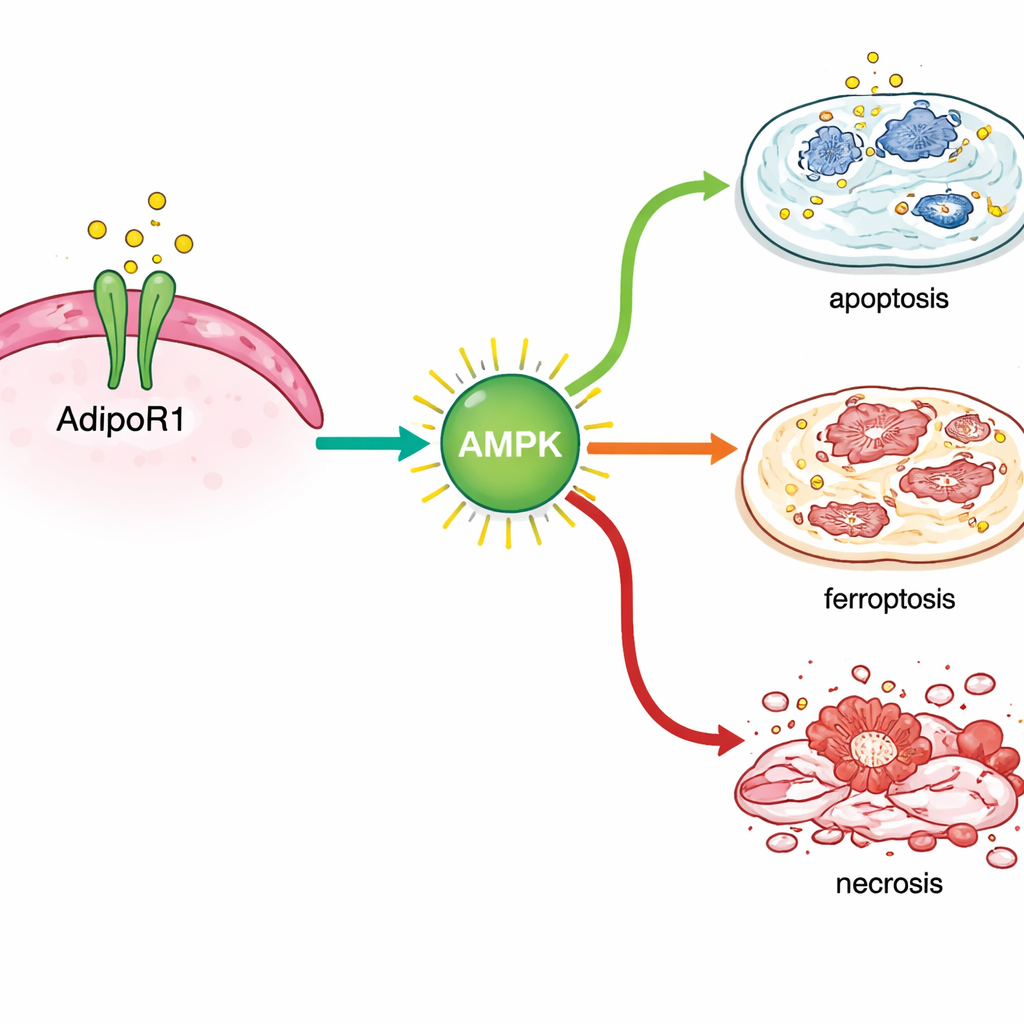
現在の治療と競合せず協調して働く
研究チームは次に、AdipoR1を活性化することが標準治療を補完できるかを検討しました。ホルモン感受性乳がん細胞では、AdipoRonとタモキシフェンの併用が単独より強い増殖抑制を示しました。トリプルネガティブ系の細胞株では、AdipoRonはパクリタキセルやドキソルビシンといった一般的な化学療法剤の効果を高めました。ホルモン感受性乳腫瘍を移植したマウスでは、研究者らは経口でAdipoRonを投与しました。処理された動物の腫瘍は成長が遅く、組織学的に観察すると壊死領域が大きくなっていました。重要なのは、治療期間を通じてマウスに行動、体重、肝機能に明白な副作用は見られなかった点です。
患者への示唆
総じて、この知見は乳がん細胞でAdipoR1を作動させることで重複する複数の細胞死ルートが動員され、主要な生存システムが弱められ、かつこのアプローチが異なる遺伝的背景のがんにわたって有効であることを示唆します。現行治療を置き換えるのではなく、AdipoR1を標的とする薬剤(AdipoRonのようなもの)は、ホルモン療法、化学療法、将来の標的薬に対して腫瘍をより脆弱にする付加的な治療として作用する可能性があります。臨床応用に先立ち、より強力で選択的なAdipoR1作動薬の開発、どの患者の腫瘍が受容体を強く発現するかの明確化、安全性の慎重な評価が必要です。それでも、本研究は興味深い発想を示しています:私たち自身の脂肪組織からの信号が、がんを助長する代わりに戦う方向に向け直されうるということです。
引用: Sato, S., Yamanaka, T., Komori, Y. et al. AdipoR1–AMPK axis suppresses breast cancer across molecular subtypes via multimodal cell death pathways, including ferroptosis and apoptosis. Cell Death Dis 17, 384 (2026). https://doi.org/10.1038/s41419-026-08583-7
キーワード: 乳がん, アディポカイン, AdipoR1, 細胞死経路, がん代謝