Clear Sky Science · ja
短鎖アシルCoAデヒドロゲナーゼはミトコンドリアDNAの脱メチル化と漏出を開始し、大腸がんにおける抗腫瘍免疫を促進する
なぜ私たち自身の細胞が時にがんを免疫から隠すのか
大腸がんは世界で最も致命的ながんの一つであり、その一因はしばしば体の免疫防御がそれを認識して攻撃できないことにあります。本研究は、がん細胞の脂肪の燃やし方、ミトコンドリアがそのDNAを扱う方法、そして免疫系が腫瘍の存在を察知するかどうかの間に予期せぬつながりを明らかにします。この一連の事象をたどることで、研究者らは長年知られた天然化合物ハイペリシンが大腸がんで免疫攻撃を再活性化する可能性を持つことも示しています。
結腸腫瘍で欠落したミトコンドリアの「守り手」
研究チームはまず、大規模なヒトおよびマウスのデータセットを検索し、大腸がんで一貫して変化する代謝遺伝子を見つけ出しました。そこで注目されたのが短鎖アシルCoAデヒドロゲナーゼ(ACADS)で、通常はミトコンドリアで短鎖脂肪酸の分解を助ける酵素です。患者試料と複数のマウスモデルのいずれにおいても、腫瘍組織では周辺の正常な結腸よりもACADSの発現が著しく低下していました。マウスの結腸がん細胞でACADSを低下させると腫瘍はより速く、より攻撃的に成長し、逆にACADSを増やすと腫瘍成長は抑制されました。腸上皮に特異的にACADSを欠損させた遺伝子改変マウスは、化学誘発性の大腸炎関連がんモデルでより多く、より大きな腫瘍を発生させ、ACADSが腸で腫瘍抑制因子として働くことを支持しました。
腫瘍が免疫の警報信号を下げる仕組み
これらの成長効果は、培養皿上でのがん細胞の増殖速度だけでは説明がつきませんでした。増殖速度はほとんど変わらなかったからです。代わりに、ACADS欠損による腫瘍増殖は免疫系が健全な動物でのみ起こり、腫瘍微小環境の変化を示唆しました。ヒト大腸がんの単一細胞解析では、低ACADSの腫瘍はより多くの腫瘍細胞と免疫抑制的な細胞(骨髄由来抑制細胞、特定のマクロファージ、制御性T細胞など)に囲まれ、有益なT細胞やナチュラルキラー細胞は少ないことが示されました。このパターンは、がんを攻撃から守る「免疫抑制的な近傍」を指し示します。 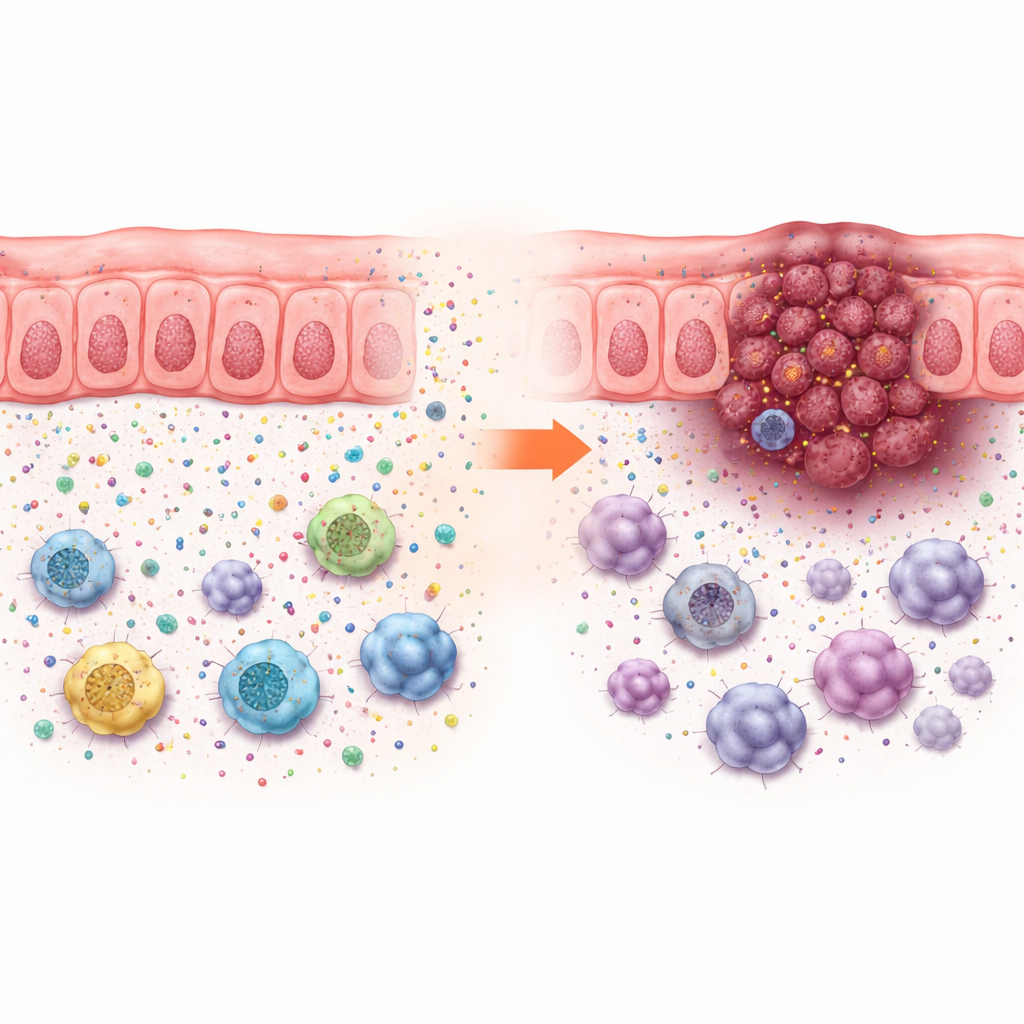
隠れた引き金としてのミトコンドリアDNA漏出
脂肪を燃やす酵素と免疫DNAセンサーを結びつけるのは何か?答えはミトコンドリアDNA(mtDNA)にあります。ストレス下で、mtDNAの断片がミトコンドリアから細胞質に漏れ出し、そこでcGASがそれらを危険信号として検知します。研究者らは、ACADS欠損のがん細胞ではこの細胞質区画中のmtDNAが減少していることを示しましたが、総mtDNA量自体は変わっていませんでした。ACADS高発現細胞でmtDNAの漏出を阻害するとcGAS–STINGが停止し、これらの漏出したDNA断片が重要な警報であることが確認されました。驚くべきことに、活性酸素種、カルシウムの急増、ミトコンドリア形態の大きな変化などの古典的なミトコンドリアストレス因子ではこの差を十分に説明できませんでした。代わりに本研究は、ミトコンドリア膜の「門」と、より重要にはmtDNA自体の化学的修飾に注目しています。 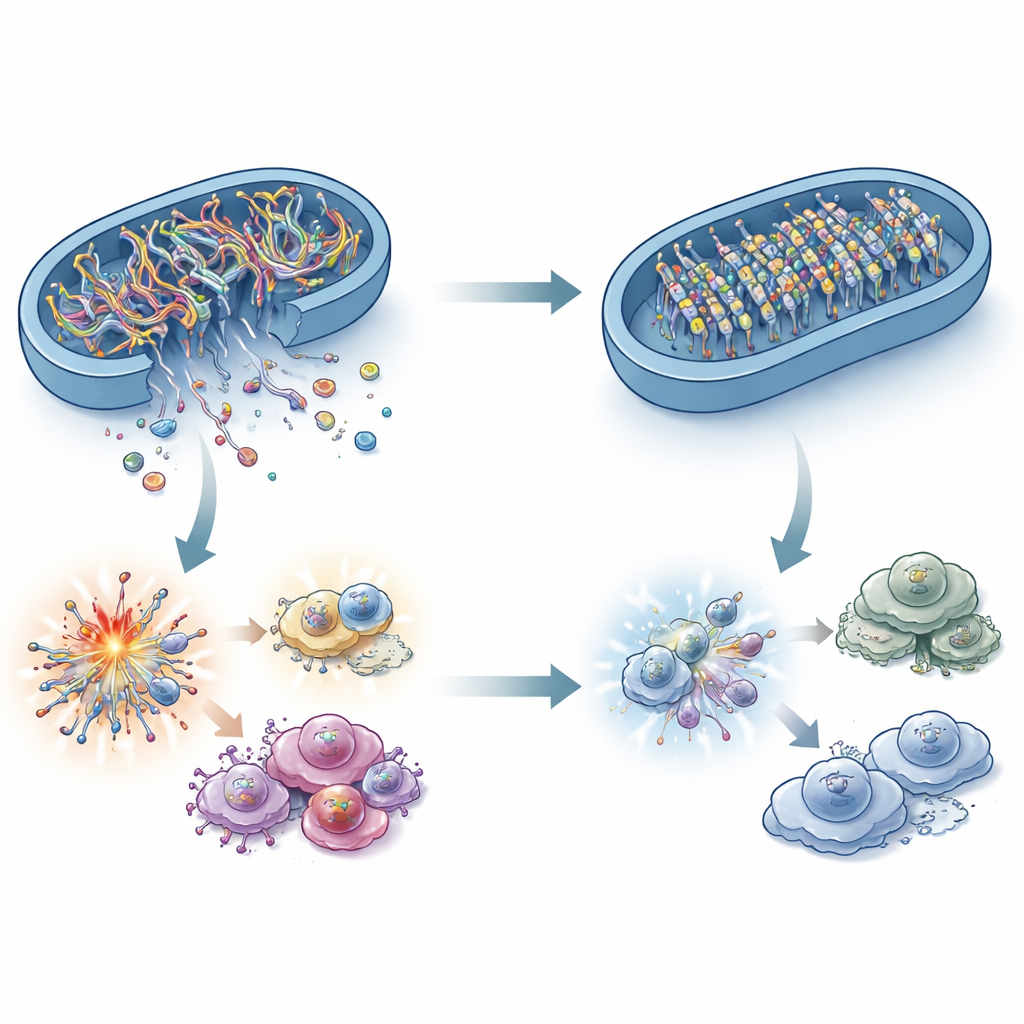
警報を内部に閉じ込めるDNAメチル化の仲間
タンパク質相互作用スクリーニングを通して、ACADSはミトコンドリアに局在するDNAメチル化酵素DNMT1の一形態と結合することが見いだされました。ACADSが失われると、このミトコンドリア型DNMT1が蓄積し、mtDNAに余分なメチル基を付加しました。これらの修飾はmtDNAを安定化させ、断片化や漏出しにくくします。ミトコンドリアDNMT1を過剰に負荷した細胞ではmtDNAの逃避が減少し、cGAS–STINGシグナルが抑えられて腫瘍成長が促進されました。一方、薬剤デシタビンでDNMT1を阻害するとmtDNA漏出が回復し、ACADS欠損腫瘍の増殖が遅くなりました。患者試料でもこれらの知見が反映されており、低ACADSは高いミトコンドリアDNMT1、弱いSTINGシグナル、少ないエフェクターT細胞、より多くの免疫抑制細胞、およびチェックポイント免疫療法への反応性の低下と一致していました。
古い化合物で免疫防御を再覚醒する
この経路を治療に活用できるかを検討するために、研究者らはコンピュータベースのスクリーニングを用いてACADSに結合する分子を探索しました。その結果、ハイペリシンという天然色素が同定されました。ハイペリシンは以前、特定の皮膚リンパ腫に対する光増感治療として試験されたことがあります。大腸がん細胞では、ハイペリシンはACADSの発現を増加させ、ミトコンドリアDNMT1を減少させ、mtDNA漏出を促進し、cGAS–STINGシグナルを再活性化しました。これらの変化はACADSの存在に依存していました。マウス腫瘍モデルおよびヒト大腸腫瘍の短期培養では、ハイペリシン処理により腫瘍が縮小するか、免疫細胞がより活性なT細胞優位の状態へとシフトしました。臨床応用にはさらに研究が必要ですが、これらの結果は薬理的にACADSを「再びオンにする」ことで、冷たい免疫抑制腫瘍を免疫療法に反応しやすい状態へと変換する可能性を示唆しています。
患者と将来の治療への意味
日常的な言葉で言えば、本研究は一部の大腸がんが成長する理由の一つとして、ミトコンドリア酵素を沈黙させていることを示しています。本来その酵素は、微小なDNA断片を細胞内に漏れさせ、それらがフレアのように免疫系を呼び込む働きをします。DNAメチル化の仲間がそのミトコンドリアDNAを固定してしまうと、ACADS欠損腫瘍はそれらのフレアを隠して免疫の検出を回避してしまいます。ACADS活性を回復すること、例えばハイペリシン様の薬剤によって、このミトコンドリアの警報システムを再開し、抗腫瘍免疫を強化し、既存の免疫療法への反応を改善する可能性があります。したがってACADS、ミトコンドリアDNMT1、STING経路の活動は、より効果的な大腸がん治療を目指す上で有用なバイオマーカーおよび標的となり得ます。
引用: Yang, F., Wang, M., Hu, S. et al. Short-chain acyl-CoA dehydrogenase initiates mtDNA demethylation and leakage to fuel antitumor immunity in colorectal cancer. Sig Transduct Target Ther 11, 113 (2026). https://doi.org/10.1038/s41392-026-02675-8
キーワード: 大腸がん, 腫瘍免疫, ミトコンドリアDNA, 脂質代謝, cGAS-STING経路