Clear Sky Science · ja
PTCH1のC末端ドメインの部分的切断はがんでGLI–PI3Kループの非正統的活性化を介して腫瘍形成を促進する
ごく小さなタンパク変化が結腸がんで問題になる理由
結腸がんは通常、遺伝的な不具合が徐々に蓄積して発生します。本研究は、細胞表面タンパク質PTCH1に生じる意外に小さな変化に注目し、その尾部の一部が切り取られることが結腸がん細胞の増殖促進、転移能の向上、および既存薬への抵抗に寄与し得ることを示します。この隠れた増殖スイッチを理解することで、一部の患者に対するより精密な治療の扉が開く可能性があります。
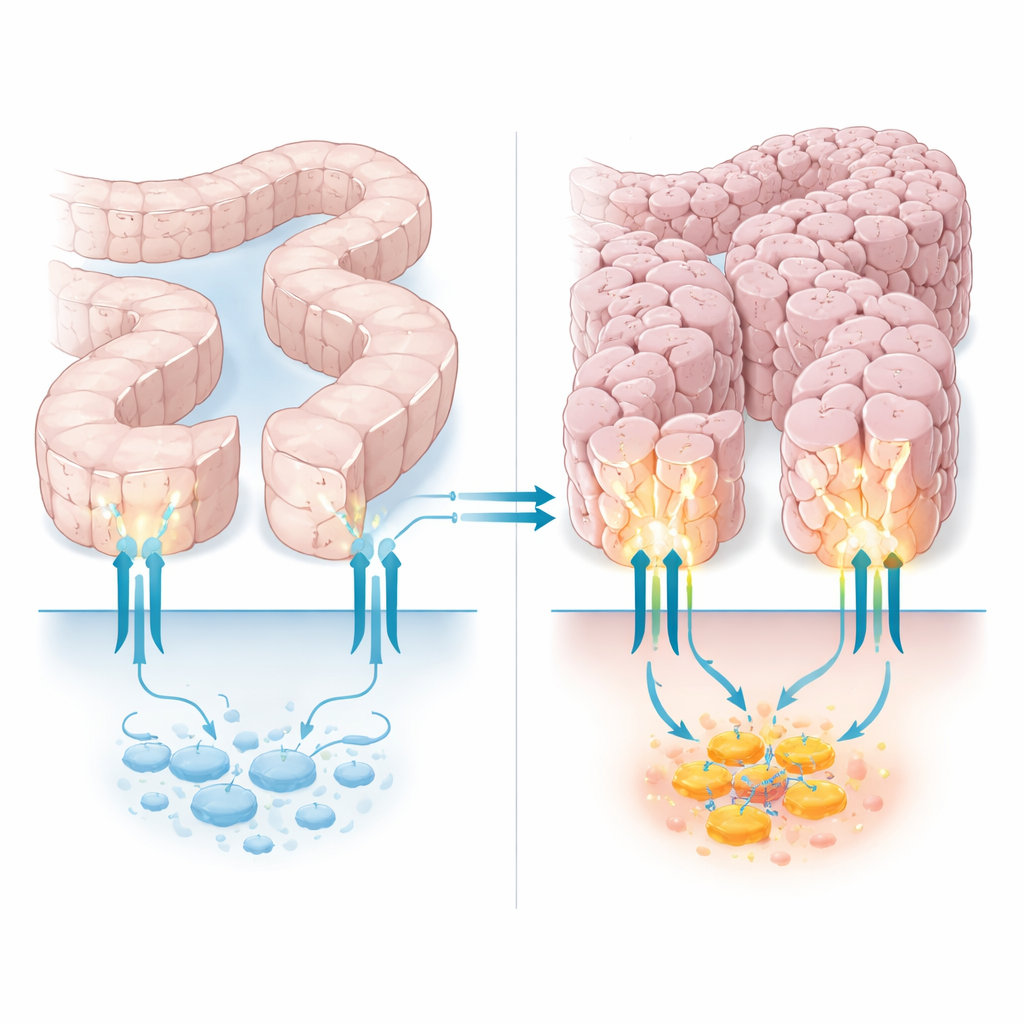
細胞の門番にあるもう一つの役割
PTCH1は発生や組織修復で用いられる通信経路であるヘッジホッグ経路の門番として知られています。古典的な役割では、PTCH1はパートナータンパク質のSmoothenedを抑えて、GLIという一群のDNA制御因子を調節します。しかしPTCH1は細胞内に長く柔らかい尾部を持ち、細胞死や細胞成分のリサイクルなどに関与する他のタンパク質のドッキング部位として働きます。以前の研究は、結腸、胃、子宮のがんの一部がこの内側の尾部の一部を切り落とす変異を持つことを示していました。これらの変異は古典的なヘッジホッグのスイッチを破壊するようには見えませんでしたが、がん細胞がストレスに強く生き延びる能力を高めており、この尾部断片がPTCH1の腫瘍抑制的役割に静かに寄与していることを示唆していました。
影響を確かめるためのがん細胞の設計
尾部短縮変異が実際に何をもたらすかを確かめるため、研究者らはCRISPR/Cas9遺伝子編集を用いて結腸がん細胞株にこれらの変異を再現しました。PTCH1尾部に異なる切断を持つ2つの編集クローンを、正常なPTCH1を持つ細胞と比較しました。変異細胞は分裂が速く、コロニー形成がはるかに多く、接着しない状態でも生き残る能力(体内での拡がりと関連する挙動)を示しました。マウスに移植すると、尾部変異細胞は数週間ではるかに大きな腫瘍を形成し、分裂中の細胞が増えていました。重要なのは、編集細胞は依然としてPTCH1を産生し、その主要な門番機能を保持していたことであり、攻撃性の増加はPTCH1自体の喪失ではなく、尾部の特化した細胞内機能喪失に起因することを示しています。
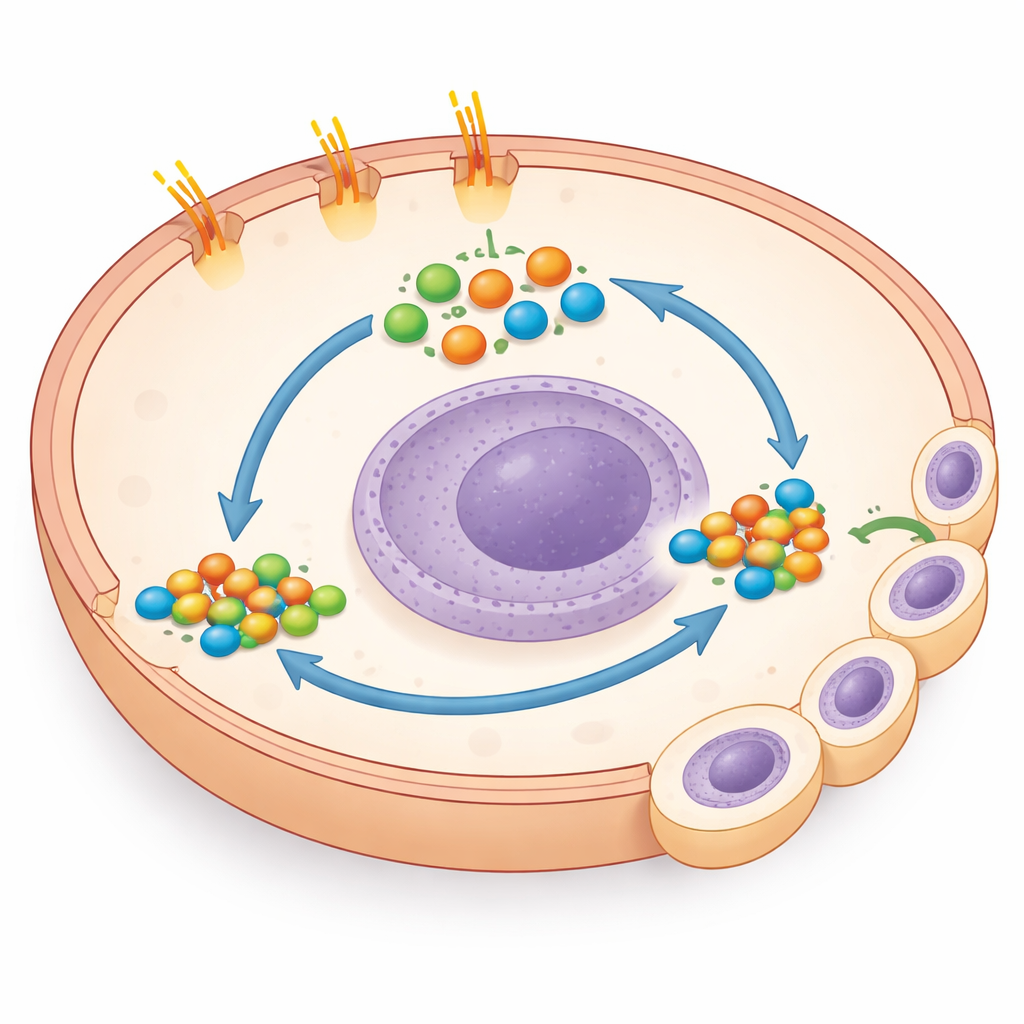
強力な増殖スイッチへの意外な近道
基礎生物学を掘り下げると、研究チームは予想外の発見をしました:尾部が短縮された細胞は、増殖と生存を促す遺伝子プログラムの主要駆動因子であるGLI1とGLI2のレベルが著しく上昇していました。通常、GLI活性はSmoothenedの解放によって上がりますが、ここではSmoothenedを阻害しても効果がありませんでした。代わりに、小分子でGLIを直接阻害するか、遺伝学的手法でGLI1を低下させると、培養皿内およびPTCH1尾部変異を自然に持つ他の結腸がん細胞株でも変異細胞の増殖が急激に抑えられました。これは尾部喪失が古典的なヘッジホッグスイッチをバイパスする“非正統的”経路でGLIを活性化し、がん細胞がその近道に強く依存するようになることを示しています。
複数の増殖回路が活性化するが、一つのループが支配的
細胞のRNAを配列決定したところ、PTCH1尾部の短縮で活性が変化する何千もの遺伝子が見つかりました。その多くはEGFR、Ras、および代謝や幹細胞様性を制御するシグナル系など、よく知られたがん回路に属していました。変異細胞はEGFRとそのリガンドの活性上昇、そして二つの主要な下流経路であるMAPKとPI3K/Aktの高活性を示しました。しかし、研究者らがEGFRやそのMAPK分岐を阻害しても変異細胞の増殖は部分的にしか抑えられませんでした。一方で、低用量のPI3K阻害剤は増殖とコロニー形成を強く抑え、GLI1レベルも低下させ、PI3K/Aktがこの新しいGLI活性化機構の重要なパートナーであることを示しました。
腫瘍成長を駆動する自己増強ループ
さらに実験を進めるとフィードバックサイクルが明らかになりました:PTCH1の尾部切断はGLI活性を高め、GLIはPI3K/Aktシグナルの高止まりを助け、PI3K/AktはGLIを安定化・活性化するのです。GLIかPI3Kのいずれかを遮断するとこのループは崩れ、変異細胞の増殖優位性は失われましたが、単にPI3K/Aktを上げてもGLIの直接的な遮断を克服することはできませんでした。さらに、GLIタンパク質を通常は不活性化する働きのある酵素PKAの活性が低下しており、これがGLI駆動プログラムへの傾斜をさらに助長していると考えられます。
将来の治療にとっての意味
患者にとっての主要なメッセージは、一部の結腸がんがPTCH1尾部変異を抱え、GLI–PI3Kの正のフィードバックループを静かに結びつけて腫瘍を成長させ、より馴染みのあるヘッジホッグスイッチやEGFR–MAPK経路を標的とする薬から逃れる助けになっている可能性がある、ということです。これらの腫瘍はむしろGLIを直接遮断する治療やPI3K/Aktを標的とする治療に特に感受性があるかもしれません。本研究は、PTCH1の配列決定、特にこれらの変異がより頻繁に見られる結腸の右側からの腫瘍に対して行うことが、PI3KやGLIを標的とする戦略で恩恵を受ける患者を特定する助けになり得ることを示唆しており、ごくわずかなタンパクの切断が有用な治療手がかりになり得ることを示しています。
引用: Caballero-Ruiz, B., Bordone, R., Coni, S. et al. Partial truncation of the C-terminal domain of PTCH1 in cancer promotes tumourigenesis by non-canonical activation of a GLI-PI3K loop. Oncogene 45, 1013–1025 (2026). https://doi.org/10.1038/s41388-026-03698-9
キーワード: 結腸がん, ヘッジホッグシグナル伝達, PTCH1変異, GLI転写因子, PI3K–Akt経路