Clear Sky Science · it
Approfondimenti a singola cellula sulla eterogeneità trofoblastica e la disfunzione adattativa nella restrizione selettiva della crescita fetale
Quando un gemello rimane indietro
Per i genitori in attesa di due gemelli, può essere profondamente angosciante quando un bambino smette di crescere quanto l’altro, pur condividendo lo stesso utero e la stessa placenta. Questa condizione, chiamata restrizione selettiva della crescita fetale, non solo mette a rischio la salute del gemello più piccolo prima della nascita, ma può anche influenzare lo sviluppo a lungo termine. Questo studio utilizza analisi all’avanguardia a singola cellula per scrutare la placenta condivisa di queste gravidanze gemellari, rivelando come piccole alterazioni in specifiche cellule placentari e nelle risposte immunitarie possano inclinare l’equilibrio tra una crescita sana e una pericolosa carenza.
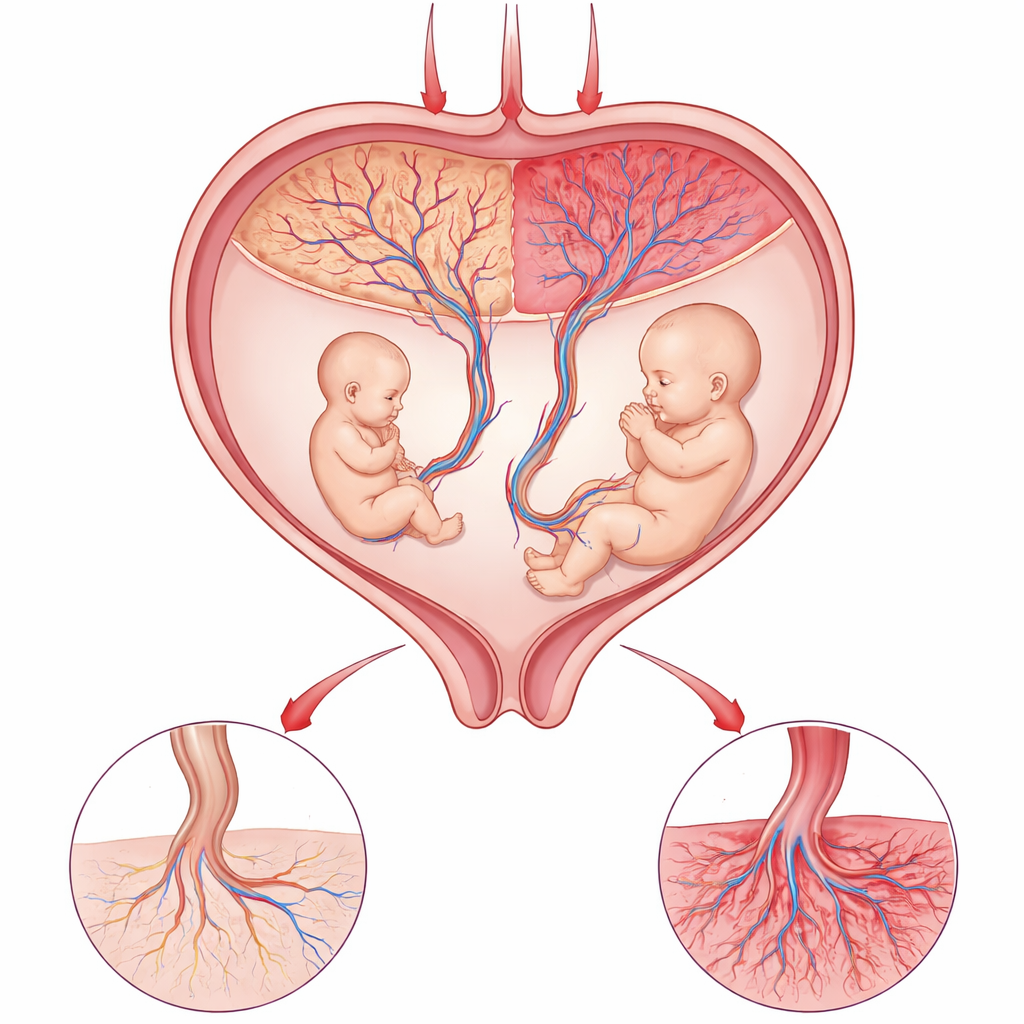
Il delicato equilibrio della placenta
La placenta è il collegamento vitale tra madre e bambino, fornendo ossigeno e nutrienti mentre rimuove i rifiuti. In alcune gravidanze di gemelli identici, entrambi i feti condividono una singola placenta ma occupano territori diversi al suo interno. Quando un gemello diventa molto più piccolo dell’altro, i medici sanno che qualcosa è andato storto a livello locale in quell’organo condiviso. Poiché i gemelli hanno la stessa madre e geni quasi identici, offrono un potente esperimento naturale: qualsiasi differenza significativa nella crescita è probabilmente da attribuire al funzionamento delle rispettive parti della placenta, piuttosto che a differenze tra i feti stessi.
Zoom sulle singole cellule placentari
I ricercatori hanno raccolto campioni placentari da tre gravidanze in cui un gemello era significativamente più piccolo dell’altro. Usando il sequenziamento dell’RNA a singola cellula — un metodo che legge l’attività di migliaia di geni in cellule individuali — hanno profilato più di 175.000 cellule provenienti dalle diverse regioni placentari. Questo ha permesso di classificare le cellule in tipi distinti, compresi cellule di supporto, cellule dei vasi sanguigni e diversi tipi di cellule immunitarie. Si sono concentrati su un gruppo chiave chiamato citotrofoblasti villosi, uno strato di cellule che riveste le piccole proiezioni a forma di dito dove il sangue materno incontra la circolazione fetale e che continuamente rigenera e ripara la superficie della placenta.
Due stati cellulari chiave: struttura contro modalità di sopravvivenza
All’interno di questi citotrofoblasti villosi, il team ha identificato due principali stati con ruoli molto diversi. Un gruppo, caratterizzato da una molecola chiamata TP63, agiva come custode strutturale: sosteneva la barriera madre-bambino, manteneva le connessioni cellula-cellula e contribuiva a mantenere organizzato il tessuto. L’altro gruppo, caratterizzato da un enzima chiamato LDHA, era orientato verso un’intensa produzione energetica e la gestione dello stress, attivando vie legate ai mitocondri, allo stress ossidativo e al controllo della qualità delle proteine. Nei territori placentari dei gemelli più piccoli, le cellule protettive TP63 risultavano impoverite, mentre le cellule orientate allo stress LDHA si espandevano e si replicavano più attivamente. Analisi computazionali di “traiettoria” suggerivano che le cellule venivano spinte lungo un percorso dalla funzione strutturale sana verso una modalità di sopravvivenza, con meno cellule che raggiungevano lo stato totalmente fuso che normalmente mantiene una superficie di scambio liscia ed efficiente.
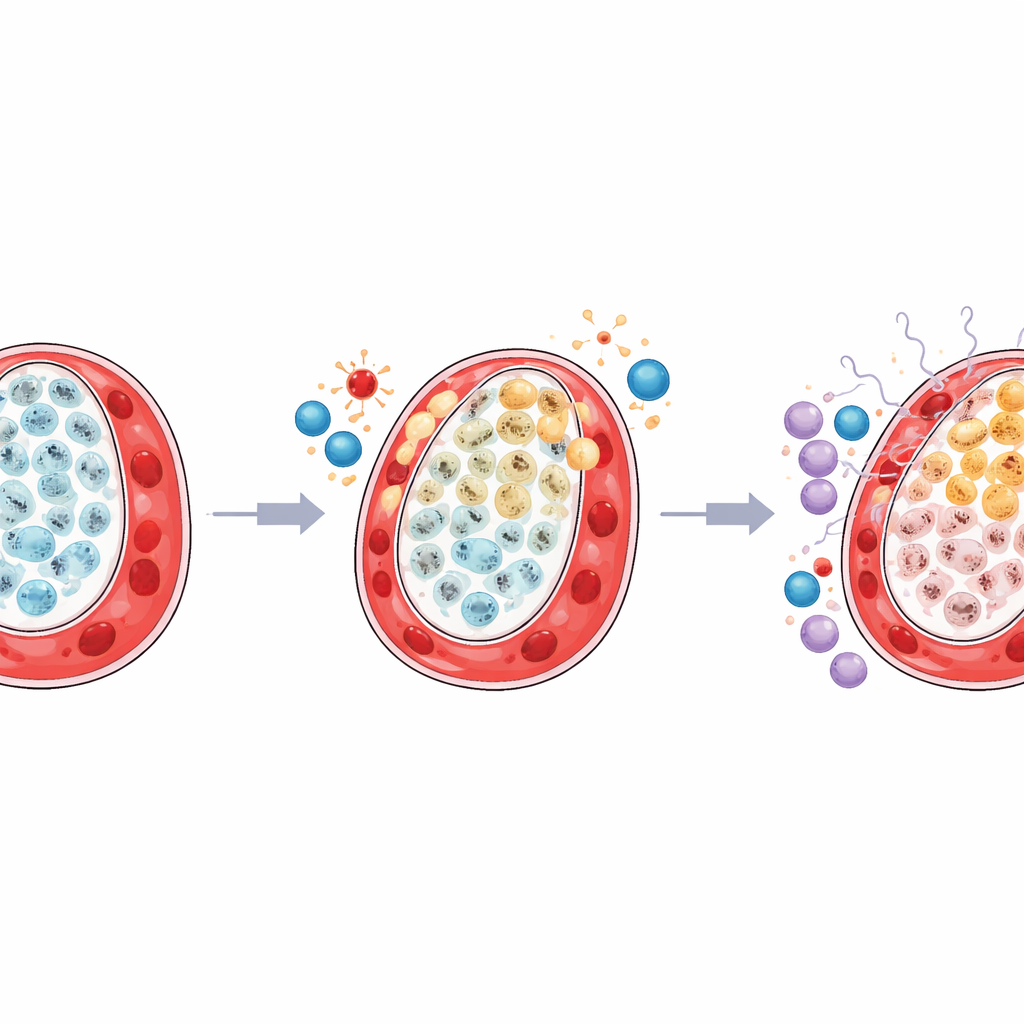
Un vicinato infiammato attorno alle cellule sotto stress
Lo studio ha inoltre rilevato che l’ambiente immunitario circostante nel territorio placentare del gemello più piccolo era rimodellato in modo dannoso. Un tipo utile di macrofagi residenti, noti come cellule di Hofbauer, che normalmente supportano la salute tissutale e gestiscono il metabolismo, risultava ridotto. Allo stesso tempo, alcuni linfociti natural killer, predisposti a risposte antivirali e infiammatorie, diventavano più abbondanti e più attivi. Una mappatura dettagliata dei segnali scambiati tra le cellule ha mostrato che i trofoblasti di tipo LDHA sotto stress interagivano più intensamente con le cellule immunitarie attraverso percorsi guidati dall’interferone e da molecole di allarme correlate. Nel frattempo, la comunicazione tra le cellule strutturali TP63 e le cellule stromali e vascolari di supporto si indeboliva, suggerendo che venivano perse sia la sostegno fisico sia la regolazione immune pacificante.
Un collasso a tre vie che limita la crescita fetale
Nel complesso, il lavoro dipinge un quadro chiaro e accessibile di ciò che va storto nella placenta quando un gemello rimane indietro. Le cellule di supporto strutturale che mantengono la superficie di scambio compatta e ordinata si esauriscono, le cellule stressate affamate di energia prendono il sopravvento e il sistema immunitario si sposta verso uno stato più infiammatorio. Questi tre fili — perdita di struttura, sovraccarico metabolico e infiammazione cronica — si rinforzano a vicenda e compromettono gradualmente la capacità della placenta di fornire ossigeno e nutrienti sufficienti al bambino più piccolo. Identificando i tipi cellulari e le vie di segnalazione coinvolte, questo studio fornisce una mappa per futuri test e trattamenti volti a individuare prima i problemi placentari e, forse, a riportare queste cellule verso un equilibrio più salutare.
Citazione: Bi, Y., Yang, J., Li, X. et al. Single-cell insights into trophoblast heterogeneity and adaptive dysfunction in selective fetal growth restriction. Commun Biol 9, 387 (2026). https://doi.org/10.1038/s42003-026-09798-2
Parole chiave: placenta, gravidanza gemellare, restrizione della crescita fetale, sequenziamento dell'RNA a singola cellula, cellule trofoblastiche