Clear Sky Science · it
Quantificazione dei micronuclei da immagini ematologiche su vetrini interi mediante IA come biomarcatore farmacodinamico traducibile per inibitori della risposta al danno del DNA
Perché dei puntini minuscoli nel sangue possono raccontare grandi storie
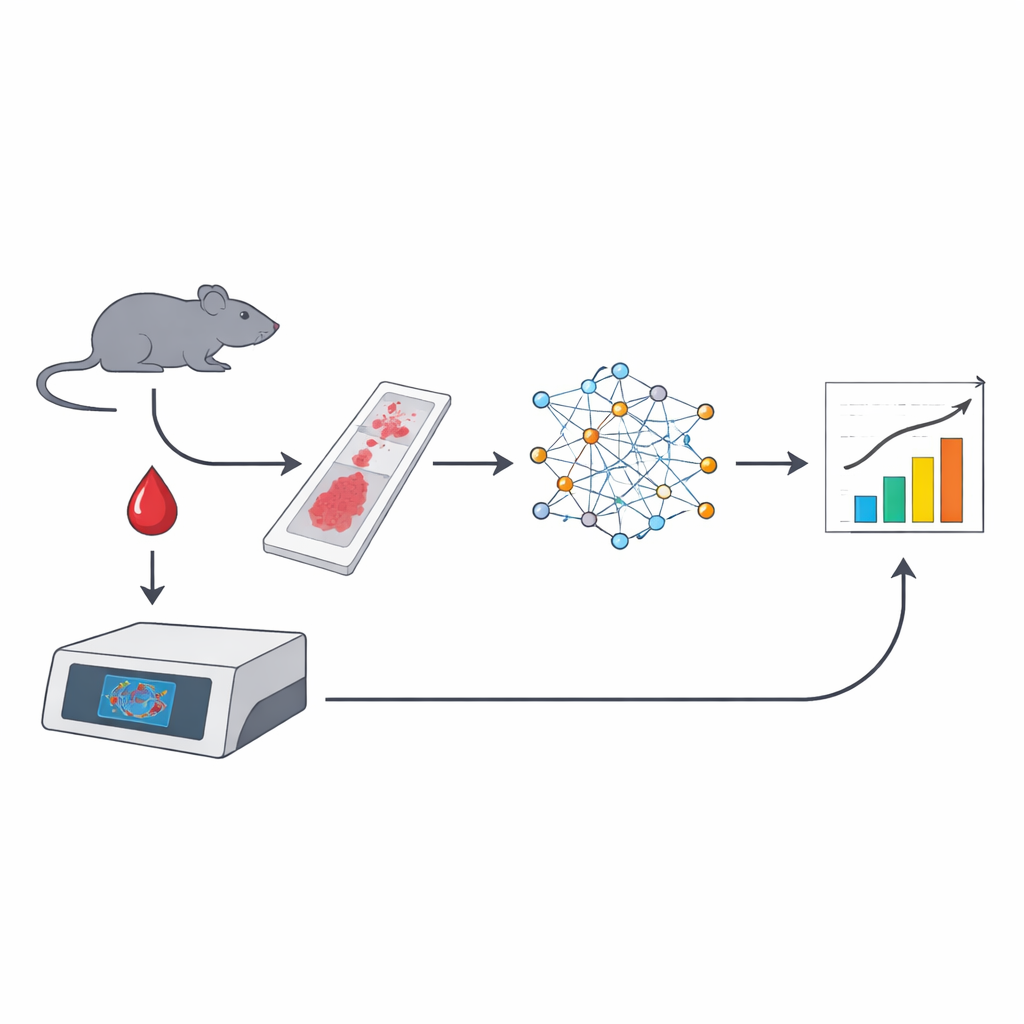
I medici e gli scienziati cercano sempre metodi semplici per capire se un farmaco antitumorale sta facendo ciò che deve all’interno del corpo. Questo studio mostra che piccole macchie nei globuli rossi, chiamate micronuclei, possono funzionare come indicatori naturali del danno al DNA provocato da alcuni trattamenti antitumorali. Combinando l’imaging a vetrino intero in stile microscopio con l’intelligenza artificiale (IA), i ricercatori hanno trasformato poche gocce di sangue in una lettura ricca e automatizzata di quanto efficacemente agiscono i farmaci che prendono di mira il DNA.
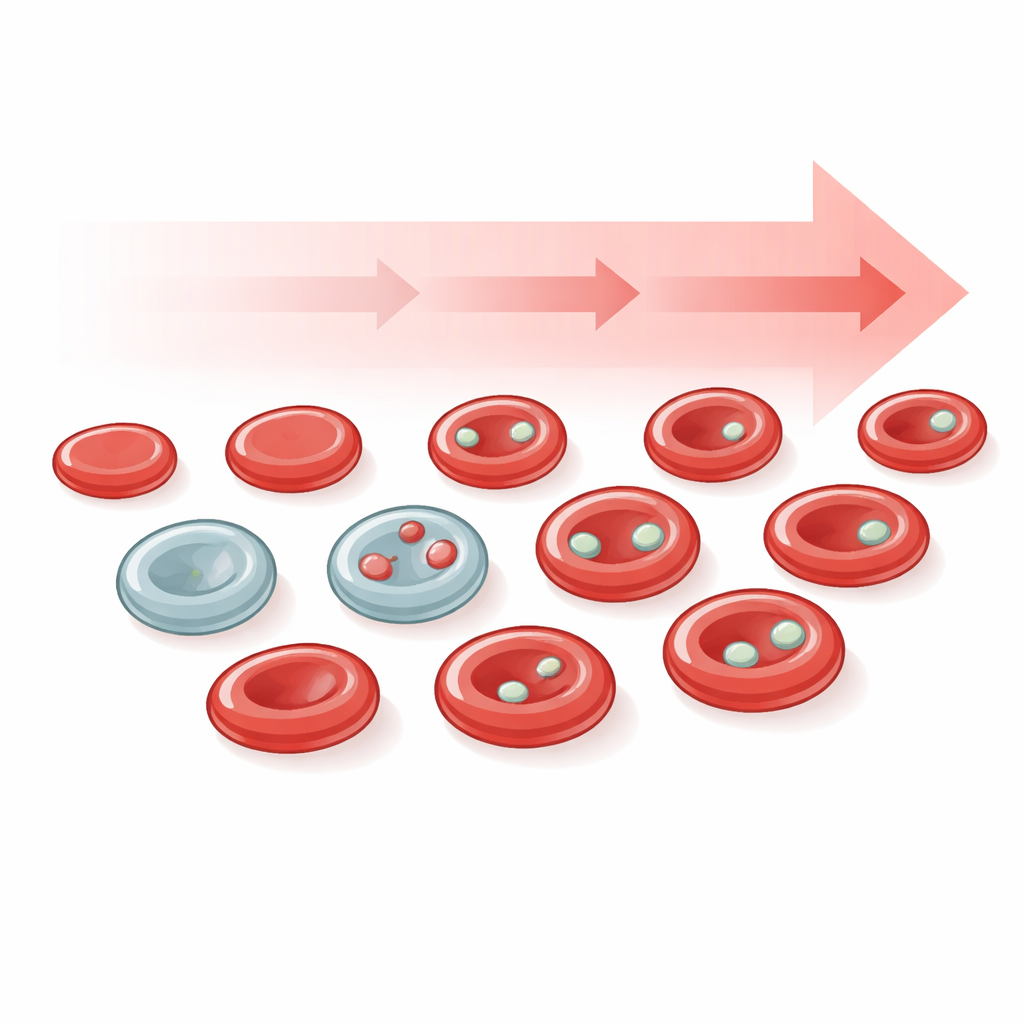
Piccole isole di DNA nei globuli rossi
I micronuclei sono piccole sacche di DNA che si trovano separate dal nucleo principale di una cellula. Si formano quando i cromosomi si rompono o vengono distribuiti in modo errato durante la divisione cellulare, eventi comuni nel cancro e dopo l’esposizione ad agenti che danneggiano il DNA. Nella maggior parte dei tessuti, individuare veri micronuclei al microscopio è difficile perché sottili sezioni tissutali possono ingannare l’occhio. I globuli rossi offrono una soluzione: durante la maturazione espellono normalmente il loro nucleo principale, ma eventuali micronuclei formatisi precedentemente possono restare come puntini piccoli e ben definiti. Queste strutture note da tempo, storicamente chiamate corpi di Howell–Jolly, sono quindi micronuclei reali e comodi che circolano nel sangue e possono rivelare quanto danno al DNA si sia verificato di recente.
Trasformare gli strisci di sangue in dati con l’IA
Il gruppo ha sviluppato una pipeline automatizzata che parte da strisci di sangue standard di topi, colorati con un colorante fluorescente per il DNA o con i comuni coloranti May–Grünwald Giemsa utilizzati nei laboratori ospedalieri. I vetrini interi sono stati scannerizzati ad alta risoluzione e sono stati addestrati modelli di deep learning supervisionato a riconoscere i globuli rossi, individuare i micronuclei e distinguere i reticolociti immaturi dagli eritrociti maturi sulla base di sottili differenze di dimensione e colore. Da una singola immagine il sistema poteva analizzare più di 100.000 cellule, segnalare quelle contenenti micronuclei e persino contare le cellule con più di un micronucleo—una capacità che la citometria a flusso convenzionale non esegue facilmente.
Collegare piccole variazioni nel sangue alla potenza del farmaco
I ricercatori hanno poi verificato se la frequenza dei globuli rossi positivi per micronuclei fosse correlata all’esposizione a chemioterapici che danneggiano il DNA e a farmaci che bloccano la risposta al danno del DNA, come gli inibitori PARP. Nei topi trattati con cisplatino o paclitaxel, i conteggi basati su IA hanno rilevato gli aumenti attesi di cellule micronucleate. Nei topi portatori di tumore trattati con gli inibitori PARP olaparib o saruparib, dosi più alte producevano aumenti maggiori delle cellule contenenti micronuclei e una più marcata riduzione del tumore. Nell’arco di diverse settimane di somministrazione quotidiana, piccoli campioni di sangue seriali (di soli circa 5 microlitri ciascuno) hanno permesso al gruppo di seguire come i micronuclei si accumulassero lentamente e poi diminuissero dopo la sospensione del trattamento. Confrontando il metodo su vetrini con la citometria a flusso standard, i due approcci hanno mostrato una forte concordanza, dimostrando che il nuovo flusso di lavoro è sia accurato sia robusto.
Zoom sui globuli rossi giovani per segnali più nitidi
Poiché i globuli rossi giovani (reticolociti) hanno una probabilità particolarmente alta di contenere micronuclei freschi, gli investigatori hanno addestrato i loro algoritmi a suddividere la popolazione dei globuli rossi in cellule immature e mature su vetrini colorati di routine. Questo affinamento ha rivelato che i micronuclei erano molto più arricchiti e dinamici nei reticolociti rispetto alle cellule più vecchie, fornendo un segnale più sensibile e rapidamente variabile dell’attività del farmaco. Le immagini a vetrino intero hanno anche reso possibile monitorare la qualità del campione in sé—for example, individuando globuli rossi deformati dopo una conservazione inadeguata—in modo che i vetrini non idonei potessero essere segnalati prima dell’analisi, un passaggio importante per l’uso clinico futuro.
Che cosa potrebbe significare per la cura del cancro in futuro
Lo studio dimostra che un piccolo campione di sangue, una colorazione standard del vetrino e una pipeline di imaging alimentata dall’IA possono insieme fornire una misura scalabile e minimamente invasiva di quanto intensamente i farmaci che prendono di mira il DNA stanno influenzando l’organismo. Pur essendo il lavoro condotto nei topi e i globuli rossi rappresentativi solo di quanto accade all’interno dei tumori, il forte legame tra i segnali dei micronuclei e la risposta tumorale suggerisce che questo approccio potrebbe diventare uno strumento pratico nello sviluppo farmacologico e, infine, negli studi clinici. In termini semplici, contare questi microscopici “puntini” di DNA nel sangue può aiutare ricercatori e clinici a tarare i dosaggi, confrontare nuovi farmaci e seguire gli effetti del trattamento nel tempo—senza biopsie invasive ripetute.
Citazione: Yong, K.H.R., Robak, W.S., Mulderrig, L. et al. Micronucleus quantification from whole-slide haematology images using AI serves as a translatable pharmacodynamic biomarker for DNA damage response inhibitors. Sci Rep 16, 11437 (2026). https://doi.org/10.1038/s41598-026-41458-7
Parole chiave: micronuclei, globuli rossi, inibitori PARP, patologia digitale, risposta al danno del DNA