Clear Sky Science · it
Potenziale effetto gonadoprotettivo della sitagliptina contro la disfunzione testicolare indotta da paclitaxel mediante la mediazione della via di segnalazione PERK/CHOP/NLRP3/Sestrin2
Perché questo studio è importante per i pazienti oncologici
La chemioterapia salva vite ma può danneggiare silenziosamente la fertilità, soprattutto negli uomini. Un farmaco oncologico molto usato, il paclitaxel, è noto per arrecare danni ai testicoli e ridurre la qualità dello sperma. Questo studio su ratti pone una domanda pratica con chiara rilevanza umana: una pillola per il diabete già approvata, la sitagliptina, può essere riproposta per proteggere il sistema riproduttivo maschile dagli effetti collaterali del paclitaxel senza interferire con la sua azione antitumorale?
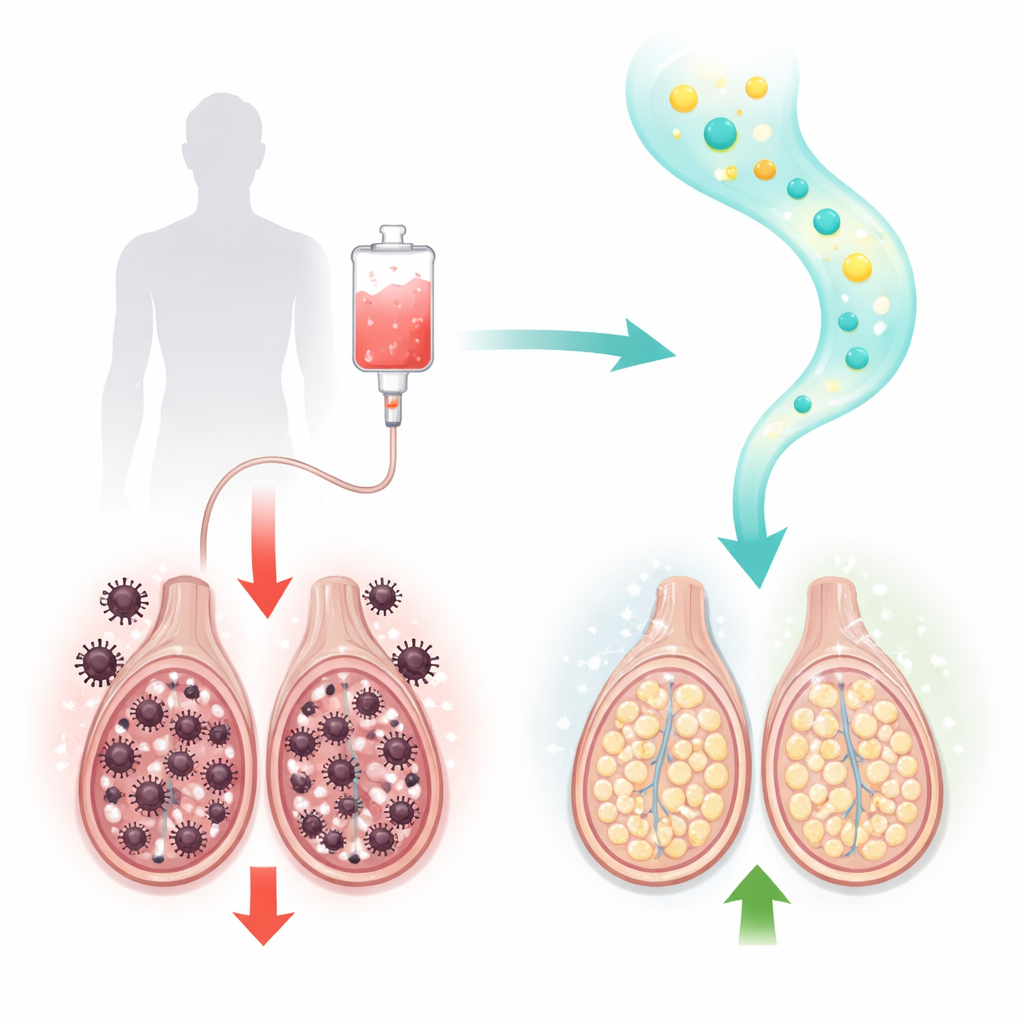
Un farmaco anticancro con un costo nascosto
Il paclitaxel è un trattamento di riferimento per tumori solidi come quelli al seno, ovaio e polmone. Agisce bloccando la macchina della divisione cellulare nelle cellule tumorali ad accrescimento rapido. Sfortunatamente, anche le cellule proliferanti degli organi sani sono vulnerabili. Nei ratti maschi, il trattamento con paclitaxel ha prodotto segni classici di danno testicolare: conteggio spermatico, motilità e vitalità sono calati nettamente, mentre è aumentata la percentuale di spermatozoi deformi. Al microscopio i ricercatori hanno osservato tubuli seminiferi danneggiati (dove si formano gli spermatozoi) e cellule di Leydig produttrici di ormoni compromesse, insieme ad assottigliamenti degli strati tissutali. Le analisi del sangue hanno confermato una forte riduzione del testosterone e di un enzima chiave per la sua sintesi, la 17β‑idrossisteroide deidrogenasi.
Un farmaco per il diabete come protettore inaspettato
La sitagliptina è ampiamente prescritta per controllare la glicemia nelle persone con diabete di tipo 2. Studi precedenti hanno suggerito che, oltre agli effetti metabolici, la sitagliptina può attenuare lo stress ossidativo dannoso, l’infiammazione e la morte cellulare in organi come fegato, rene e cervello. Sulla scia di queste evidenze, i ricercatori hanno diviso i ratti maschi in quattro gruppi: controlli non trattati, un gruppo solo con paclitaxel e due gruppi trattati con paclitaxel più sitagliptina a dose bassa o alta per due settimane. Hanno quindi confrontato qualità dello sperma, livelli ormonali, struttura tissutale e un insieme di “sistemi di allarme” molecolari nei testicoli che percepiscono lo stress e innescano infiammazione e suicidio cellulare.
Come la sitagliptina ha attenuato lo stress cellulare e l’infiammazione
Il paclitaxel ha spinto i testicoli in uno stato di stress ossidativo e intracellulare: i livelli di prodotti dannosi (misurati come malondialdeide) sono aumentati, mentre le difese naturali come il glutatione ridotto e l’enzima catalasi sono diminuite. In profondità nelle cellule, il reticolo endoplasmatico — la “fabbrica” del ripiegamento proteico — ha attivato una via di pericolo chiamata PERK–CHOP, segnale che lo stress prolungato sta indirizzando le cellule verso la morte. Contemporaneamente, un complesso proteico infiammatorio (NLRP3) è diventato altamente attivo, aumentando mediatori infiammatori come l’interleuchina‑1β e attivando una cascata di proteine coinvolte nella morte cellulare, tra cui il citocromo c e la caspasi‑3. La sitagliptina ha invertito gran parte di questi effetti. Entrambe le dosi hanno ridotto i danni ossidativi e ripristinato le difese antiossidanti. Hanno ridotto in modo marcato l’attivazione della via di stress PERK–CHOP e frenato l’infiammazione e l’apoptosi guidate da NLRP3. Una proteina protettiva chiamata Sestrin2, che aiuta a neutralizzare le specie reattive e che è stata collegata a una migliore salute degli spermatozoi, è stata aumentata dalla sitagliptina sia a livello genico sia proteico.
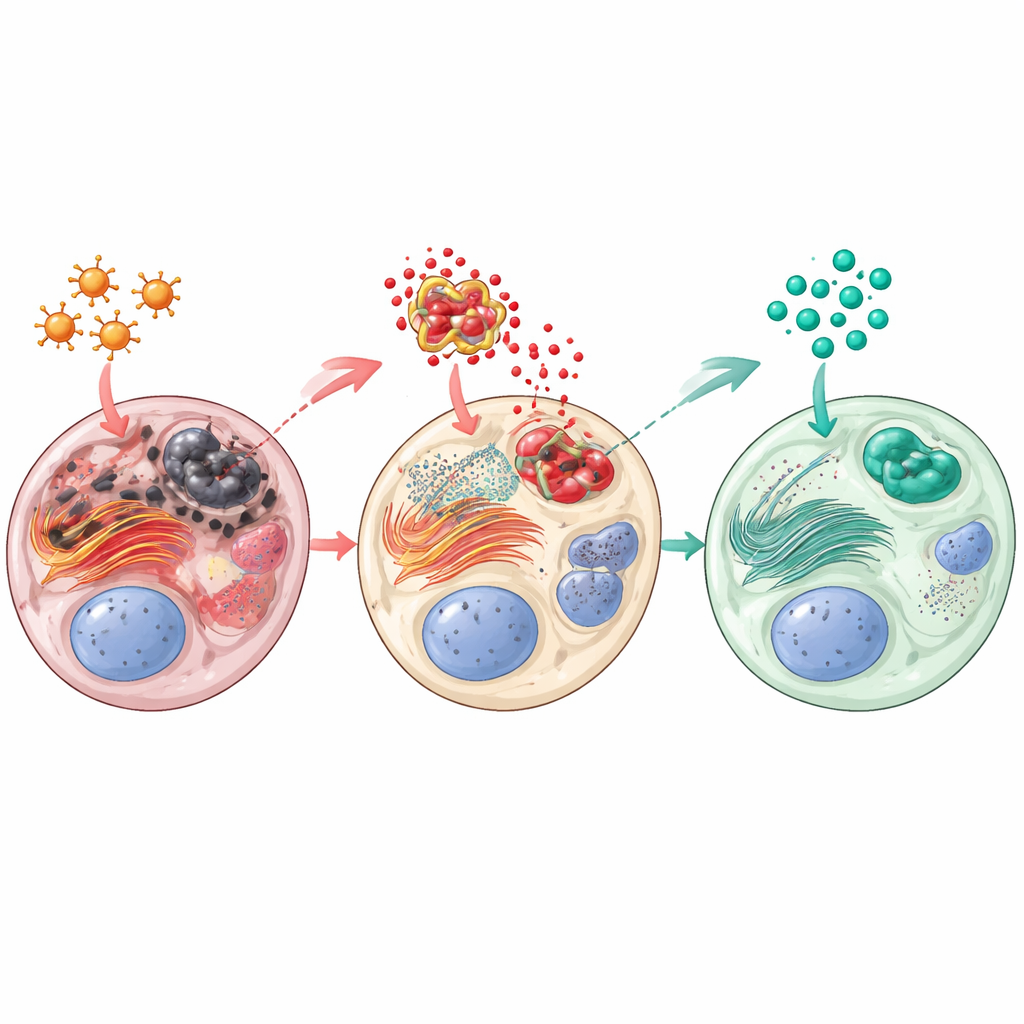
Sperma migliore, tessuto più sano, ormoni più forti
I miglioramenti biochimici si sono tradotti in benefici funzionali tangibili. I ratti trattati con sitagliptina dopo paclitaxel hanno mostrato conteggi spermatici più elevati, motilità migliore e meno spermatozoi anomali rispetto agli animali trattati solo con paclitaxel, con la dose più alta di sitagliptina che si è avvicinata maggiormente ai valori normali. Testosterone e 17β‑idrossisteroide deidrogenasi sono aumentati, suggerendo un recupero della produzione di steroidi da parte delle cellule di Leydig. Sia con il microscopio ottico sia con quello elettronico, i testicoli trattati con sitagliptina mostravano tubuli seminiferi più ordinati, più cellule di Leydig, strati cellulari più spessi e sani e meno distorsioni strutturali. Complessivamente, il farmaco ha contribuito a preservare l’architettura e la funzione necessarie alla continua produzione di spermatozoi.
Cosa potrebbe significare per gli uomini in chemioterapia
Questo lavoro animale suggerisce che la sitagliptina può attenuare in modo significativo il danno testicolare indotto da paclitaxel, silenziando una rete di segnali dannosi — stress ossidativo, stress del ripiegamento proteico intracellulare, infiammazione e morte cellulare programmata — in gran parte tramite l’aumento di Sestrin2 e la riduzione dell’asse PERK/CHOP/NLRP3. Poiché la sitagliptina è già impiegata in clinica per il diabete, emerge come un candidato realistico da testare come possibile coadiuvante protettivo della fertilità negli uomini che ricevono paclitaxel, in particolare in quelli con diabete. Gli autori sottolineano che sono ancora necessari studi sull’uomo, ma i risultati aprono una possibilità promettente: una pillola familiare potrebbe un giorno aiutare i pazienti oncologici a conservare non solo la vita, ma anche la possibilità di diventare padri.
Citazione: El-Beheiry, K.M., El-Shitany, N.A., El-Sayad, M.ES. et al. Potential gonadal-beneficial effect of sitagliptin against paclitaxel-induced testicular dysfunction via mediating PERK/CHOP/NLRP3/Sestrin2 signaling pathway. Sci Rep 16, 9090 (2026). https://doi.org/10.1038/s41598-026-40511-9
Parole chiave: paclitaxel, sitagliptin, fertilità maschile, stress ossidativo, tossicità testicolare