Clear Sky Science · it
La perdita dell’omeostasi dei neutrofili è associata ad alterazioni funzionali dei mitocondri nei pazienti con COVID-19 critico
Perché questo è importante per i pazienti con COVID-19
Oggi la maggior parte delle persone sa che il COVID-19 è più di una semplice infezione polmonare, ma il modo in cui il virus ribalta le difese dell’organismo è ancora in parte sconosciuto. Questo studio analizza da vicino i neutrofili, un tipo comune di globuli bianchi, nei pazienti con COVID-19 in condizioni critiche in terapia intensiva. Esaminando come queste cellule sopravvivono, muoiono e utilizzano i loro piccoli “impianti energetici” interni (i mitocondri), i ricercatori rivelano uno schema di neutrofili iperattivi e persistenti che potrebbe contribuire a spiegare l’infiammazione prolungata, il danno al sangue e lesioni d’organo nella forma grave della malattia.
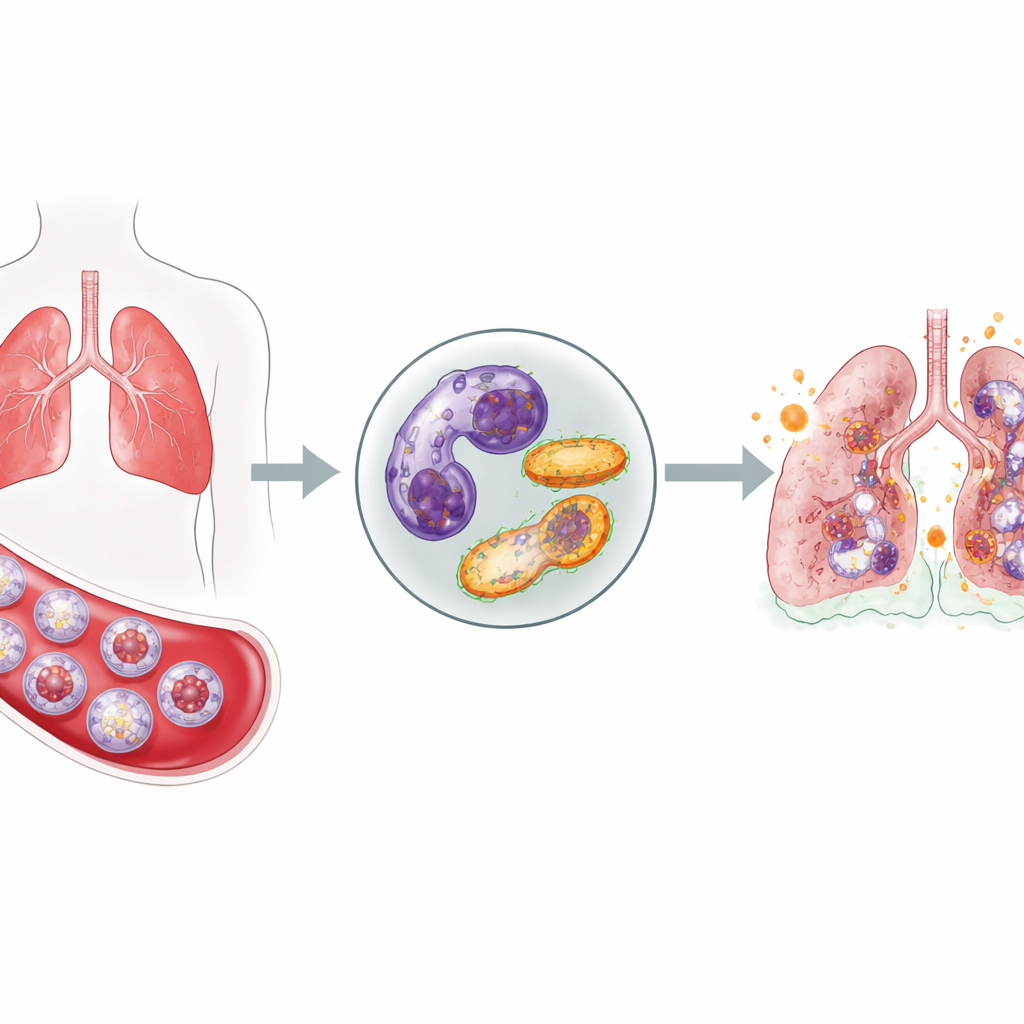
Cellule di prima linea che non si ritirano
I neutrofili sono tra i primi a intervenire contro le infezioni: arrivano rapidamente nel sangue, migrano nei tessuti e rilasciano molecole tossiche per uccidere i microbi invasori. Normalmente, dopo aver svolto il loro compito, si autodistruggono silenziosamente e vengono rimosse, evitando così danni ai tessuti sani. Nei pazienti critici con COVID-19 il quadro è molto diverso. Rispetto ai volontari sani, questi pazienti mostrano un’impennata di neutrofili nel sangue e, cosa importante, molti di questi sono cellule immature espulse in fretta dal midollo osseo. Contemporaneamente, vari test indicano che un numero minore di neutrofili entra nella loro normale morte programmata, suggerendo che queste cellule aggressive permangono più a lungo del dovuto.
Segnali genetici sottili ma un chiaro schema di sopravvivenza
I ricercatori hanno anche analizzato piccole molecole regolatorie chiamate microRNA nei neutrofili di sopravvissuti e non sopravvissuti in terapia intensiva. Alcune di queste molecole risultavano alterate in modi che, sulla carta, puntano a percorsi disturbati che controllano la morte cellulare e l’equilibrio del calcio. Tuttavia, quando hanno misurato indicatori diretti della morte cellulare non hanno riscontrato grandi differenze tra sopravvissuti e non sopravvissuti: entrambi i gruppi mostravano una ridotta autodistruzione dei neutrofili rispetto alle persone sane. Questo significa che i profili di microRNA vanno considerati più come spunti per studi futuri che come indicatori certi di esito, e sottolineano che il fallimento complessivo dei neutrofili nel disattivarsi è una caratteristica comune della COVID-19 grave.
Spostamenti del calcio e “impianti energetici” sovraccarichi
Per capire perché i neutrofili non morivano nei tempi previsti, il gruppo si è concentrato su due sistemi strettamente collegati all’interno delle cellule: i segnali del calcio e i mitocondri. Gli ioni calcio fungono da piccoli interruttori per molte decisioni cellulari, inclusa l’autodistruzione. I ricercatori hanno osservato che i neutrofili dei pazienti con COVID-19 grave avevano meno calcio libero all’interno, insieme a livelli ridotti di proteine chiave che normalmente aiutano a trasferire il calcio nei mitocondri e ad aprire una valvola di sicurezza che può innescare la morte cellulare. Allo stesso tempo, i mitocondri risultavano inusualmente “carichi”, con un gradiente elettrico più alto attraverso le membrane e un consumo di ossigeno aumentato, in particolare attraverso una delle principali vie respiratorie. Invece di spegnersi, questi mitocondri iperattivi producevano più molecole reattive dell’ossigeno, che possono danneggiare i tessuti circostanti e alimentare l’infiammazione.
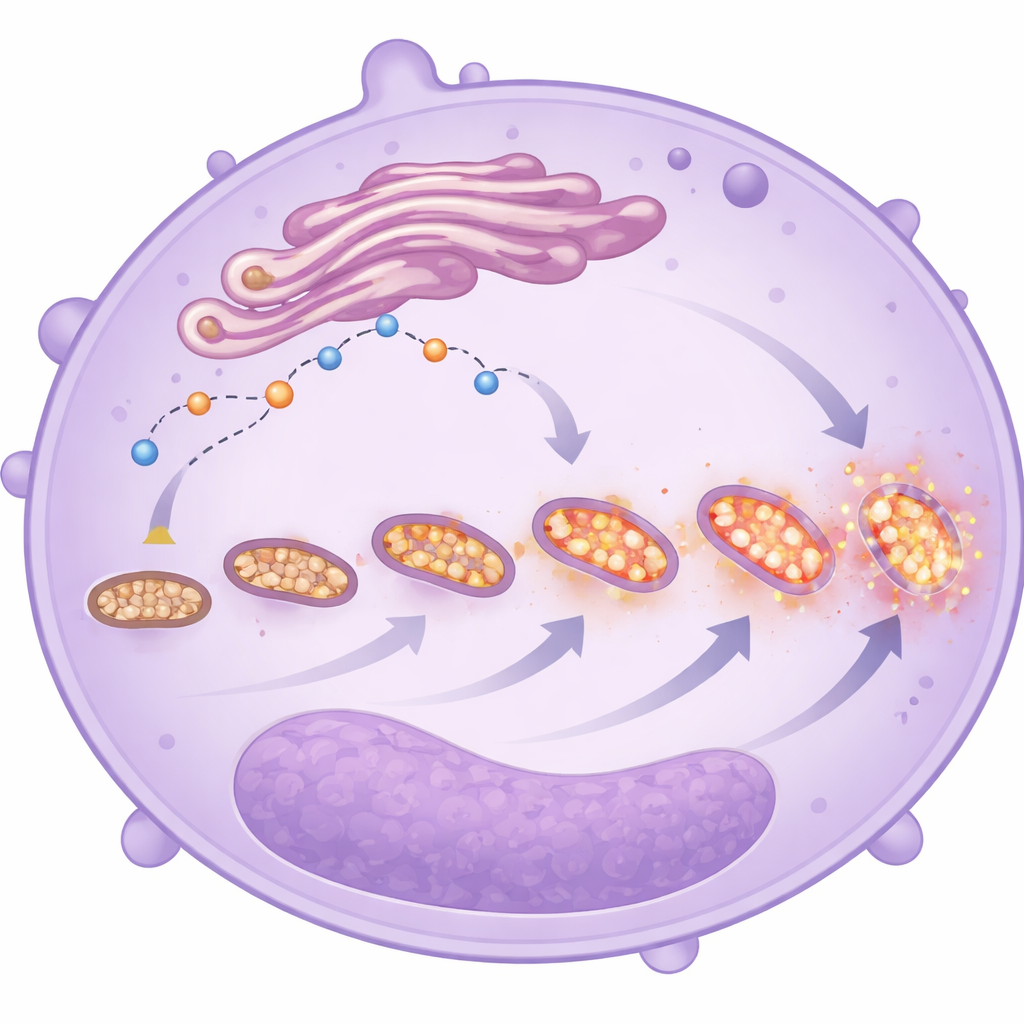
Mitocondri stressati e frammentati
Immagini al microscopio elettronico e coloranti fluorescenti hanno offerto uno sguardo più ravvicinato alla forma e al comportamento di questi mitocondri. Nei neutrofili dei pazienti più gravi, i mitocondri erano più numerosi ma più piccoli e più frammentati—caratteristiche che spesso indicano stress. Queste cellule mostravano inoltre livelli più elevati di specie reattive dell’ossigeno mitocondriali, indipendentemente dall’esito del paziente. Insieme alla gestione alterata del calcio e al ritardo della morte cellulare, questi cambiamenti descrivono neutrofili che hanno modificato la loro strategia energetica: invece di affidarsi principalmente alla semplice degradazione degli zuccheri, fanno maggior ricorso al metabolismo mitocondriale, soprattutto nelle cellule immature. Questo cambiamento può aumentare la loro capacità di migrare, persistere e rilasciare molecole dannose nei polmoni e in altri organi, anche se lo studio non può provare che siano la causa diretta di esiti peggiori.
Cosa potrebbe significare per le cure future
In termini semplici, lo studio suggerisce che nella COVID-19 critica i neutrofili diventano troppi, troppo giovani e troppo difficili da spegnere. I loro segnali intracellulari di calcio e i mitocondri sono rimodulati in modo da mantenerli vivi e altamente attivi, producendo ondate di sostanze ossigeno‑reattive dannose. Pur essendo uno studio osservazionale che non dimostra nesso di causa-effetto, evidenzia diversi possibili “manopole di controllo” in queste cellule—come regolatori del calcio e checkpoint mitocondriali—che un giorno potrebbero essere mirati per riportare delicatamente i neutrofili a un comportamento normale. Se la ricerca futura confermerà queste idee, trattamenti che ristabiliscono l’adeguato spegnimento dei neutrofili o che calmano i loro mitocondri sovraccarichi potrebbero contribuire a ridurre i danni collaterali causati da queste cellule cruciali durante la COVID-19 grave e, possibilmente, in altre patologie critiche.
Citazione: Elkhodiry, A.A., Yasseen, B.A., El-sayed, H. et al. Disruption of neutrophil homeostasis is associated with functional alterations in mitochondria of critically ill COVID−19 patients. Sci Rep 16, 7838 (2026). https://doi.org/10.1038/s41598-026-38741-y
Parole chiave: COVID-19, neutrofili, mitocondri, infiammazione, malattia critica